Т е о р е т и ч е с к а я ч а с т ь
1. Окислительные свойства перманганата калия KMnO4 в различных cредах (кислой, нейтральной и щелочной)
Перманганат калия KMnO4 – один из наиболее распространенных сильных окислителей, широко использующийся в химической промышленности, в лабораторной практике и в медицине. Состав продуктов его восстановления зависит, прежде всего, от среды растворов, в которых оно осуществляется. При этом, как правило:
1) В кислой среде KMnO4 восстанавливается до соединений 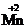 (MnSO4, MnCl2):
(MnSO4, MnCl2):
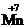 + 5e– →
+ 5e– → 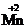 или
или 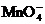 + 8H+ + 5e– →
+ 8H+ + 5e– → 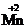 + 4H2O; E° = 1,51 B.
+ 4H2O; E° = 1,51 B.
2) В нейтральной среде KMnO4 восстанавливается до соединений 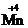 , состав которых условно выражается формулой MnО2:
, состав которых условно выражается формулой MnО2:
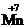 + 3e– →
+ 3e– → 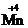 или
или 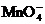 + 2H2О + 3e– → MnО2 + 4ОH—; E° = 0,60 B.
+ 2H2О + 3e– → MnО2 + 4ОH—; E° = 0,60 B.
3) В щелочной средеKMnO4 восстанавливается до соединений 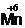 (K2MnO4, Na2MnO4):
(K2MnO4, Na2MnO4):
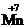 + 1e– →
+ 1e– → 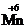 или
или 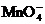 + 1e– →
+ 1e– → 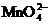 ; E° = 0,56 B.
; E° = 0,56 B.
При этом происходит резкое изменение окраски растворов в соответствии с данными таблицы 1:
Таблица 1. Окраска соединений марганца в зависимости от степени его окисления
| Степень окисления марганца | Форма существования в растворе или в осадке | Примеры соединений | Окраска раствора или осадка |
| +7 | 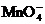 (р-р) (р-р) | KMnO4, NaMnO4 | розово-фиолетовая |
| +6 | 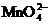 (р-р) (р-р) | K2MnO4, Na2MnO4 | изумрудно-зелёная |
| +4 |  (осадок) (осадок) | MnО2 | бурая |
| +2 | 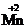 (р-р) (р-р) | MnSO4, MnCl2 | практич. бесцветная |
Окислительно-восстановительные свойства пероксида водорода
Поскольку в молекулах пероксида водорода атомы кислорода находятся в промежуточной степени окисления (–1), то это вещество, в зависимости от условий, может окисляться до простого вещества кислорода ( 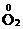 ), восстанавливаться до воды (
), восстанавливаться до воды ( 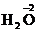 ) или диспропорционировать с одновременным образованием указанных веществ.
) или диспропорционировать с одновременным образованием указанных веществ.
Внутримолекулярное окисление-восстановление
Если в составвещества входят одновременно частицы-восстановители и частицы-окислители, оно может подвергаться внутримолекулярному окислению-восстановлению. К таким реакциям относится, например, реакция термического разложения дихромата аммония ( 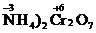 . При нагревании этого вещества начинается ОВР за счёт того, что содержащиеся в нём частицы
. При нагревании этого вещества начинается ОВР за счёт того, что содержащиеся в нём частицы 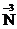 являются восстановителями, а частицы
являются восстановителями, а частицы 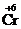 –окислителями.
–окислителями.
Диспропорционирование и конпропорционирование
Реакции диспропорционирования (дисмутации) – ОВР внутримолекулярного типа, в ходе которых одновременно окисляются и восстанавливаются атомы одного и того же элемента, входящие в состав одного исходного вещества («самоокисление-самовосстановление»).
Пример: 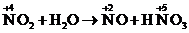 . В этой реакции внутримолекулярного типа частицы
. В этой реакции внутримолекулярного типа частицы 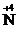 одновременно восстанавливаются до
одновременно восстанавливаются до 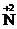 и окисляются до
и окисляются до 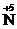 .
.
Реакции конпропорционирования (конмутации) – ОВР межмолекулярного типа, в ходе которых одновременно окисляются и восстанавливаются атомы одного и того же элемента, входящие в состав разных исходных веществ.
Пример: 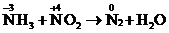 . В этой реакции межмолекулярного типа частицы
. В этой реакции межмолекулярного типа частицы 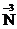 окисляются, а частицы
окисляются, а частицы 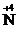 восстанавливаются до
восстанавливаются до 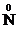 .
.
