К лабораторно-практическим занятиям по общей химии
К лабораторно-практическим занятиям по общей химии
Федеральное агентство по здравоохранению
и социальному развитию
Северный научный центр РАМН
Северный государственный медицинский университет
Методические рекомендации
к лабораторно-практическим
занятиям по общей химии
Архангельск
Северный государственный медицинский университет
2009 год
Печатается по решению центрального
координационно-методического совета
Северного государственного медицинского
университета
Под общей редакцией А.Е. Щеголева, канд. хим. наук, доцента кафедры общей и биоорганической химии СГМУ
Авторы-составители: Е.А. Айвазова, канд. биол. наук, зав. кафедрой общей и биоорганической химии; Г.П. Суханова, канд. тех. наук, доцент кафедры общей и биоорганической химии; Е.А. Журавлёва, канд. биол. наук, ст. преп. кафедры общей и биоорганической химии;Т.Г. Антонова, ст. преп. кафедры общей и биоорганической химии; А.В. Лоскутова, ассистент кафедры общей и биоорганической химии; О.Е. Титова, ассистент кафедры общей и биоорганической химии;А.Е. Щеголев, канд. хим. наук, доцент кафедры общей и биоорганической химии
Рецензенты: Н.А. Матонина, ассистент кафедры
общей и биоорганической химии СГМУ;
Н.Б. Чагина, канд. техн. наук, доцент кафедры химии ПГУ имени М.В. Ломоносова
Методические рекомендации содержат материал для подготовки студентов к лабораторно-практическим занятиям по общей химии для студентов лечебного, педиатрического, стоматологического факультетов и медико-профилактического отделения факультета медицинской профилактики и экологии. Приведены контрольные вопросы и задачи для самостоятельного решения.
Могут быть полезны также и студентам других факультетов медицинских университетов.
© Щеголев А.Е., 2009
© Северный государственный
медицинский университет, 2009
Весь изучаемый материал по общей химии распределён по главам, соответствующим тематике лабораторно-практичес-ких занятий. Основой для изучения общей химии служат учебники и учебные пособия, приведённые в списке литературы, и лекции по общей химии, читаемые на данных факультетах.
Занятие 1 (Вводное).
Содержание занятия:
1. Инструктаж по технике безопасности.
ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ ПРИ РАБОТЕ СТУДЕНТОВ В ЛАБОРАТОРНЫХ ПРАКТИКУМАХ СГМУ
Спешка, небрежность в работе, незнание приемов обращения с реактивами и приборами делают работу в лаборатории опасной!!!
· Работать в лабораторных практикумах кафедры разрешается только в халатах с длинными рукавами.
· Рабочее место следует содержать в чистоте, не загромождать его посудой и посторонними предметами.
· Приступая к работе, студент должен:
- уяснить методику работы;
- проверить соответствие взятых веществ веществам, указанным в описании работы.
· Все процедуры при выполнении практической работы необходимо производить только на своем рабочем месте или вытяжном шкафу. Запрещается перемещение ёмкостей с реактивами из вытяжного шкафа.
· Имеющиеся на рабочих местах реактивы необходимо использовать только по назначению.
· Отмеривание реактивов следует производить с помощью калиброванной посуды или пипеток с грушами. Категорически запрещается отмеривать жидкие реагенты и биологические жидкости путем их всасывания в пипетку ртом !!!
· Будьте особенно осторожны в обращении с концентрированными растворами кислот, щелочей, огнеопасными и ядовитыми веществами.
· Во избежание разбрызгивания жидкости (что грозит получением ожогов) концентрированные кислоты и щелочи следует добавлять к воде или водному раствору, а не наоборот.
· Пипетку с концентрированной кислотой надо приподнять и подержать над склянкой, пока кислота с наружной стенки пипетки не стечет в склянку, и только затем следует перенести пипетку к рабочей пробирке.
· При попадании кислоты (щелочи) на кожу рук, лица или одежду нужно немедленно промыть это место под сильной струей воды, а затем протереть ватой, смоченной 2% раствором гидрокарбоната натрия (уксусной кислоты), а затем насухо вытереть.
· Не оставляйте открытыми склянки с жидкостями и банки с сухими реактивами. Склянок из штативов не вынимать!!!
· Пролитые или рассыпанные реактивы немедленно удалите с рабочей поверхности стола.
· Правильно пользуйтесь нагревательными приборами и строго соблюдайте правила безопасности при нагревании.
· Нагревательные приборы должны стоять на термоизолирующей прокладке – асбестовой, керамической, мраморной.
· При нагревании растворов в пробирках отверстие пробирки направлять в сторону от себя и от работающих рядом товарищей; не заглядывать в пробирку сверху, т.к. возможен выброс раствора.
· При упаривании раствора и прокаливании вещества на песчаной бане тигли и фарфоровые чашки снимать с бани только с помощью тигельных щипцов.
· Пробирку с веществом слегка прогрейте всю, затем нагревайте пробирку ниже уровня жидкости в ней.
· При первых признаках отравления (головокружение, тошнота и т.д.) пострадавшего вывести на свежий воздух и дать подышать нашатырный спирт.
· При всех несчастных случаях обращаться к преподавателю или лаборанту.
Категорически запрещается выполнять в лаборатории экспериментальные работы, не связанные с выполнением учебного практикума!!!
Лабораторная работа
Выполнение демонстрационных опытов (в процессе обсуждения теоретического материала).
Опыт 1. Определение осмотического давления раствора сахарозы.
Осмометр вынимают из штатива. Затем, наклонив его в сторону боковой (широкой) трубки, через отверстие этой трубки с помощью пипетки заполняют исследуемым раствором сахара. Продолжая держать осмометр в наклоненном положении, боковую (широкую) трубку плотно закрывают пробкой так, чтобы в ней не оставалось пузырьков воздуха, а уровень раствора в капилляре был возможно ниже. Заполненный осмометр погружают в стакан с дистиллированной водой до нижнего уровня капилляра и закрепляют в штативе. Если в течение первых 30 минут высота раствора в капилляре не увеличится, заменяют осмометр. Через 1.5–2 часа от начала опыта (когда осмос прекратится) измеряют высоту подъема раствора в капиллярной трубке от поверхности воды в стакане. Осмотическое давление раствора рассчитывают по формуле:
Росм. = h∙ ρ∙ g (Па)
где: h – высота подъема раствора в капилляре (м);
ρ– плотность исследуемого раствора (кг/м3);
g – ускорение свободного падении я тела, (м/с2).
Результаты опыта оформляют в виде таблицы, приводя подробный рисунок осмометра и расчет осмотического давления.
| Продолжительность осмоса | h, м | ρ, кг/м3 | Р, Па |
Опыт 2. Рост искусственной «клетки» Траубе.
В цилиндр наливают 150–200 мл раствора СиSО4 и бросают кристаллик К4[Fe(CN)6]. За счет реакции
2 CuSO4 + K4[Fe(CN)6] = Cu2[Fe(CN)6] + 2 K2SO4
на поверхности кристалла образуется сплошная пленка гексацианоферрата(II) меди, пропускающая воду, но задерживающая частицы солей. Вследствие равности концентраций внутри оболочки и вне ее вода начинает поступать внутрь «клетки». Оболочка растягивается и разрывается в самом слабом месте. На этом месте вновь возникает пленка из Cu2[Fe(CN)6], и так постепенно развивается вытянутая полость, очертаниями напоминающая водоросль или гидру.
Опыт 3. Гемолиз эритроцитов.
Берут 3 пробирки. В первую наливают из бюретки 3 мл дистиллированной воды, во вторую (пипеткой) 3 мл раствора хлорида натрия с массовой долей NaCl 0.2%, в третью (пипеткой) – 3 мл раствора хлорида натрия с массовой долей NaCl 0.9%; в каждую пробирку вносят по 2 капли крови и встряхивают.
Через полчаса отмечают, в каких пробирках произошел гемолиз эритроцитов.
Работу оформляют в виде таблицы.
| Содержание пробирки | Что наблюдали | Вывод (отсутствие или наличие гемолиза) |
| 3 мл Н2О + 2 капли крови 3 мл р-ра NaCL c ω = 0.2 % + 2 капли крови 3 мл р-ра NaCL c ω = 0.9 % + 2 капли крови |
Контрольные вопросы и задачи
1. Какие свойства растворов называются коллигативными?
2. Что такое полупронецаемые мембраны? Приведите примеры полупроницаемых мембран.
3. Дайте определение осмоса и осмотического давления. Какие существуют методы определения осмотического давления?
4. Какое из перечисленных утверждений верно: при одинаковой молярной концентрации и температуре максимальное осмотическое давление имеет разбавленный раствор:
а) хлорида натрия; б) хлорида калия; в) хлорида кальция,
г) глюкозы.
5. Будут ли изотоничны водные растворы двух нелетучих неэлектролитов, если температуры и молярные концентрации растворов одинаковы? Ответ мотивируйте.
6. Будут ли изотоничны водные растворы двух нелетучих неэлектролитов (М1 > М2), если температуры растворов и массовые доли этих веществ в растворах одинаковы? Если, на ваш взгляд, растворы неизотоничны, то в котором из них — первом или втором — осмотическое давление выше? Почему?
7. Как будет меняться во времени осмотическое давление подкисленного раствора сахарозы при 80°С? Ответ мотивируйте.
8. Опишите поведение эритроцитов при 37°С в водных растворах следующих веществ:
а) фруктозы, ω = 2%, плотность 1.006 г/мл;
б) сульфата натрия, ω = 16%, плотность 1.151 г/мл, α = 1;
в) мочевины, С = 0.3 моль/л.
9. Раствор, полученный растворением 50 г органического вещества в 1300 мл воды обладает при 20°С осмотическим давлением 0.01 атм и плотностью 1.01 г/мл. Определите молярную массу органического вещества.
10. Какую массу глюкозы следует взять для приготовления
0.5 л водного раствора, изотоничного плазме крови при температуре 37°С?
11. При 20°С смешали 1 л раствора сахарозы, осмотическое давление которого 2.4 атм с 3 л раствора KCl, осмотическое давление которого 4.8 атм. Найти осмотическое давление смешанного раствора, если αHCl = 1.
12. Будут ли изотоничны плазме крови при температуре 37°С следующие растворы:
а) 5%-й водный раствор глюкозы (ρ = 1.08 г/моль);
б) водный раствор, содержащий в 0.1 л раствора дезоксирибозу массой 1.34 г;
в) раствор фруктозы с молярной концентрацией 0,303 моль/л;
г) водный раствор карбоната калия с массовой долей К2СО3 0.7% и плотность 1.005 г/мл (αК2СО3 = 1).
13. Рассчитайте осмотическое давление при 37°С
(R = 0,082 л·атм/К):
а) 0.1 М раствора СаCl2 (αСаCl2 = 1)
б) внутриклеточной жидкости, если состав раствора (моль/л): [Na+] =35; [K+] =115; [Ca2+] =5; [Clˉ] = 20; [HCO3ˉ] = 20; [H2PO4ˉ] = 100; [SO42-] =10.
в) раствора, в 2 л которого содержится 90 г глюкозы
(М =180 г/моль).
Занятие 13. КОЛЛИГАТИВНЫЕ СВОЙСТВА РАСТВОРОВ.
закон рауля
Цель занятия:
Сформировать системные знания о коллигативных свойствах разбавленных растворов; научиться использовать закон Рауля для расчета соответствующих параметров разбавленных растворов, в том числе биологических жидкостей.
Содержание занятия:
1. Обсуждение теоретических вопросов по теме.
2. Решение задач.
3. Тестовый контроль по теме «Коллигативные свойства растворов».
Вопросы, предлагаемые для обсуждения на занятии:
1. Насыщенный пар, давление насыщенного пара над чистым растворителем. Относительное понижение давления насыщенного пара растворителя над разбавленным раствором нелетучего неэлектролита; закон Рауля.
2. Температуры кипения и замерзания растворов. Относительное повышение температуры кипения и понижение температуры замерзания (депрессии) разбавленных растворов неэлектролитов по сравнению с чистыми растворителями; следствия из закона Рауля. Эбуллиоскопическая и криоскопическая постоянные, их физический смысл.
3. Отклонение растворов электролитов от закона Рауля и его следствий. Изотонический коэффициент.
4. Взаимосвязь между коллигативными свойствами растворов. Осмометрия, криометрия и применение их в медико-биологических исследованиях.
Контрольные вопросы и задачи
1. Объясните с помощью принципа смещения химического равновесия повышение температуры кипения и понижение температуры замерзания раствора по сравнению с чистым растворителем.
2. Что называется давлением насыщенного пара? Как оно изменяется над раствором по мере увеличения концентрации нелетучего неэлектролита?
3. Не производя расчетов, укажите, какой из трех растворов с одинаковой массовой долей – хлорида бария, хлорида магния, хлорида кальция – имеет минимальную и максимальную температуру замерзания. Ответ мотивируйте.
4. Барбитуровая кислота, производные которой имеют большое значение в медицине, состоит (по массе) из 42.11 % углерода, 3.58% водорода, 42.11% кислорода и 12.28% азота. Температура кипения раствора, содержащего 10.21 г барбитуровой кислоты в 360 г ССl4, на 1.25 К выше температуры кипения чистого ССl4. Какова молярная масса и молекулярная формула барбитуровой кислоты (ЕССl4 = 5.02).
5. Многие моносахариды отвечают простейшей формуле Сn(H2O)n. Выведите молекулярную формулу ксилозы, водный раствор которой с массовой долей вещества 1.96% замерзает при -0,248°С.
6. Чему равна температура замерзания водного раствора, содержащего глюкозу с массовой долей 3%, если Кводы = 1,86.
7. Какую массу сахарозы следует растворить в 250 г воды, чтобы получить раствор, кипящий при 100.2°С. При какой температуре будет замерзать этот раствор?
8. Понижение температуры замерзания плазмы крови равно 0.56°С. Рассчитайте массу воды, которую необходимо добавить к 100 г 10% раствора NaCl, для получения раствора, изотоничного крови при 37°С.
9. Как можно вычислить величину осмотического давления раствора нелетучего неэлектролита, если известна депрессия (∆Тзам.) раствора?
Занятие 14. ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ. ПОТЕНЦИОМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ рН
Цель занятия:
Научиться составлять схему гальванического элемента, представлять электронные уравнения процессов, протекающих на электродах. Научиться определять рН исследуемых растворов.
Содержание занятия:
1. Обсуждение теоретических вопросов по теме занятия.
2. Решение задач.
3. Выполнение лабораторной работы.
Вопросы, предлагаемые для обсуждения на занятии:
1. Сущность метода потенциометрии и его медико-биологическое значение.
2. Механизм возникновения электродного потенциала.
3. Уравнение Нернста. Зависимость электролитного потенциала от различных факторов. Стандартный электродный потенциал. Ряд напряжений металлов.
4. Классификация электродов.
5. Устройство электродов I и II рода. Стеклянный и хлорсеребряный электроды.
6. Гальванический элемент: схема, электродные реакции, расчет ЭДС.
7. Редокс-электроды. Уравнение Петерса. Биологическое значение редокс-потенциала
8. Диффузные и мембранные потенциалы, их биологическое значение.
Лабораторная работа
Потенциометрическое определение рН исследуемого раствора при помощи стеклянного электрода
При измерении рН растворов с помощью приборов «ЭВ-74», «рН-340», «рН-121» составляют гальванический элемент из стеклянного и хлорсеребряного электродов, погруженных в исследуемый раствор.
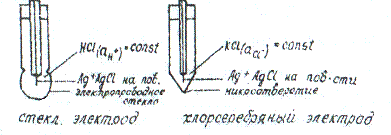
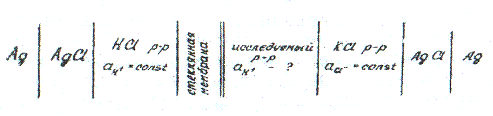
Схема гальванического элемента
Указания для выполнения и оформления работы
(иономер ЭВ- 74)
I. Включение прибора(его следует включить за 30 мин до начала работы).
1. Проверить заземление прибора – клемма на задней стенке прибора должна быть присоединена к линии заземления.
2. Нажать клавиши «t°» и «-1÷19» на лицевой панели прибора.
3. Подключить прибор к сети 220 V с помощью шнура и включить тумблер «сеть» на лицевой панели прибора. При этом должна засветиться индикаторная лампочка.
II. Подготовка гальванического элемента к работе– через 15 мин после включения прибора.
1. Получить у преподавателя исследуемый раствор.
2. Аккуратно приподнять вверх стаканчик с дистиллированной водой, в который опущены электроды и термометр, отвести в сторону поворотный столик – подставку и освободить электроды, опустив стакан вниз.
3. В чистый стакан налить до отметки исследуемый раствор и промыть им электроды, осторожно поднимая вверх стаканчик с раствором и стараясь при этом не касаться электродов.
4. Вылить из стаканчика исследуемый раствор, налить до отметки новую порцию его, ввести электроды в раствор, столик – подставку вернуть в начальное положение и поставить на него стакан. Электроды при этом должны быть погружены в раствор на 2 см.
5. Проверить подключение гальванического элемента к прибору «ЭВ-74»: штекер, которым заканчивается тонкий провод от вспомогательного электрода, должен быть подключен до упора в гнездо «всп» на задней стенке прибора, а штекер, которым заканчивается толстый кабель от измерительного электрода, подключен до упора в гнездо «изм», расположенное рядом с гнездом «всп».
III. Установка температуры раствора
1. Проверить установку переключателя рода термокомпенсации на задней стенке прибора в положении «ручн». Такое включение необходимо при работе с растворами, имеющими комнатную температуру (20±10°С).
2. Нажать клавишу малого диапазона «14÷19».
3. Ручкой « температура раствора» на лицевой панели установить по верхней шкале показывающего прибора (оцифровка 0÷100) температуру, соответствующую показаниям термометра, погруженного в исследуемый раствор.
IV. Определение рН (его следует проводить через 10 мин после подготовки гальванического элемента к работе и все полученные данные сразу же внести в таблицу).
1. Нажать клавиши «анионы/катионы», «рН» и «-1÷19» на лицевой панели прибора.
2. По нижней шкале показывающего прибора (оцифровка -1÷19) найти и записать отсчет (рН ориентировочное).
3. Нажать клавишу одного из узких диапозонов рН (-1÷4; 4÷ 9; 9÷14; 14÷19), в пределах которого находится рН ориентир.
Внимание!Дальнейшее определение и расчет рН исследуемого раствора проводят по-разному (п. 4 или п. 5) в зависимости от выбранного узкого диапазона.
4. Если нажата клавиша «-1÷4», то по верхней шкале прибора (оцифровка «-1÷4») находят отсчет с точностью до сотых долей единицы и записывают его (рНиссл.). Отключают узкий диапазон, нажав клавишу «-1÷19». Повторяют определение отсчета еще 2 раза, затем приглашают преподавателя к рабочему месту для проверки показаний прибора и результата работы
5. Если нажата одна из клавиш «4÷9», «9÷14», «14÷19», то по верхней шкале (оцифровка 0÷5) находят отсчет с точностью до сотых долей единицы и записавают его (рН1). Отключают узкий диапазон, нажав клавишу «1÷19». Повторяют определение отсчета еще 2 раза. Расчет рН исследуемого раствора (рНиссл.) выполняют по формуле:
рНиссл. = рНнач. + рН1,
где рНнач — значение рН, соответствующее началу выбранного узкого диапазона. Затем к рабочему месту приглашают преподавателя для проверки показаний прибора и результата работы.
V. Окончание работы.
1. Отключить тумблер «сеть» на лицевой панели прибора, выключить прибор из сети.
2. Осторожно заменить в гальваническом элементе стаканчик с исследуемым раствором на стаканчик с дистиллированной водой, аккуратно приподняв стакан вверх и отводя в сторону столик–подставку.
3. Оформить отчет по работе. При оформлении работы:
а) привести подробные схемы рисунков стеклянного и хлорсеребряного электродов, схему исследуемого гальванического элемента.
б) Привести таблицу.
| 1. Температура растворы | t, °C |
| 2. Широкий диапазон измерения рН | -1 ÷ 19 |
| 3. Отсчет по шкале широкого диапазона | pHориент. |
| 4. Узкий диапазон измерения рН (соответствует положению тумблера «пределы измерения») | |
| 5. Отсчеты по шкале узкого диапазона «рН» с точностью до сотых долей еденицы | 1. 2. 3. рН1(ср.) = |
| 6. рНиссл. = рНнач. + рН1, где рНнач – значение рН, соответствующее началу выбранного узкого диапазона. | рНиссл. = |
Контрольные вопросы и задачи
1. Рассчитайте электродные потенциалы магния в растворе его соли при концентрации иона Mg2+ 0,1; 0,01 и 0,001 моль/л при температуре 25°C.
2. Приведите схему медно-никелевого гальванического элемента, определите знаки электродов, составьте уравнения реакций, протекающих на электродах, выведите формулу ЭДС и рассчитайте ЭДС данного гальванического элемента, если С (Cu2+) = 10-2 моль/л, а С (Ni2+) = 10-4 моль/л.
3. В каком направлении будут перемещаться электроны во внешней цепи следующих гальванических элементов:
а) Mg | Mg2+|| Pb2+ | Pb
б) Pb | Pb2+ || Cu2+ | Cu
в) Сu | Cu2+ || Ag+ | Ag
4. Потенциал водородного электрода в некотором растворе равен -118 мВ. Вычислите активность ионов водорода в этом растворе.
5. Никелевые пластины опущены в растворы NiSO4 c концентрациями 0.01 и 0.05 моль/л. Привести схему данного гальванического элемента, электродные реакции, рассчитать ЭДС.
6. Приведите схемы гальванических элементов, с помощью которых можно определить стандартный электродный потенциал металла.
Решение.
n(NaOН) 0,04 моль
С(Х) = ———————— = ————— = 0.2 моль/л;
V(раствора NaOН) 0.2 л
в) Молярная концентрация эквивалента
Молярное соотношение реагирующих веществ далеко не всегда равно 1:1, оно определяется стехиометрическими коэффициентами в уравнении реакции. Поэтому для удобства расчетов в химии используют понятие – химический эквивалент вещества, дающее возможность выразить количества реагирующих и образующихся веществ одинаковыми числами.
Химический эквивалент —это некая реальная или условная частица, которая может присоединять, высвобождать или быть каким-либо другим образом эквивалентна одному иону водорода в кислотно-основных реакциях или одному электрону в окислительно-восстановительных реакциях.
Например, в реакции (1):
H2S + NaOH = NaHS + Н2О
эквивалентом сероводорода будет одна молекула H2S (реальная частица), а в реакции (2):
H2S + 2NaOH = Na2S + 2Н2О
эквивалентом того же вещества будет ½ молекулы H2S (условная частица). Для реакции (3):
4Н2O2 + H2S = 4Н2O + H2SO4
эквивалентом сероводорода будет 1/8 молекулы H2S (условная частица), поскольку
S-2 – 8 ē = S+6.
Важным обстоятельством является то, что одно и то же вещество может иметь несколько эквивалентов. Определить эквивалент можно только исходя из конкретной химической реакции.
Число, обозначающее, какая доля реальной частицы вещества X эквивалентна одному иону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции, называется фактором эквивалентности (fэкв.(X)).
Фактор эквивалентности может быть равен или меньше единицы:
fэкв.= 1/z
где z – основность кислоты или кислотность основания в данной кислотно-основной реакции, число отданных или принятых электронов в окислительно-восстановительных реакциях.
В первой реакции fэкв.(H2S) = 1, во второй реакции fэкв.(H2S) = ½, в третьей реакции fэкв.(H2S) = 1/8.
В обменных реакциях без участия протона величина z равна суммарному заряду обменивающихся ионов (без учета знака заряда), z – всегда целое положительное число.
В реакции:
Al2(SО4)3 + 3Ва(ОН) 2 = 2Аl(ОН)3 + 3BaSO4
z = 2 (число ионов) × 3 (заряд иона) = 6
fэкв.(Al2(SO4)3) = 1/6
Поскольку эквивалент является реальной или условной частицей, то единицей его количества является моль.
Молярная масса эквивалента вещества X равна произведению фактора эквивалентности на молярную массу вещества X. Обозначается M(l/z X)
M(l/z X) = l/z × M(X).
Единица молярной массы эквивалента 1 г/моль. Например, молярная масса эквивалента сероводорода в первой реакции равна молярной массе сероводорода и рассчитывается по формуле:
M (l H2S) = l × M(H2S) = 1 × 34 г/моль = 34 г/моль;
во второй реакции:
M(½ H2S) = ½ × M(H2S) = ½ × 34 г/моль = 17 г/моль;
в третьей реакции:
M(l/8 H2S) = l/8 × M(H2S) = l/8 × 34 г/моль = 4,25 г/моль.
Молярная концентрация эквивалента C(l/z X) показывает количество вещества эквивалента (в молях), которое содержится в 1 л раствора. C(l/z X) равна отношению количества вещества эквивалента в растворе к объему этого раствора.
n(l/z Х) m(Х)
С(l/z Х) = —————— = ——————————, моль/л.
V(раствора) М(l/z Х) × V(раствора)
Пример. В водном растворе объемом 0,5 л содержится серная кислота массой 2,45 г. Рассчитать молярную концентрацию эквивалента раствора серной кислоты, fэкв. (H2SO4) = ½.
Решение.
Расчет молярной массы эквивалента серной кислоты:
M(½H2SO4) = ½ × M(H2SO4) = ½ × 98 г/моль = 49 г/моль.
Расчет молярной концентрации эквивалента раствора серной кислоты:
m(H2SO4) 2.45 г
С(½H2SO4) = —————————————— = ——————— = 0.1моль/л.
М(½H2SO4) × V(раствора H2SO4) 49 г/моль × 0.5 л
Для перехода от одного способа выражения концентрации к другому можно воспользоваться соотношением:
C(l/z Х) = z × C(X).
Если фактор эквивалентности равен 1, молярная концентрация эквивалента вещества будет равна молярной концентрации. Во всех других случаях она всегда будет больше молярной концентрации во столько раз, во сколько раз эквивалент меньше реальной частицы.
г)Моляльность b(Х) показывает количество вещества Х (в молях), которое содержится в растворителе массой 1 кг. Моляльность равна отношению количества вещества (в молях) к массе растворителя (в кг).
n(X) m(X)
b(X) = ——————— = ———————————, моль/кг.
m(растворителя) M(X) × m(растворителя)
Пример. Рассчитайте моляльность раствора гидроксида калия, если в воде массой 0,5 кг растворено 0,05 моль КОН.
Решение.
n(КОН) 0.05 моль
b(КОН) = ——————— = ————— = 0.1 моль/кг.
m(растворителя) 0.5 кг
д)Молярная доля показывает, какую часть от общего количества компонентов раствора составляет растворенное вещество X, и равна отношению количества растворенного вещества к общему количеству компонентов раствора.
n(X)
молярная доля = ——————————,
n(X) + n(растворителя)
где n(Х) – количество (в молях) растворенного вещества,
n (растворителя) – количество (в молях) растворителя.
Пример. Рассчитать молярную долю КОН в растворе, если в воде массой 72 г растворено едкого калия массой 11,2 г.
Решение.
1. Расчет количества воды и КОН в данном растворе:
m(H2O) 72 г
а) n(H2O) = ———— = ————— = 4 моль;
М(H2O) 18 г/моль
m(КOН) 11.2 г
б) n(КОН) = ———— = ————— = 0.2 моль;
М(КОН) 56 г/моль
2. Расчет молярной доли:
n(КОН) 0.2 моль
молярная доля = ———————— = ———————— = 0.048.
n(КОН) + n(H2O) 0.2 моль + 4 моль
ж) Титр (Т) — величина, измеряемая массой растворенного вещества X (г), содержащегося в 1 мл раствора. Титр и молярная концентрация связаны простым соотношением:
Т(Х) × 1000
С(Х) = ——————
М(Х)
Количественный анализ
Кривые титрования
В процессе кислотно-основного титрования происходит изменение концентрации ионов водорода и соответственно рН раствора.
Графическое изображение зависимости рН от объёма добавляемого рабочего раствора (или от степени нейтрализации анализируемого раствора) называется кривой титрования.
1. Нейтрализация сильной кислоты сильным основанием
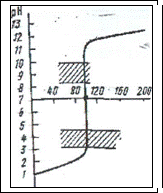
HCl + NaOH = NaCl + H2O
В начале титрования добавление небольшого количества щелочи не оказывает влияние на рН раствора. По мере приближения к точке эквивалентности увеличение рН идет более быстро. Добавление последней капли рабочего раствора приводит к резкому изменению рН титруемого раствора и изменению цвета индикатора.
Резкое изменение рН раствора вблизи точки эквивалентности называется скачком титрования. Середина скачка титрования соответствует точке эквивалентности.
В данном случае рН в точке эквивалентности будет нейтральной, т.к. образующаяся в результате реакции нейтрализации соль не подвергается гидролизу.
Следовательно, при титровании сильных кислот сильными основаниями (и наоборот) можно применять индикаторы, интервал перемены окраски которых от 4 до 10 (метиловый красный, метиловый оранжевый, фенолфталеин и др.). Наиболее подходящим будет тот, у которого рТ=7.
Однако необходимо учесть, что присутствие растворимого оксида углерода (IV) в растворе смещает рН точки эквивалентности в кислую среду, поэтому обычно применяют метиловый оранжевый (рТ=4). Довольно значительное отклонение рТ данного индикатора от рН в точке эквивалентности в данном случае не имеет значения, т.к. для изменения окраски индикатора необходимо прилить к раствору очень малый (менее 1 капли) избыток рабочего раствора.
2. Нейтрализация слабой кислоты сильным основанием (и наоборот)

СН3СООН + NaOH = CH3COONa + Н2O
В точке эквивалентности реакция среды будет щелочной вследствие гидролиза образующейся соли:
СН3СООˉ + Н2O = СН3СООН + ОНˉ
Скачок титрования находится в пределах рН от 7.8 до 10, а точка эквивалентности примерно при рН = 8.9, поэтому следует применять индикаторы, изменяющие окраску при рН > 7, например, фенолфталеин, у которого рТ = 9.
3. Нейтрализация слабого основания сильной кислотой (и наоборот)
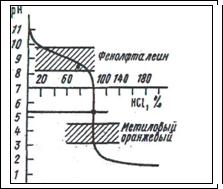
NH4OH + HCl = NH4Cl + Н2O
В точке эквивалентности реакция среды будет кислой, вследствие гидролиза образующейся соли:
NH4+ + Н2O = NH4OH + H+
Скачок титрования находится в пределах рН от 4.0 до 6.2, а точка эквивалентности при рН = 5.1. Поэтому следует применять индикаторы, изменяющие окраску при рН < 7, например, метиловые оранжевый или красный. Таким образом, при выборе индикатора в методе нейтрализации необходимо учитывать следующее:
· индикатор должен изменять свой цвет при значениях рН близких к точке эквивалентности;
· переход цвета индикатора должен быть удобен для зрительного восприятия (порядок титрования). Например, фенолфталеин удобно использовать при титровании кислоты щелочью, т.к. при этом бесцветная окраска индикатора сменяется на малиновую.
Лабораторная работа №1. Приготовление раствора H2SO4 с С(½H2SO4) = 0.1 моль/л
Исходный раствор H2SO4 имеет:
ρ (плотность) = _____г/мл (найдена с помощью ареометра);
ω(массовая доля) = _____% (см. приложение 1);
а) расчет массы навески безводной H2SO4, необходимой для приготовления раствора с С(½H2SО4) = 0,1моль/л объемом 0,2 л; M(H2S04)= 98 г/моль;
m(H2SО4) = С(½H2SО4) × V(H2SО4) × М(½H2SО4) = …(г),
где М(½H2SО4) = ½ × М(H2SО4).
б) расчет массы навески раствора H2SO4 c ω(%) = …
m(H2SО4) × 100
m´(р-раH2SО4) = ——————— = …_(г).
ω
в) расчет объема раствора H2SO4 с ρ = … г/мл.
m´(р-раH2SО4)
V(р-ра H2SО4) = ——————— =_… (мл).
ρ (р-раH2SО4)
Примечание: m и m' рассчитывают с точностью до сотых долей единицы; V(H2SO4) – c точностью до сотых долей, затем округляют до десятых.
Приготовление раствора. Рассчитанный объем раствора H2SO4 отмеряют при помощи мерного цилиндра (или бюретки), осторожно вливают в мерную колбу, затем доливают до метки дистиллированной водой и тщательно перемешивают.
Окончание работы. Раствор из колбы переливают в бутылочку, на этикетке пишут факультет, номер группы, фамилию. Бутылочку с раствором ставят в лабораторный стол, на котором указан номер группы и факультет.
Приложение №1. Плотность и концентрация раствора серной кислоты.
| ρ, г/см | 1,013 | 1,027 | 1,040 | 1,055 | 1,069 | 1,083 | 1,098 | 1,112 |
| ω, % |
Лабораторная работа 2. Установление концентрации рабочего раствора серной кислоты по стандартному раствору тетрабората натрия Nа2В4О7.
Концентрация рабочего раствора С(1/2 Na2B4O7) =
0.l моль/л. Индикатор-метиловый оранжевый (интервал перемены окраски 3.1–4.4).
Уравнение реакции:
Na2B4О7 + 7Н2О = 2NaOH + 4Н3ВО3
Методика титрования.
Стандартный раствор буры объемом 10 мл, отмеренный пипеткой Мора, титруют раствором серной кислоты в присутствии 1 капли индикатора до появления оранжево-розовой окраски.
Для повышения точности титрования можно использовать "свидетель", который готовят, отмерив в колбу 10 мл воды, 1 каплю кислоты и1 каплю индикатора. Пробу титруют до появления такой же окраски как в колбе-свидетеле. Розовая окраска в конце титрования означает, что в колбе избыток кислоты около 1 капли.
Обработка результатов эксперимента.
Титрование проводят с точностью до сотых долей миллилитра. Из совокупности отдельных результатов отбросьте промахи (сходимость результатов 0,1 мл) и найдите среднее значение из трёх сходящихся результатов.
Расчет молярной концентрации эквивалента серной кислоты по закону эквивалентов:
C(1/2H2SO4) = 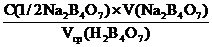 , моль/л
, моль/л
Концентрацию рассчитывают с точностью до трёх значащих цифр. Оформляют работу и сдают преподавателю.
Лабораторная работа 3. Определение концентрации и массы КОН или NaOH в растворе.
Концентрация рабочего раствора серной кислоты устанавливается в предыдущем опыте. Индикатор-метиловый оранжевый.
Уравнение реакции:
H2SO4 + 2Na
