Тема 5. Ионообменные смолы
Пример 1. Расположите катионы солей CaCl2, Na2SO4, KCl, FeCl3, LiNO3 в ряд по увеличению способности поглощаться их Н+–формой катионита из водных растворов. Как изменится этот ряд, если растворители будут слабо полярными ?
Решение. Адсорбционная способность ионов зависит от величины заряда и радиуса. Чем больше заряд иона, тем сильнее он проявляет способность к ионному обмену. Для ионов одинакового заряда максимальную ионообменную способность проявляют те ионы, радиус которых в гидратированном состоянии меньше. Поэтому способность поглощаться катионитами из водных растворов возрастает в ряду ионов:
Li+ < Na+ < K+ < Ca2+ < Fe3+
В слабо полярных растворителях надо учитывать радиус несольватированных ионов, поэтому способность ионов поглощаться катионитами возрастает в следующем ряду:
K+ < Na+ < Li+ < Ca2+ < Fe3+
Пример 2. На титрование 0,50 г воздушно-сухого сильнокислотного катионита с сульфатными группами – SO3H пошло 25,5 мл 0,100 М раствора гидроксида натрия. Вычислите обменную емкость катионита, если массовая доля воды в образце составляет 8%.
Решение. Дано Решение
| m = 0,50 г V(NaOH)= 25,5 мл C(NаOH) = 0,100 М w(H2O) = 8 % | Обменную емкость ионитов (ОЕ) характеризуют количеством эквивалентов (ммоль) активных групп (или противоинов), содержащихся в 1 г сухого ионита и способных обмениваться в растворе на эквивалентное количество ионов того же знака. | |
| ОЕ – ? |
1. Реакция ионного обмена протекает по уравнению:
R–SO3H + NaOH  R – SO3Na + H2O
R – SO3Na + H2O
Из этого уравнения видно, что обмен происходит между Н+ и Na+ в эквивалентных количествах. Следовательно, количество NaOH равно количеству ионов Н+, содержащихся в сухом катионите.
2. Находим массу сухого катионита:
m(сухого катионита) = m(катионита)× w(катионита) = 0,5×0,92 = 0,46 (г)
3. Рассчитаем ОЕ катионита, исходя из ее определения:
ОЕ = 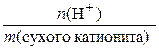 =
= 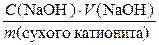 =
= 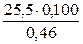 =5,54 (ммоль/г)
=5,54 (ммоль/г)
Пример 3.Через колонку с катионитом в Н+ – форме пропустили 20.00 мл раствора KCl. Элюат оттитровали 15.00 мл 0.1 М раствора NaOH. Определить содержание KCl в анализируемом растворе.
Решение.При пропускании через катионит в Н+ – форме раствора KCl в результате ионообменной реакции 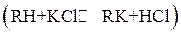 в элюате появляется соляная кислота, количество которой эквивалентно количеству соли, т.е.
в элюате появляется соляная кислота, количество которой эквивалентно количеству соли, т.е. 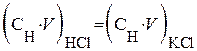 . При титровании кислоты раствором щелочи справедливо равенство:
. При титровании кислоты раствором щелочи справедливо равенство: 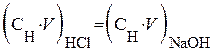 или
или 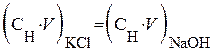 . Тогда, содержание KCl в анализируемом растворе рассчитывают следующим образом:
. Тогда, содержание KCl в анализируемом растворе рассчитывают следующим образом:
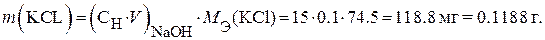
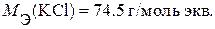
Пример 4.Какая масса Со2+ останется в растворе, если через колонку, заполненную 5 г катионита в Н+ – форме, пропустили 200.0 мл 0.1 н раствора CoCl2. Полная динамическая емкость катионита равна 1.60 мэкв/г.
Решение. 1. Рассчитаем количество миллимоль эквивалентов Со2+ – ионов, пропущенных через колонку с катионитом:
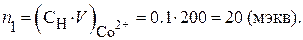
2. Количество миллимоль эквивалентов Со2+ – ионов, поглощенных 5 г катионита вычисляем из формулы:
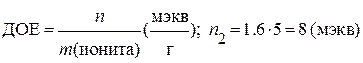
3. Количество миллимоль эквивалентов Со2+ – ионов, оставшихся в растворе, равно: 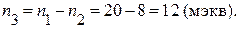
4. Масса Со2+ – ионов, оставшихся в растворе, составляет:
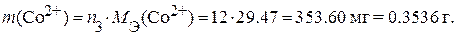
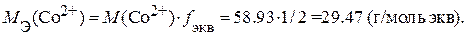
Задачи
В колонку, заполненную сильнокислотным катионитом КУ-2,8 введен раствор, содержащий катионы (см. табл.). В какой последовательности выйдут эти катионы из колонки при вымывании их 0,5 М HCl? Дать пояснения.
| Вариант | Катионы | |||
| Fe3+ | Ca2+ | Li+ | К+ | |
| Ni2+ | Mg2+ | Rb+ | Na+ | |
| Al3+ | Be2+ | In3+ | Mo2+ | |
| Fe3+ | Ca2+ | Li+ | К+ | |
| V2+ | K+ | Pb2+ | Be2+ | |
| Zr2+ | Mn2+ | Na+ | Cr3+ | |
| Eu3+ | Nb3+ | Nd3+ | Mg2+ | |
| Sr2+ | Ti2+ | Bi3+ | Li+ | |
| La3+ | W2+ | Ba2+ | Tb3+ | |
| Co2+ | Cr3+ | Ni2+ | Mn2+ | |
| Y3+ | Sn2+ | Cu2+ | In3+ |
В какой последовательности при вымывании раствором щелочи из колонки, заполненной анионитом, выйдут растворы солей (см. табл.).
| Вариант | Соли | |||
| NaCl | NaBr | NаI | Na2SO4 | |
| К2СrO4 | Na3AsO4 | K2S | KCl | |
| NiSO4 | Na2CO3 | NaNO3 | KBr | |
| Na2C2O4 | KI | K2SO4 | NaNO2 | |
| K3AsO4 | KNO2 | NH4Cr2O7 | NiSO4 | |
| Na2CO3 | KCl | K2S | (NH4)2 C2O4 | |
| K2CrO4 | NaNO2 | ZnSO4 | K3AsO4 | |
| KNO2 | NаI | Na2CO3 | NaNO3 | |
| NaNO3 | K2S | NaBr | NiSO4 | |
| K3AsO4 | NH4Cr2O7 | K3AsO4 | KCl | |
| Na2CO3 | (NH4)2 C2O4 | K2CrO4 | NаI | |
| Na2C2O4 | ZnSO4 | NaNO3 | NH4Cr2O7 | |
| K2S | Na2CO3 | K3AsO4 | KCl | |
| NаI | (NH4)2 C2O4 | K2CrO4 | Na2CO3 |
1.На титрование 0,4 г анионита, содержащего группы –ОН, пошло 20,8 мл 0,01н раствора соляной кислоты. Рассчитать обменную емкость анионита в ммоль/г.
2.Определите обменную ёмкость катионита КУ-2, если 1,125 г его залито 50,0 мл 0,100моль/л CaCl2. На титрование фильтрата израсходовано 6,50 мл 0,0970 моль/л NaOH. Влажность ионита 0,12%.
3.Через колонку с катионитом в Н+ – форме пропустили 20,00 мл раствора KCl. Элюат оттитровали 15,00 мл 0,1 М раствора NaOH. Определить содержание KCl в анализируемом растворе.
4.Какая масса Со2+ останется в растворе, если через колонку, заполненную 5 г катионита в Н+ – форме, пропустили 200,0 мл 0,1 н раствора CoCl2. Полная динамическая емкость катионита равна 1,60 мэкв/г.
5.Навеску 2.0000 г образца, содержащего NaNO3, растворили в 100.0 мл воды. 10.00 мл этого раствора пропустили через колонку с катионитом в
Н+ – форме, а элюат оттитровали 15.00 мл раствора NaOH с концентрацией 4 × 10–3 г/мл. Рассчитать массовую долю NaNO3 в образце.
6.Навеску 2.0000 г образца, содержащего ZnSO4 и различные органические вещества, растворили в 100.0 мл воды. 10.00 мл этого раствора пропустили через колонку с катионитом в Н+ – форме, а элюат оттитровали 15.00 мл раствора NaOH с концентрацией 4.44 мг/мл. Рассчитать массовую долю Zn в образце.
7.Навеску 1.5000 г образца, содержащего MgCl2, растворили в 200.0 мл воды. 20.00 мл этого раствора пропустили через колонку, заполненную катионитом в Н+ – форме, а элюат оттитровали 12.50 мл КOH с концентрацией 5.6 мг/мл. Рассчитать массовую долю Mg в образце.
8.Определить массовую долю азота в азотном удобрении, если навеска 1.1200 г удобрения растворена в мерной колбе емкостью 250.0 мл, и раствор пропущен через колонку с катионитом в Н+ – форме. На титрование 10.00 мл кислоты в элюате израсходовано 12.00 мл раствора NaOH с концентрацией 3.8 г/л.
9.Какой объем 0.07 н раствора MgCl2 нужно пропустить через 100 мл набухшего слоя катионита КУ-2 в Н+ – форме, динамическая обменная емкость которого равна 1200 мэкв/л для полного поглощения Mg2+ – ионов?
10.Определить содержание соли в растворе CaCl2, если 100.0 мл его пропущено через катионит в Н+ – форме и элюат оттитрован 10.00 мл раствора КОН с концентрацией 1.12 мг/мл.
11.Определить массовую долю фосфора в удобрении, если навеска 6.2500 г удобрения растворена в произвольном объеме воды и раствор пропущен через катионит в Н+ – форме. На титрование полученного элюата израсходовано 4.10 мл раствора NaOH с концентрацией, равной 1.74 г/л.
12.Навеску 2.0000 г образца, содержащего Na2SO4 и различные органические примеси, растворили в 100.0 мл воды. 10.00 мл этого раствора пропустили через колонку, заполненную катионитом в Н+ – форме, а элюат оттитровали 15.00 мл NaОН с концентрацией 4 г/л. Рассчитать массовую долю Na2SO4 в образце.
13.1.0000 г образца, содержащего KCl и различные органические вещества, растворили в 50.0 мл воды. 5.00 мл этого раствора пропустили через катионит в Н+ – форме. Элюат оттитровали 15.00 мл раствора КOH с концентрацией, равной 0.56 г/л. Определить массовую долю KCl в образце.
14.Сколько граммов анионита АВ-17 в Cl– – форме потребуется для выделения NO3– – ионов из 500.0 мл раствора NaNO3 с титром 0.008500 г/мл, если статическая обменная емкость анионита составляет 5 мэкв/г?
15.20.00 мл раствора NH4Cl из мерной колбы емкостью 200.0 мл пропустили через колонку с катионитом КУ-2 в Н+ – форме. Элюат оттитровали 10.00 мл раствора NaОН с титром по соляной кислоте, равным 0.003650 г/мл. Определить содержание соли в анализируемом растворе.
16.Какой объем 0.5 М раствора NaNO3 нужно пропустить через 100 мл набухшего слоя катионита КУ-2 в Н+ – форме, динамическая обменная емкость которого равна 1.2 мэкв/мл для полного поглощения Na+ – ионов?
17.Сколько граммов цинка останется в растворе, если через колонку с 3 г катионита пропустили 250.0 мл раствора Zn(NO3)2 с титром, равным 0.009470 г/мл? Полная динамическая обменная емкость катионита составляет 5 мэкв/г.
18.Навеску 2.0000 г образца, содержащего NaNO3, растворили в 100.0 мл воды. 10.00 мл этого раствора пропустили через колонку с катионитом в Н+ – форме, а элюат оттитровали 15.00 мл раствора NaOH с концентрацией 4 × 10–3 г/мл. Рассчитать массовую долю NaNO3 в образце.
19.Навеску 1.5000 г образца, содержащего MgCl2, растворили в 200.0 мл воды. 20.00 мл этого раствора пропустили через колонку, заполненную катионитом в Н+ – форме, а элюат оттитровали 12.50 мл КOH с концентрацией 5.6 мг/мл. Рассчитать массовую долю Mg в образце.
20.Сколько граммов анионита АВ-17 в Cl– – форме потребуется для выделения NO3– – ионов из 250.0 мл раствора NaNO3 с титром 0.008100 г/мл, если статическая обменная емкость анионита составляет 5 мэкв/г?
21.Определить содержание соли в растворе CaCl2, если 50.0 мл его пропущено через катионит в Н+ – форме и элюат оттитрован 10.00 мл раствора КОН с концентрацией 1.00 мг/мл.
22.Навеску 1.0000 г образца, содержащего MnSO4 и различные органические вещества, растворили в 100.0 мл воды. 10.00 мл этого раствора пропустили через колонку с катионитом в Н+ – форме, а элюат оттитровали 15.00 мл раствора NaOH с концентрацией 4.44 мг/мл. Рассчитать массовую долю Mn в образце.
23.Какой объем 0.5 М раствора КNO3 нужно пропустить через 100 мл набухшего слоя катионита КУ-2 в Н+ – форме, динамическая обменная емкость которого равна 1.2 мэкв/мл для полного поглощения К+ – ионов?
24.Определить массовую долю фосфора в удобрении, если навеска 4.000 г удобрения растворена в произвольном объеме воды и раствор пропущен через катионит в Н+ – форме. На титрование полученного элюата израсходовано 2.10 мл раствора NaOH с концентрацией, равной 2.05 г/л.
25.Через колонку с катионитом в Н+ – форме пропустили 10,00 мл раствора KCl. Элюат оттитровали 11,00 мл 0,1 М раствора NaOH. Определить содержание KCl в анализируемом растворе.
