Ионообменные реакции. гидролиз солей
При взаимодействии растворов электролитов реакции происходят между ионами растворенных веществ. Химический процесс можно записать в молекулярной и ионно-молекулярной формах. Однако ионная форма отражает его точнее. При составлении ионных уравнений реакций вещества малодиссоциированные, малорастворимые (выпадающие в осадок) и газообразные изображаются в виде молекул.
Пример 1.Записать в молекулярной и ионно-молекулярной формах уравнения реакций между следующими веществами: H2SO4 и BaCl2; Na2СО3 и НCl.
Решение:
1) H2SO4 + BaCl2= Ва SO4 ↓+ 2 НCl – молекулярное уравнение,
2Н + + SO4 2-_+ Ва2+ + 2Cl- = ВаSO4 ↓ + 2Н+ + 2Cl- – полное ионно-молекулярное уравнение;
Ва2+ + SO4 2- = ВаSO4 ↓ – сокращенное ионно-молекулярное уравнение.
Сокращенное ионно-молекулярное уравнение показывает, что в реакции участвуют только ионы Ва2+ и SO4 2-.
2) Na2СО3 + 2НCl = 2NaCl + Н2О + СО2↑
2 Na + + СО3 2-_+ 2Н++ 2Cl- = 2 Na + + 2Cl- + Н2О + СО2↑
СО3 2-_+ 2Н+ = Н2О + СО2↑
Гидролизомназывается взаимодействие солей и воды с образованием слабодиссоциирующих веществ, одновременно сопровождающееся смещением ионного равновесия воды. Отсюда следует, что не всякое взаимодействие соли с водой является гидролизом, а следовательно, не все соли гидролизу подвергаются.
Гидролизу подвергаются соли, образованные катионом сильного основания и анионом слабой кислоты (Na2CO3, CH3COOK), катионом слабого основания и анионом сильной кислоты ( ZnCl2, Al2(SO4)3), катионом слабого основания и анионом слабой кислоты (CH3COONH4, Al2S3).
Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются.
При анализе состава солей нужно помнить, что:
| 1. К сильным основаниям относятся: LiOH, KOH, NaOH, CsOH, RbOH, Ca(OH)2, Ba(OH)2, Sr(OH)2, Rа(OH)2. 2. К сильным кислотам относятся: H2SO4, H2SеO4, HNO3, HClO4, HBr, HI, HCl. | 3. Слабые основания образуют катионы всех остальных металлов и NH4+. 4. К слабым кислотам относятся: H2SO3, HNO2, HClO, HF, H3PO3, H2CO3, H2S, H2SiO3,CH3COOH и др. |
Соли, образованные многокислотными основаниями или многоосновными кислотами, подвергаются ступенчатому гидролизу. Более легко протекает первая ступень гидролиза, и на ней, как правило, при обычных условиях гидролиз солей завершается. Скорость гидролиза зависит от растворимости солей, оснований и кислот, поэтому необходимо учитывать этот фактор (прил. 7).
Гидролизу подвергается не все количество находящейся в растворе соли, а только часть ее. Иначе говоря, в растворе устанавливается равновесие между солью и образующими ее кислотой и основанием. Доля вещества, подвергающаяся гидролизу, - степень гидролиза, - зависит от константы этого равновесия, а также от температуры и концентрации соли.
Запишем уравнение гидролиза в общем виде. Пусть НА – кислота, МОН – основание, МА – образованная ими соль. Тогда уравнение гидролиза будет иметь вид:
МА + Н2О ↔НА + МОН
Этому равновесию отвечает константа
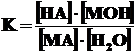 .
.
Концентрация воды в разбавленных растворах представляет собой практически постоянную величину. Обозначая К·[ Н2О] =Кг, получим
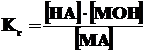 .
.
Величина Кг называется константой гидролиза соли. Ее значение характеризует способность данной соли подвергаться гидролизу; чем больше Кг, тем в большей степени (при одинаковых температуре и концентрации соли) протекает гидролиз. Для соли, образованной катионом сильного основания и анионом слабой кислоты, константа гидролиза связана с константой диссоциации кислоты Ккисл зависимостью:


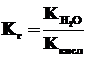 .
.
Это уравнение показывает, что Кг тем больше, чем меньше Ккисл . Иными словами, чем слабее кислота, тем в большей степени подвергаются гидролизу ее соли.
Для солей, образованных катионом слабого основания и анионом сильной кислоты, аналогичное выражение связывает константу гидролиза с константой диссоциации основания Косн:
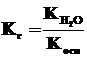 .
.
Поэтому, чем слабее основание, тем в большей степени подвергаются гидролизу образованные им соли.
Степень гидролиза определяется природой соли, ее концентрацией и температурой. Природа соли проявляется в величине константы гидролиза.
Зависимость степени гидролиза (h) от концентрации выражается через закон разбавления:
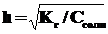 ,
,
то есть с разбавлением раствора степень гидролиза увеличивается.
Влияние температуры на степень гидролиза вытекает из принципа Ле-Шателье. Все реакции нейтрализации протекают с выделением теплоты, а гидролиз с поглощением теплоты. Поскольку выход эндотермических реакций с ростом температуры увеличивается, то и степень гидролиза растет с повышением температуры.
Пример 1.Составить молекулярное и ионное уравнение гидролиза соликарбоната натрия.
Решение. Соль Na2СO3 образована сильным основанием (NaOH) и слабой кислотой (H2СO3), таким образом,гидролиз соли будет протекать по аниону. Так как ион СO32- содержит 2 заряда, то гидролиз возможен в 2 ступени: первая ступень протекает в обычных условиях, вторая – при нагревании или разбавлении. Рассмотрим гидролиз по первой ступени:
Сокращенное ионное уравнение гидролиза:

полное ионное уравнение гидролиза:
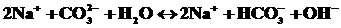
молекулярное уравнение:
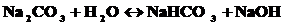
Так как в растворе накапливаются гидроксид-ионы, то среда щелочная, т.е. рН>7.
Пример 2. Составить молекулярное и ионное уравнение гидролиза соли хлорида алюминия.
Решение.Гидролиз солей, образованных слабым основанием (Al(OH)3) и сильной кислотой (HCl) протекает по катиону:
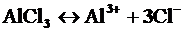
В обычных условиях гидролиз протекает по первой ступени, незначительно – по второй. Третья ступень практически не протекает, однако разбавление или нагревание усиливают гидролиз.
Первая ступень:
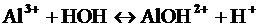
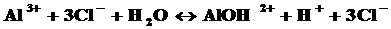
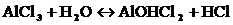
Так как в растворе накапливаются ионы водорода, то среда кислая, т.е. рН<7.
Пример 3. Составить молекулярное и ионное уравнение гидролиза соли, образованной слабым основанием и слабой кислотой.
Решение.Гидролиз солей, образованных слабым основанием и слабой кислотой, протекает полностью и с достаточно большой скоростью, например:
Al2 (CO3)3+3Н2О=2Al(OH)3+3CO2 .
Подобный процесс наблюдается при смешивании растворов Na2CO3 и AlCl3, в которых соответственно имеются избыток ионов ОН- и Н+:
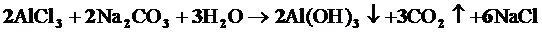
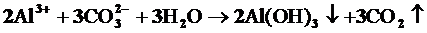
Задачи к главе 9
Й уровень
336-340. Записать в молекулярной и ионно-молекулярной формах уравнения реакций между веществами А и Б, приводящих к образованию малорастворимых осадков или газов:
| Задачи | |||||
| А | NiСl2 | К2СО3 | СuSO4 | Рb(NО3)2 | АgNО3 |
| Б | Н2S | Н2SО4 | Na3РО4 | KI | AlBr3 |
341-345. Составьте уравнения гидролиза солей А и Б в молекулярной и ионно-молекулярной формах. Укажите, каким будет рН их растворов (рН>7, рН<7, рН=7):
| Задачи | |||||
| А | NiSО4 | СоСl2 | Аl2(SO4)3 | Zn(NО3)2 | АgNО3 |
| Б | К2СО3 | НСООNа | Na3РО4 | Li3ВО3 | KIO |
346-350. Составьте уравнения гидролиза солей А и Б в молекулярной и ионно-молекулярной формах. Запишите уравнение совместного гидролиза этих солей в молекулярной форме, если одним из продуктов совместного гидролиза является гидроксид металла соли А:
| Задачи Задачи | |||||
| A | SnSO4 | CrCl3 | Zn(NO3)2 | АlСl3 | Gа2(SО4)3 |
| Б | K2S | K2CO3 | СН3СООNа НСООNа Li2CO3 | Nа2Sе | Nа2СО3 |
351-355. Составьте уравнения гидролиза солей А и Б в молекулярной и ионно-молекулярной формах. Укажите, каким будет рН их растворов (рН>7, рН<7, рН=7):
| Задачи | |||||
| А | FеСl2 | Nа2S | Sn(NО3)2 | Nа2SеО3 | КСlО |
| Б | FеСl3 | Nа2SO3 | Sn(NО3)4 | Nа2SеО4 | КIО |
Й уровень
356-360. Составьте уравнения гидролиза солей А и Б в молекулярной и ионно-молекулярной формах и укажите, как изменится (уменьшится или увеличится) степень гидролиза этой соли при: а) при уменьшении ее концентрации; б) уменьшении рН; в) увеличении температуры, учитывая, что реакция гидролиза является эндотермической?
| Задачи | |||||
| A | V2(SО4)3 | Na3ВО3 | Тi(SО4)2 | КВrО | SnCl4 |
| Б | NiSО4 | СоСl2 | Аl2(SO4)3 | Zn(NО3)2 | АgNО3 |
361-365. Укажите направление смещения равновесия гидролиза соли А при добавлении к раствору веществ Б, В и Г:
| Задачи | |||||
| А | МnСl2 | КАsО2 | СоSО4 | SbСl3 | NаРО2 |
| Б | НСl | НNO3 | Н2SО4 | НСl | НNО3 |
| В | КОН | NаОН | КОН | RbОН | КОН |
| Г | NаСl | LiNO3 | Nа2SО4 | КСl | NаNО3 |
366-370. Какое из веществ Б, В или Г следует добавить к раствору соли А, чтобы степень гидролиза увеличилась?
| Задачи | |||||
| А | Nа2SeО3 | Li2S | Pb(NO3)2 | СоSО4 | SbСl3 |
| Б | НСl | НNО3 | Н2SО4 | НNО3 | НСl |
| В | КОН | NаОН | КОН | NаОН | NаОН |
| Г | NаNО3 | K2SО4 | K2SО4 | КNО3 | KF |
Й уровень
371-375. Записать в молекулярной и ионно-молекулярной формах уравнения реакций между водными растворами следующих веществ:
| Задачи | |||||
| А | Са(ОН)2 | Са(ОН)2 | Аl(NО3)3 | Zn (NО3)2 | SnCl2 |
| Б | СО2(изб.) | СО2 | КОН(изб.) | КОН(изб.) | КОН(изб.) |
Для каждого случая указать причину смещения равновесия в сторону прямой реакции.
376-380.Значение рН 0,1 М раствора соли А составляет В. Рассчитайте константу Кг и степень гидролиза h. Составьте уравнение гидролиза в ионно-молекулярной форме. По вычисленным значениям Кг и h мотивированно укажите, к продуктам или к исходным веществам смещено равновесие гидролиза:
| Задачи | |||||
| А | Аl(NО3)3 | CdSO4 | Nа2SО3 | КВrО | GаСl3 |
| B |
381-385.Вычислите рН водного раствора А с концентрацией с, моль/л, если степень диссоциации α = 0,8:
| Задачи | |||||
| А | Ва(ОН)2 | NaОН | НNO3 | НВr | НСlО4 |
| с, моль/л | 0,1 | 0,01 | 0,001 | 0,05 | 0,1 |
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
Молекулярные соединения, образующие комплексные ионы, способные к существованию как в растворе, так и в кристалле, называются комплексными. Строение комплексных соединений объясняет координационная теория. В комплексных соединениях различают внешнюю и внутреннюю (комплексный ион) сферы. Во внутренней сфере комплексных соединений:
1) центральное место занимает комплексообразователь – обычно положительно заряженный ион;
2) вокруг комплексообразователя расположены или координированы лиганды (адденды), т.е. ионы противоположного знака или нейтральные молекулы;
3) находится координационное число, показывающее, сколько лигандов удерживает комплексообразователь.
Во внешнюю сферу входят катионы или анионы. Комплексные соединения – неэлектролиты не имеют внешней сферы, например, [Pt(NH3)2Cl4]. Типичными комплексообразователями являются d-элементы: Ag+, Au+, Cu+, Cu2+, Hg2+, Cd2+, Zn2+, Fe2+ , Fe3+, Co2+, Ni2+, Pt4+ и другие, а также s,p – элементы ( Ве, Al, Sn, Pb). Важнейшими лигандами являются:
1) нейтральные молекулы, имеющие дипольный момент: Н2О, NН3, СО, NО и другие;
2) ионы СN-, NО2-, Сl-, Br-, J-, S2O32-, ОН-, СО32- и другие.
Значения координационного числа (КЧ) для некоторых ионов комплексообразователей приведены в таблице:
| КЧ=2 | КЧ=4 | КЧ=6 | КЧ=8 |
| Ag+, Au+, Cu+ | Cu2+, Hg2+, Cd2+, Ве2+ , Al3+, Pt2+ | Zn2+, Fe2+, Fe3+, Co2+, Ni2+, Pt4+, Сr3+ | Cа2+, Ва2+, Sr2+, Ti4+ |
Как видно, чаще всего координационное число имеет значения 4 и 6. Заряд комплексного иона равен алгебраической сумме зарядов комплексообразователя и лигандов. При этом заряд комплексообразователя принимается равным его степени окисления. Вследствие того, что любое комплексное соединение в целом электронейтрально, алгебраическая сумма зарядов внешней и внутренней сфер комплексного соединения равна нулю.
Пример 1. Вычислить заряды следующих комплексных ионов, образованных хромом (III): а) [CrCl(H2O)5]; б) [CrCl2(H2O)4]; в) [Cr(C2О4)2(H2O)2].
Решение.Заряд иона хрома (III) принимаем равным +3, заряд молекулы воды равен нулю, заряды хлорид- и оксалат-ионов соответственно равны -1 и -2. Составляем алгебраические суммы зарядов для каждого из указанных соединений: а) +3 + (-1) =+2; б) +3 +2(-1) = +1; в) +3 +2(-2) = -1.
Названия комплексных солей образуют по общему правилу: сначала называют анион, а затем – катион в родительном падеже. Название комплексного катиона составляют следующим образом: сначала указывают числа (используя греческие числительные: ди, три, тетра, пента, гекса и т.д.) и названия нейтральных лигандов, причем вода называется аква, а аммиак – аммин. Затем указывают числа и названия отрицательно заряженных лигандов с окончанием «о» ( Cl- - хлоро, SO42- - сульфато, ОН- - гидроксо и т.д.); последним называют комплексообразователь, указывая его степень окисления (в скобках римскими цифрами после названия комплексообразователя).
Пример 2. Назвать комплексные соли: [PtCl(NH3)3]Cl, [СоBr(NH3)5]SO4, Ва[Сr(SСN)4(NH3)2].
Решение. [PtCl(NH3)3]Cl – хлорид триамминхлороплатины (II); [СоBr(NH3)5]SO4 – сульфат пентамминбромокобальта (III); Ва[Сr(SСN)4(NH3)2] –диамминтетрароданохромат (III) бария.
В водных растворах комплексные соли диссоциируют в две стадии. Внешнесферная диссоциация комплексных солей происходит практически полностью с образованием комплекных ионов и ионов внешней сферы. Эта диссоциация называется первичной. Комплексные ионы, в свою очередь, под воздействием дополнительных внешних факторов, подвергаются вторичной диссоциации на центральный ион и лиганды. Вторичная диссоциация протекает незначительно и характеризуется константой равновесия, называемой константой нестойкости комплексного иона. Чем устойчивее комплексный ион, тем меньше его константа нестойкости.
Пример 3. Написать уравнения первичной и вторичной диссоциации комплексной соли [Ag(NH3)2]Cl. Составить выражение для константы нестойкости комплексного иона.
Решение. Первичная диссоциация протекает согласно уравнению:
[Ag(NH3)2]Cl→ [Ag(NH3)2]+ + Cl-
Комплексный ион, в свою очередь, подвергается вторичной диссоциации на центральный ион и лиганды: [Ag(NH3)2]+↔ Ag+ +2 NH3. Составим выражение для константы нестойкости комплексного иона:
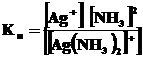 .
.
ЗАДАЧИ К ГЛАВЕ 10
Й уровень
386-390. Составить выражение для константы нестойкости комплексного иона А и определить в нем степень окисления иона – комплексообразователя:
| Задачи | |||||
| А | [Fe(CN)6]4- | [Hg(CN)4]2- | [AuCl4] - | [PtCl6] 2- | [Fe(CN)6]3- |
Й уровень
391-395. Составить координационную формулу комплексной соли с названием А и написать для нее уравнения первичной и вторичной диссоциации:
| Задачи | |||||
| А | Дицианоарген-тат калия | Гексанитро-кобальтат (III) калия | Бромид гексамминко- бальта(III) | Сульфат тетрамминкар-бонатохрома (III) | Гексацианоферрат (III) калия |
Й уровень
396-400. Составить уравнения первичной и вторичной диссоциации комплексного соединения А. Написать в молекулярной и ионно-молекулярной формах уравнения обменных реакций, происходящих между веществами А и В, имея в виду, что образующиеся комплексные соли нерастворимы в воде. Дать названия продуктам реакции:
| Задачи | |||||
| А | К4[Fe(CN)6] | Nа3[Со(CN)6] | К3[Fe(CN)6] | Nа3[Со(CN)6] | К4[Fe(CN)6] |
| B | CuSO4 | Fe SO4 | AgNO3 | NiSO4 | Zn SO4 |
