В) Разложением некоторых солей кислород содержащих кислот (карбонатов, нитратов, сульфатов)
НОМЕНКЛАТУРА ОКСИДОВ

Давая название оксида вначале называют элемент образующий оксид, после чего указывают валентность (если она у данного элемента переменная), затем добавляют слово «оксид»
СаО – кальция оксид Валентность у данных элементов постоянная
Na2O - натрия оксид
Р2О3 - фосфора (III) оксид
Р2О5 - фосфора (V) оксид Валентность элементов переменная
Cu2О - меди (I) оксид
CuО - меди (II) оксид
Физические свойства оксидов
Важнейшими физическими свойствами оксидов являются их агрегатное состояние и растворимость в воде.
По агрегатному состоянию оксиды могут быть твердые, жидкие, газообразные:
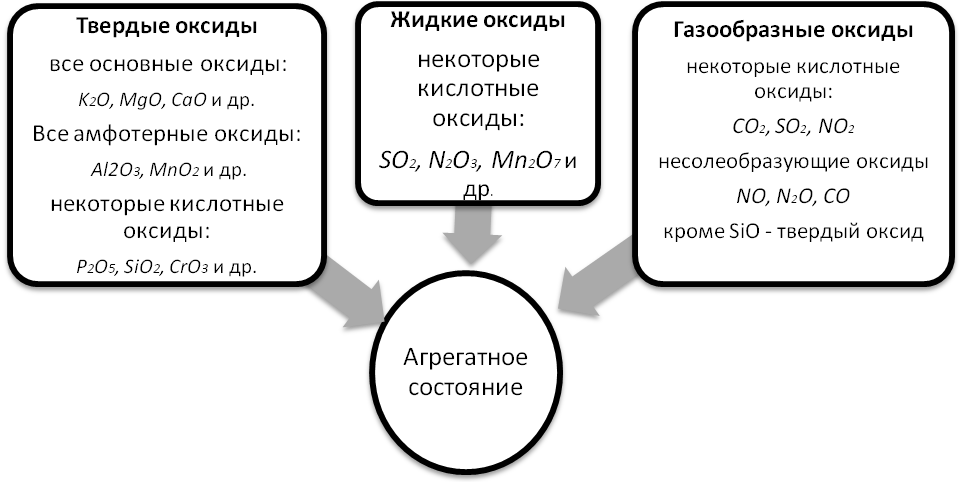
По растворимости в воде оксиды делятся на растворимые и нерастворимые.
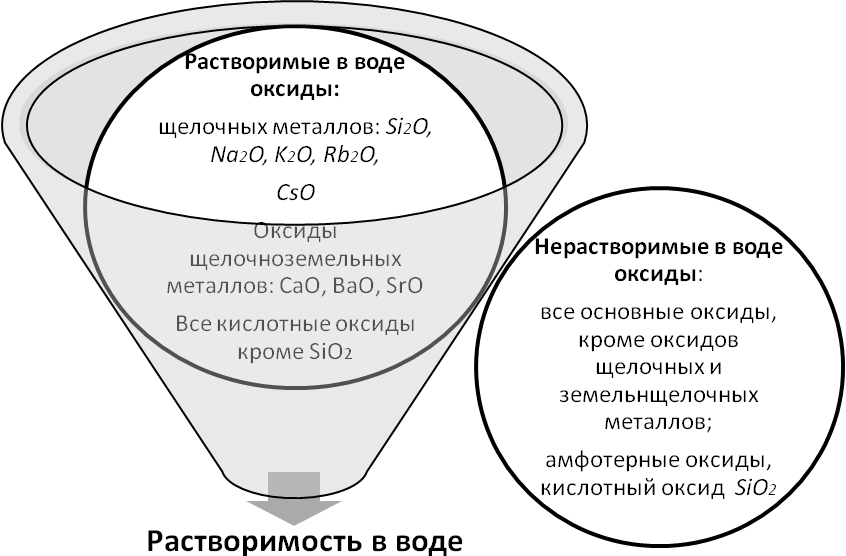
ХИМИЧЕСКИЕ СВОЙСТВА
1. Основные оксиды взаимодействуют с кислотами с образованием солей и воды:
Основной оксид + Кислота — Соль + Вода
ВаО + 2НС1 = ВаС12 + Н20
2. Основные оксиды взаимодействуют с кислотными оксидами с образованием солей:
Основной оксид + Кислотный оксид = Соль
СаО + СО2 = СаСОз
3. Растворимые в воде основные оксиды взаимодействуют с водой с образованием растворимых оснований (щелочей). Взаимодействие сопровождается выделением большого количества тепла:
Оксид щелочного или щелочноземельного металла + Вода = Щелочь
Na2О + Н2О = 2NaOH
4. Кислотные оксиды взаимодействуют с основаниями, в результате чего образуется соль и вода:
Кислотный оксид + Основание = Соль + Вода
Р2О5 + 6КОН = 2К3РО4 + ЗН2O
5. Все кислотные оксиды, кроме кремния IV оксида, взаимодействуют с водой с образованием кислородсодержащих кислот:
Кислотный оксид + Вода = Кислота
N2О5 + H2О = 2HNO3
6. Амфотерные оксиды взаимодействуют с кислотами, с образованием соли и воды:
Амфотерный оксид + Кислота = Соль + Вода
ZnO + 2НС1 = ZnCl2 + Н2O
7. Проявляя кислотные свойства, амфотерные оксиды взаимодействуют со щелочами с образованием соли и воды:
Амфотерный оксид + Щелочь = Соль + Вода
t
ZnO + 2NaOH —›Na2ZnO2 + H2O
Амфотерные оксиды при нагревании взаимодействуют с кислотными оксидами, с образованием соли
Амфотерный оксид + Кислотный оксид = Соль
t
А12Оз + 3SOs → A12(SO4)3
9. Амфотерные оксиды взаимодействуют с основными оксидами при нагревании, с образованием соли:
Амфотерный оксид + Основной оксид = Соль
t
А12О3 + Na2О —› 2NaA1O2
ПОЛУЧЕНИЕ ОКСИДОВ
I. Основные оксиды
Путем окисления металла:
t
Металл + О2 = Основной оксид 4
Na + О2 = 2Na2О
Б) Термическое разложение нерастворимых оснований:
t
Нерастворимое основание = Основной оксид + Вода
t
2Fe(ОH)3 = Fe2О3 + 3H2О
В) Разложением некоторых солей кислород содержащих кислот (карбонатов, нитратов, сульфатов)
t
СаСO3—›Са0 + СO2#
t
Fe2(SO4)3 —›Fe2О3 + 3 SO3#
t
2Cu(NO3)2 —›2 CuO + 4NО2 +O2 #
ΙΙ. Кислотные оксиды:
А) Путем окисления неметалла:
Неметаллы и некоторые + = Кислотный оксид металлы (Сr, Мп)
S+ O2 = SO2
