Групповой реагент, общие и фармакопейные реакции катионов II аналитической группы
Групповым реагентом на катионы второй аналитической группы является водный раствор соляной кислоты.
Реакция катиона свинца Рb2+
Хлороводородная кислота и растворимые хлориды HCl и NaCl осаждают из растворов солей свинца (П) со слабокислой реакцией белый хлопьевидный осадок хлорида свинца (П), легко растворимый в горячей воде:
Pb(NO3)2 + 2HCl = PbCl2 ↓ + 2HNO3
Pb2+ + 2Cl- = PbCl2↓
Гидроксиды щелочных металлов KOH и NaOH из растворов солей свинца (П) осаждают гидроксид свинца (П) – осадок белого цвета.
Pb(NO3)2 + 2КОН = PbCl2 ↓ + 2КNO3
Pb2+ + 2ОН- = Pb(ОН)2↓
Гидроксид свинца (П) обладает амфотерными свойствами, поэтому он растворяется в разбавленной азотной или уксусной кислотах или в избытке щелочи:
Pb(OН)2 + 2КОН = К2[Pb(OН)4]
Серная кислота H2SO4 и растворимые сульфаты выделяют из растворов свинцовых солей осадок белого цвета:
Pb(NO3)2 + H2SO4 = PbSO4 ↓ + 2HNO3
Pb2+ + H2SO4 = PbSO4 ↓
Иодид калия КJ, взаимодействуя с растворами свинцовых солей, дает желтый осадок иодида свинца (П):
Pb(NO3)2 + KJ = PbJ2 ↓ + 2KNO3
Pb2+ + 2J = PbJ2 ↓
Хромат калия K2CrO4 или хромат натрия Na2CrO4 выделяет из слабокислых растворов солей свинца (П) желтый осадок хромата свинца (П):
Pb(NO3)2 + K2CrO4 = PbCrO4 ↓ + 2KNO3
Pb2+ + CrO42- = PbCrO4
Осадок не растворяется в уксусной кислоте, но растворяется в азотной кислоте и гидроксидах щелочных металлов. Реакция чувствительна и является характерной для ионов Pb2+.
Реакции катиона серебра Ag+
1. Хлороводородная кислота HCl и растворимые хлориды осаждают из нейтральных и кислых растворов солей серебра в виде белого творожистого осадка хлорид серебра:
AgNO3 + HCl = AgCl↓ + HNO3
Ag+ + Cl- = AgCl↓
Осадок легко растворяется в избытке аммиака с образованием комплексной соли:
AgCl + 2NH3H2O = [Ag(NH3)2Cl + 2H2O
Иодид калия KJ образует с ионом Ag+ светло-желтый осадок:
AgNO3 + KJ = AgJ↓ + KNO3
Ag+ +J- = AgJ↓
Иодид серебра не растворяется в растворе аммиака в отличие от хлорида серебра.
Хромат калия K2CrO4 выделяет из слабокислых растворов солей серебра (II) желтый осадок хромата серебра:
2AgNO3 + K2CrO4 = Ag2CrO4 ↓ + 2KNO3
2Ag+ + CrO42- = AgCrO4 ↓
Осадок растворяется в растворе аммиака, гидроксидах щелочных металлов и азотной кислоте. Не растворяется в уксусной кислоте.
4.Образуйте заданную комплексную частицу в соединение и укажите для него:
- внешнюю координационную сферу;
- внутреннюю координационную сферу;
- комплексообразователь;
- лиганды;
- координационное число;
- назвать полученные соединения.
[Co(NH3)6]*, где Co3+
-Внутренняя координационная сфера- [Co(NH3)6]
-Комплексообразователь- Co3+
-Лиганды- NH30
-КЧ-6
5.Составьте уравнения гидролиза солей:
NaNO3, Ca(CN)2, MgS, CuI2, Cr2(SO4)3, CrCl3
Укажите рН раствора.
NaNO3 + HOH= гидролиз не идет
Ca(CN)2+ HOH= HCN+ CaOHCN
CN-+ HOH= HCN+ OH-
CaOHCN+ HOH= Ca(OH)2+ HCN
CN-+ HOH= HCN+ OH-
Среда щелочная, фиолетовый лакмус станет синим.
Al2(SO4)3+ 2HOH= 2AlOHSO4+ H2SO4
Al3+HOH= AlOH2++ H+
2AlOHSO4+ 2HOH=(Al(OH)2)2SO4+ H2SO4
AlOH2++HOH= Al(OH)2++ H+
(Al(OH)2)2SO4+2HOH= 2Al(OH)3+ H2SO4
Al(OH)2++HOH= Al(OH)3+ H+
Среда кислая, фиолетовый лакмус станет красным
CuI2+ HOH= CuOHI+ HI
Cu2++ HOH= CuOH++ H+
CuOHI+ HOH= Cu(OH)2+ HI
CuOH++ HOH= Cu(OH)2+ H+
Среда кислая, фиолетовый лакмус станет красным.
Cr2(SO4)3+2 HOH= 2CrOHSO4+ H2SO4
Cr3++ HOH= CrOH2++H+
2CrOHSO4+ 2HOH= (Cr(OH)2) SO4+ H2SO4
CrOH2++HOH= Cr(OH)2++ H+
(Cr(OH)2) SO4+2 HOH= 2Cr(OH)3+ H2SO4
Cr(OH)2++HOH= Cr(OH)3+ H+
Среда кислая, фиолетовый лакмус станет красным.
CrCl3+HOH= CrOHCl2+ HCl
Cr3++ HOH= CrOH2++ H+
CrOHCl2+ HOH= Cr(OH)2Cl+ HCl
CrOH2++HOH= Cr(OH)2++ H+
Cr(OH)2Cl+HOH= Cr(OH)3+ HCl
Cr(OH)++HOH= Cr(OH)3+H+
Среда кислая, фиолетовый лакмус станет красным.
| департамент здравоохранения Брянской области Государственное автономное образовательное учреждение среднего профессионального образования «Брянский базовый медицинский колледж» | 060301 «Фармация» (код и наименование специальности) базовый (профиль подготовки) «Фармация» (наименование ВМК) |
Учебная дисциплинаАналитическая химия
Коды проверяемых компетенций:
ОК: 2, 3
ПК: 1.1; 1.6; 2.1; 2.2; 2.3
БИЛЕТ №12
1.При 20 °С реакция протекает за 2 мин. За сколько времени будет протекать эта же реакция при 50°С,если температурный коэффициент равен 2?
Решение: в соответствии с правилом Вант-Гоффа при повышении температуры от 20°С до 50°С скорость реакции увеличивается:
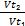 =
= 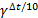 , ,
, , 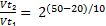 = 23=8
= 23=8
Увеличивается в 8 раза
2) скорость реакции обратно пропорциональна времени реакции. Следовательно:
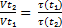 , или τ(t₂)= τ(t₁)*
, или τ(t₂)= τ(t₁)* 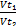
Где τ(t₁) и τ(t₂) – время реакции при температурах t1 и t2. Учитывая, что τ(t₁)= 120 сек.(2 мин), определяем время реакции при температуре t2: τ(t₁)= 120 сек* 1/8 = 15 сек.
Ответ: 15 сек.
2.Напишите характерные реакции на ион SO42-.
Хлорид бария BaCl2 осаждает из разбавленных растворов сульфатов белый осадок сульфата бария
BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl
Ba2+ + SO42- = BaSO4↓
Сульфат бария нерастворим в кислотах. Этим он отличается от других бариевых солей анионов первой группы. Реакция является фармакопейной.
