Написать уравнения электродных процессов и суммарной реакции процесса коррозии
РЕШЕНИЕ:
По таблице 11.1 находим значение стандартных электродных потенциалов железа и цинка:
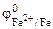 = - 0,44В,
= - 0,44В, 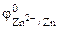 = - 0,76В.
= - 0,76В.
Так как 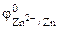 <
< 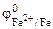 , то анодом коррозионного гальванического элемента будет являться цинк, катодом – железо.
, то анодом коррозионного гальванического элемента будет являться цинк, катодом – железо.
а) Коррозия в атмосферных условиях (H2O+O2).
Составляем схему коррозионного ГЭ:
 |  |
А (-) Zn H2O + O2 Fe (+) K
Составляем уравнения электродных процессов и суммарной реакции процесса коррозии:

 НОК ДМ
НОК ДМ
На A(-) Zn – 2ē = Zn2+ 2
На К(+) 2H2O + O2 + 4ē = 4OH- 1
 |
2Zn + 2H2O + O2 = 2Zn(OH)2 – суммарное молекулярное уравнение процесса коррозии.
б) Коррозия в кислой среде (H2SO4)
Составляем схему коррозионного ГЭ:
А (-) Zn │ H2SO4 │ Fe (+) K
или
А (-) Zn │ H+ │ Fe (+) K
Составляем уравнения электродных процессов и суммарной реакции процесса коррозии:
НОК ДМ

 На A(-) Zn – 2ē = Zn2+ 1
На A(-) Zn – 2ē = Zn2+ 1
На К(+) 2H+ + 2ē = H2 1
 |
Zn + 2H+ = Zn2+ + H2 - суммарное ионно-молекулярное уравнение процесса коррозии;
Zn + H2SO4 = ZnSO4 + H2 – суммарное молекулярное уравнение процесса коррозии.
в) Коррозия в кислой среде в присутствии кислорода (HCl+O2).
Составляем схему коррозионного ГЭ:
А (-) Zn │ HCl + O2 │ Fe (+) K
или
А (-) Zn │ H+ + O2 │ Fe (+) K
Составляем уравнения электродных процессов и суммарной реакции процесса коррозии:

 НОК ДМ
НОК ДМ
На A (-) Zn – 2ē = Zn2+ 2
 На К (+) 4H+ + O2 + 4ē = 2H2O 1
На К (+) 4H+ + O2 + 4ē = 2H2O 1
2Zn + 4H+ + O2 = 2Zn2+ + 2H2O – суммарное ионно-молекулярное уравнение процесса коррозии
2Zn + 4HCl + O2 = 2ZnCl2 + 2H2O – суммарное молекулярное уравнение процесса коррозии.
Во всех случаях коррозионному разрушению будет подвергаться более активный металл – цинк.
УРОВЕНЬ В
1. Составить схему гальванического элемента (ГЭ), образованного цинковым электродом, погруженным в 1М раствор хлорида цинка, и хромовым электродом, погруженным в 1·10-3М раствор хлорида хрома (III). Рассчитать напряжение ГЭ, написать уравнения электродных процессов и суммарной токообразующей реакции.

| РЕШЕНИЕ: Для составления схемы ГЭ необхо-димо знать величины электродных потенциалов металлов – цинка и хрома. По таблице 11.1 определяем стан-дартные электродные потенциалы металлов: |
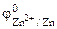 = - 0,76 В,
= - 0,76 В, 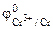 = - 0,74В.
= - 0,74В.
Хлорид цинка диссоциирует по уравнению:
ZnCl2 = Zn2+ + 2Сl-.
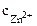 =
= 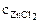 ∙α∙
∙α∙ 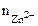 = 1∙1∙1 = 1 моль/л,
= 1∙1∙1 = 1 моль/л,
α = 1 (ZnCl2 – сильный электролит), 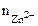 = 1, поскольку условия стандартные
= 1, поскольку условия стандартные 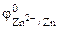 = -0,76В.
= -0,76В.
Хлорид хрома (III) диссоциирует по уравнению:
CrCl3 = Cr3+ + 3Сl-
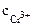 =
= 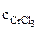 ∙α∙
∙α∙ 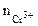 = 10-3∙1∙1 = 10-3 моль/л,
= 10-3∙1∙1 = 10-3 моль/л,
α = 1 (CrCl3 – сильный электролит), 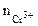 = 1, поскольку условия отличны от стандартных, рассчитываем электродный потенциал хрома:
= 1, поскольку условия отличны от стандартных, рассчитываем электродный потенциал хрома:
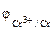 =
= 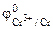 +
+ 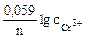 = -0,74 +
= -0,74 + 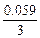 lg10-3= -0,80В
lg10-3= -0,80В
Так как 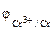 <
< 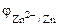 , то в ГЭ анодом будет являться хром, катодом – цинк.
, то в ГЭ анодом будет являться хром, катодом – цинк.
Составляем схему ГЭ:
А (-) Cr │ CrCl3 ││ ZnCl2 │ Zn (+) K
А (-) Cr │ Cr3+ ││ Zn2+ │ Zn (+) K
Составляем уравнения электродных процессов и суммарной токообразующей реакции:

 НОК ДМ
НОК ДМ
На A(-)Cr – 3ē = Cr3+ 2
На К(+)Zn2+ + 2ē = Zn 3

2Cr + 3Zn2+ = 2Cr3+ + 3Zn - суммарное ионно-молекулярное уравнение токообразующей реакции
2Cr + 3ZnCl2 = 2CrCl3 + 3Zn - суммарное молекулярное уравнение токообразующей реакции.
Рассчитываем напряжение ГЭ:
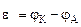 =
= 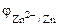 -
- 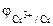 = -0,76-(-0,80)= 0,04В
= -0,76-(-0,80)= 0,04В
Ответ: ε = 0,04В.
2. Составить схему ГЭ, в котором протекает химическая реакция Fe + Ni2+ = Fe2+ + Ni. Написать уравнения электродных процессов. На основании стандартных значений энергий Гиббса образования ионов ∆fG0(298К, Men+) рассчитать стандартное напряжение ГЭ и константу равновесия реакции при 298К.
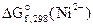 = - 64,4 кДж/моль;
= - 64,4 кДж/моль;
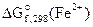 =- 84,94 кДж/моль.
=- 84,94 кДж/моль.
Дано: 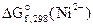 = -64,4 кДж/моль = -64,4 кДж/моль 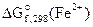 = -84,94 кДж/моль Т = 298 К = -84,94 кДж/моль Т = 298 К  ε0 - ? Кс - ? ε0 - ? Кс - ? | РЕШЕНИЕ: На основании реакции, приведенной в условии задачи, составляем уравнения электродных процессов: |
НОК ДМ

 На A(-)Fe – 2ē = Fe2+ 1 - окисление
На A(-)Fe – 2ē = Fe2+ 1 - окисление
На К(+)Ni2+ + 2ē = Ni 1 - восстановление
Анодом ГЭ является электрод, на котором происходит процесс окисления. Катодом – электрод, на котором происходит процесс восстановления. Тогда в рассматриваемом ГЭ анодом будет являться железо, катодом – никель.
Составляем схему ГЭ:
А(-) Fe │ Fe2+ ║ Ni2+ │ Ni(+)K
Рассчитываем стандартное напряжение ГЭ:
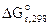 = - z∙F∙ε0,
= - z∙F∙ε0,
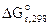 =
= 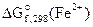 -
- 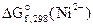 =
=
= -84,94-(-64,4) = -20,54 кДж,
ε0 = 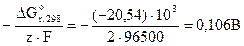
z = 2, F = 96500 Кл/моль.
Рассчитываем константу равновесия токообразующей реакции (Кc).
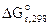 = - 2,303∙R∙T∙lgKc;
= - 2,303∙R∙T∙lgKc;
lgKс = 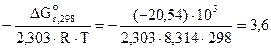
Kс = 103,6 = 3981
Ответ: ε0 = 0,106В, Kс = 3981.
3. Составить схему коррозионного ГЭ, возникающего при контакте железной пластинки площадью 20 см2 с никелевой в растворе соляной кислоты HCl. Написать уравнения электродных процессов и суммарной реакции процесса коррозии.
а) Вычислить объемный и весовой показатели коррозии, если за 40 минут в процессе коррозии выделилось 0,5 см3 газа (н.у.).
б) Вычислить весовой и глубинный показатели коррозии, если за 120 минут потеря массы железной пластинки составила 3,7∙10-3 г. Плотность железа равна 7,9 г/см3.
РЕШЕНИЕ:
По таблице 11.1 находим значения стандартных электродных потенциалов железа и никеля:
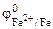 = - 0,44В,
= - 0,44В, 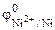 = - 0,26В.
= - 0,26В.
Так как 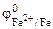 <
< 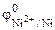 , то анодом коррозионного ГЭ будет являться железо, катодом – никель.
, то анодом коррозионного ГЭ будет являться железо, катодом – никель.
Составим схему коррозионного ГЭ:
А (-) Fe │ HCl │ Ni (+) K
или
А (-) Fe │ H+ │ Ni (+) K
Cоставляем уравнения электродных процессов и суммарной реакции процесса коррозии:
На A Fe – 2ē = Fe2+
 На К 2Н+ + 2ē = Н2
На К 2Н+ + 2ē = Н2
Fe + 2H+ = Fe2+ + H2 – суммарное ионно-молекулярное уравнение процесса коррозии.
Fe + 2HCl = FeCl2 + H2 – суммарное молекулярное уравнение процесса коррозии.
а)

| Рассчитываем объемный показатель коррозии KV по формуле: KV =  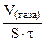 , см3/м2∙час. При расчете KV принимаем: S – [м2], τ - [час], V(газа) – [см3]. , см3/м2∙час. При расчете KV принимаем: S – [м2], τ - [час], V(газа) – [см3]. |
Из уравнения суммарной реакции процесса коррозии следует, что при коррозии выделяется водород.
Следовательно, V(газа) = 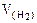 .
.
Тогда, KV = 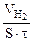 =
= 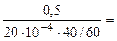 375 см3/м2∙час.
375 см3/м2∙час.
10-4 – коэффициент пересчета, см2 в м2.
Рассчитываем весовой показатель коррозии Km по формуле:
Km = 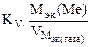 , г/м2∙час.
, г/м2∙час.
В процессе коррозии разрушению подвергается железо и выделяется водород.
Следовательно:
Мэк(Ме) = Мэк(Fe) = 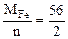 =28 г/моль,
=28 г/моль,
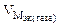
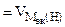 = 11200 см3/моль.
= 11200 см3/моль.
Km = 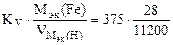 = 0,94 г/м2∙час.
= 0,94 г/м2∙час.
Ответ: KV = 375 см3/м2∙час, Km = 0,94 г/м2∙час.
б)

| Рассчитываем весовой показатель коррозии Km по формуле: Km =  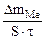 , г/м2∙час. Коррозии подвергается железо. Тогда потеря массы металла , г/м2∙час. Коррозии подвергается железо. Тогда потеря массы металла 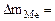 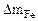 . . |
При расчете Km принимаем: 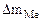 - [г]; S – [м2], τ - [час].
- [г]; S – [м2], τ - [час].
Тогда: Km = 
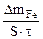 =
= 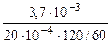 = 0,925 г/м2∙час.
= 0,925 г/м2∙час.
Рассчитываем глубинный показатель коррозии по формуле:
П = 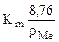 =
= 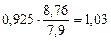 мм/год.
мм/год.
Ответ: Km = 0,925 г/м2∙час, П = 1,03 мм/год.
ЭЛЕКТРОЛИЗ РАСТВОРОВ
Таблица 11.1. Процессы протекающие на катоде при электролизе водных растворов
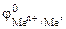 В В | Катио-ны в вод- ном рас- творе | Зоны | Процессы на катоде |
| -3,02 -2,99 -2,93 -2,92 -2,90 -2,89 -2,87 -2,71 -2,34 -1,67 | Li+, Rb+, Cs+ K+, Ba2+, Sr2+, Ca2+, Na+, Mg2+, Al3+ | I | Катионы этих металлов на катоде не восстанавли-ваются, а концентри-руются в околокатодном пространстве (католите). На катоде восстанавливаются только молекулы воды: 2Н2О + 2ē = 2ОН- + Н2 |
| -1,05 -0,76 -0,74 -0,44 -0,40 -0,28 -0,26 -0,14 -0,13 | Mn2+, Zn2+, Cr3+, Fe2+, Cd2+, Co2+, Ni2+, Sn2+, Pb2+ | II | 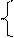 На катоде параллельно протекают два процесса: Меn+ + nē = Me 2Н2О + 2ē = 2ОН- + Н2 На катоде параллельно протекают два процесса: Меn+ + nē = Me 2Н2О + 2ē = 2ОН- + Н2 |
| 0,00 | Н+ | При электролизе кислоты 2Н+ + 2ē = Н2 | |
| +0,20 +0,23 +0,34 +0,80 +0,83 +0,85 +1,20 | Sb3+, Bi3+, Cu2+, Ag+, Pd2+, Hg2+, Pt2+ | III | Восстанавливаются только ионы этих металлов Меn+ + nē = Me |
Таблица 11.2. Последовательность окисления анионов на инертном аноде в водном растворе.
| Очередность окисления анионов | Процессы окисления на аноде. |
| 1. | Окисляются анионы бескислородных кислот (Cl-, Br-, J-, S2-, и др.) Например: 2Cl- -2ē = Cl2 |
| 2. | Окисляются ОН- ионы 4ОН- -4ē = О2 + 2Н2О |
Если в водном растворе присутствуют анионы кислородсодержащих кислот ( 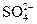 , , 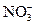 , , 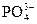 , и др.), то они на аноде не окисляются, а концентрируются в околоанодном пространстве (анолите). На аноде окиcляются только молекулы воды. 2H2O - 4е = О2+4H+ , и др.), то они на аноде не окисляются, а концентрируются в околоанодном пространстве (анолите). На аноде окиcляются только молекулы воды. 2H2O - 4е = О2+4H+ |
Примечание. Если анод изготовлен из металлов II или III зоны (растворимый анод), то при электролизе протекает только процесс его растворения Мe0 – nē = Men+
УРОВЕНЬ А

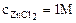
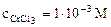 ε - ?
ε - ? 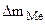 = 3,7·10-3 г. S = 20 см 2 ρFe = 7,9 г/см3 Km - ? П -?
= 3,7·10-3 г. S = 20 см 2 ρFe = 7,9 г/см3 Km - ? П -?