Устойчивость кислородсодержащих кислот хлора в ряду
HClO; HClO2; HClO3; HClO4:
| а) увеличивается | б) уменьшается |
| в) очень низкая - не могут быть выделены в свободном состоянии | г) достаточно высокая для выделения их в свободном состоянии |
Определите вещество-окислитель и укажите степень окисления элемента-окислителя в окислительно-восстановительной реакции
Br2 + NaOH ® NaBrO3 + NaBr + H2O
а) -1 б) +5 в) +1 г) 0.
5. Продуктами химического взаимодействия KCl + H2SO4(к) ® … являются:
а) HCl; KHSO4 б) Cl2;K2SO4; SO2; H2O
в) KСlO3; SO2; H2O г) KClO; S;H2O.
6. В цепочке химических реакций вещества х1 и х2
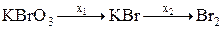
а) K2SO3; I2 б) K2S; Cl2 в) K2S, I2 г) K2SO4; Cl2
7. Укажите химическую реакцию, протекающую в водном растворе, для которой ионно-молекулярное уравнение имеет вид:
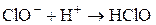
а) NaClO + HF ® HClO + NaF;
б) 2NaClO + H2SO4 ® 2HClO + Na2SO4;
в) KClO + HNO2 ® HClO + KNO2;
г) Ca(ClO)2 + H2SO4 ® 2HClO + CaSO4.
Укажите вещества, которые расположены в порядке уменьшения рН их водных растворов
а) HI; KI; KF б) KI; KF; HI
в) KF; KI;HI г) KI; HI; KF.
9. Br2 окрашивает органический растворитель (CCl4 или C6H6) в цвет
а) жёлто-зелёный б) синий в) малиновый г) оранжевый
В организме человека из галогенов в большем количестве содержится
а) F б) Cl в) Br г) I
Тестовые задания по теме: «Галогены»
Вариант № 9
1. Окислительно-восстановительные потенциалы галогенов, характеризующихся электронно-ионным уравнением Э2 + 2е- ® 2Э-
в ряду I2, Br2, Cl2, F2 :
| а) практически не изменяются | б) уменьшаются | в) увеличиваются |
| г) изменяются без явной закономерности |
2. Химическая связь для соединения РCl5
а) ионная б) координационная в) ковалентная г) ковалентная
неполярная полярная
Окислительные свойства кислородсодержащих кислот хлора в ряду
HClO; HClO2; HClO3; HClO4:
| а) увеличиваются | б) уменьшаются |
| в) не имеют закономерности | г) не характерны |
Определите вещество-восстановитель и укажите степень окисления элемента-восстановителя в окислительно-восстановительной реакции
KIO3 + Cl2 + KOH = K5IO6 +KCl + H2O
а) -5 б) +5 в) 0 г) +7.
5. Продуктами химического взаимодействия NaBr+H2SO4(к)®являются:
а) NaBrO3; SO2; H2O б) Br2; H2S; H2O; Na2SO4
в) HBr; Na2SO4 г) Br2; SO2; H2O; Na2SO4
6. В цепочке химических реакций вещества х1 и х2
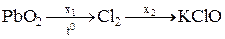
а) HClO; KNO3 б) HCl; KOH в) HCl; KCl г) KClO3; KOH
7. Укажите химическую реакцию, протекающую в водном растворе, для которой ионно-молекулярное уравнение имеет вид:
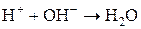
а) HClO4 + NaOH = NaClO4 + H2O;
б) HClO + NaOH = NaClO + H2O;
в) HCl + NH4OH = NH4Cl + H2O;
г) HF + NH4OH = NH4F + H2O.
Укажите вещества, которые расположены в порядке увеличения рН их водных растворов
а) HClO; NaClO; HClO4 б) NaClO; HClO; HClO4
в) HClO4; HClO; NaClO г) HClO; HClO4; NaClO.
9. I2 окрашивает органическую фазу (CCl4; C6H6) в цвет
а) оранжевый б) малиновый в) синий г) желто-коричневый
В составе земной коры из галогенов в большем количестве содержится
а) I б) Br в) Cl г) F
Тестовые задания по теме: «Галогены»
Вариант № 10
1. Для галогенов значения относительной электроотрицательности в соединениях F, Cl, Br, I:
| а) увеличиваются | б) уменьшаются | в) практически не изменяются |
| г) не имеют явной закономерности. |
2. Для соединений, в которых хлор проявляет валентность V, его состояние описывается электронной формулой:
а) 3S23p5 б) 3S23p43d1 в) 3S23p33d2 г) 3S13p33d3
