Методические указания к лабораторному практикуму по курсу
Практикум по
Общей и экологической биохимии
Часть I
«Аминокислоты. Белки.
Выделение и количественное
определение белков»
Минск
МГЭУ
Авторы:
зав. кафедрой биохимии и биофизики, канд. биол. наук Бокуть С.Б., преподаватель кафедры биохимии и биофизики Ячник Н.Н.,
доцент кафедры биохимии и биофизики Шейко Л.М.
аспирант кафедры биохимии и биофизики Сяхович В.Э.
Рекомендовано Советом Международного государственного
экологического университета им. А.Д. Сахарова, № 5 от 21.02.2002г.
Практикум по общей и экологической биохимии. Часть I: «Аминокис-лоты. Белки. Выделение и количественное определение белков» / Бокуть С.Б. и др. – Мн., 2002 – 55 с.
Практикум содержит учебно-методические материалы для проведения лабораторных работ по курсу "Общая и экологическая биохимия" со студентами 2-го курса. Для каждой лабораторной работы приводятся основы теории по конкретной теме, вопросы для подготовки к занятию, список рекомендуемой литературы, перечень заданий к занятию, описание используемых в лабораторной работе приборов, материалов и реактивов. Включены материалы, описывающие принципы методов качественного и количественного определения аминокислот, пептидов и белков. Приложение содержит информацию о строении и номенклатуре аминокислот.
Все лабораторные занятия написаны авторами настоящего издания совместно.
Соответствует учебной программе курса «Общая и экологическая биохимия» для студентов МГЭУ имени А.Д. Сахарова.
Практикум рекомендуется для студентов ВУЗов, обучающихся по специальностям медико-биологического профиля.
Ó С.Б. Бокуть, Н.Н. Ячник, Л.М. Шейко, В.Э. Сяхович, 2002
Ó Международный государственный экологический университет им. А.Д. Сахарова, 2002
 |
Содержание
| Аминокислоты. Белки. Выделение и количественное определение белков | |
| Лабораторная работа №1 Аминокислоты. Методы обнаружения и идентификации аминокислот. Качественные реакции на аминокислоты, пептиды и белки | |
| Лабораторная работа №2 Простые белки. Физико-химические свойства белков | |
| Лабораторная работа №3 Сложные белки. Методы выделения белков в гомогенном состоянии. Методы количественного определения белка. Определение белка неизвестной концентрации | |
| Приложение Строение и номенклатура аминокислот |
Методические указания к лабораторному практикуму по курсу
«Общая и экологическая биохимия»
Раздел «Аминокислоты. Пептиды. Белки»
Лабораторная работа № 1
| Темы: | I. Аминокислоты. Методы обнаружения и идентификации аминокислот |
| II. Качественные реакции на аминокислоты, пептиды и белки | |
| Цель работы: | - Ознакомление студентов с наиболее распространенными методами идентификации аминокислот - Освоение методов выявления белков, пептидов и индивиду-альных аминокислот в растворах по качественным реакциям |
Оборудование и материалы:
· Термостат
· Камера хроматографическая
· Бумага хроматографическая
· Пипетки стеклянные на 1мл и 5 мл
· Микропипетки автоматические
· Цилиндры мерные на 250мл и 100мл
· Колба емкостью 250мл
· Пробирки
· Штативы для пробирок
· Бумага фильтровальная
· Индикаторная бумага универсальная
· Сито нейлоновое
· Ванночка со льдом
Реактивы:
· Яичный белок
· Гидроксид натрия (NaOH), 10% раствор, 14.3 М раствор
· Сульфат меди (CuSO4), 2% раствор, 0.04М раствор
· Ацетат свинца (Pb(CH3COO)2), раствор
· Нитрит калия (натрия) (KNO2, NaNO2), 0.5% раствор
· Карбонат натрия (Na2CO3), 10% раствор
· Нитропруссид натрия (Na2[Fe(CN)5NO]), 10% раствор
· Нингидрин, 1% раствор
· Реактив Миллона
· a-нафтол, 0.2% спиртовой раствор
· Сульфониловая кислота, 1% раствор в 5% соляной кислоте
| · Мочевина, 40% раствор | · b-Аланин, 0.01% раствор |
| · о-фталевый диальдегид, раствор | · Аргинин |
| · Желатин, 1% раствор | · Аргинин, 3% раствор, 0.01% |
| · Фруктоза, 5% раствор | раствор |
| · Глиоксалевая кислота | · Аспарагиновая кислота |
| · Формалин, раствор | · Гистидин, 0.01% раствор |
| · Сахароза, 5% раствор | · Глицин |
| · Уксусная кислота, ледяная | · Глицин, 0.01% раствор |
| · Борная кислота, 2.5% раствор | · Глутаминовая кислота |
| · Азотная кислота (HNO3), конц. | · Метионин, 0.02% раствор |
| · Серная кислота (H2SO4), конц. | · Пролин, 0.01% раствор |
| · Соляная кислота (HCl), конц. | · Тирозин |
| · Фосфорная кислота (H3PO4), | · Триптофан, 0.01% раствор |
| конц. | · Цистеин, 0.02% раствор |
| · н-бутанол | · Смесь аминокислот (для хромато- |
| · Вода дистиллированная | графии) |
Теоретическая Часть
Аминокислоты
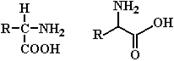 |
В процессах жизнедеятельности клетки главенствующую роль играют белки – биополимеры, построенные из мономерных единиц – L-a-аминокислот. Биологические свойства белков определяются, в основном, их аминокислотным составом, точнее порядком расположения аминокислот в полипептидной цепи, что в конечном итоге определяет пространственную структуру белка. Основными функциональными группами аминокислот являются их амино- и карбоксильные группы, которые связаны с одним и тем же (a) углеродным атомом (рис. 1.1).
Рис. 1.1 Два варианта изображения структурной формулы аминокислоты.
За исключением глицина, у которого R (см. рис. 1.1) представлен атомом водорода, у всех остальных протеиногенных аминокислот четыре группы, связанные с a-углеродным атомом, различны. Благодаря тетраэдрическому расположению четырех разных заместителей у a-углеродного атома, любая аминокислота (кроме глицина) обладает оптической активностью. При этом одни аминокислоты, входящие в состав белков, являются (при рН 7.0) право-вращающими, а другие – лево-вращающими. Тем не менее, вследствие того, что природные аминокислоты имеют пространственную конфигурацию L-глицеральдегида, все они относятся к L-a-аминокислотам.
Ионные формы аминокислот
Свободные аминокислоты включают, по крайней мере, две слабоионизованные группы: карбоксильную группу (–СОО¯ ) и аминогруппу (–NН3+). В растворе эти группы находятся в двух формах, заряженной и незаряженной, между которыми поддерживается протонное равновесие:
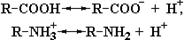 |
R–COOH и R–NH3+ являются протонированными партнерами, то есть кислотами, а R–COO¯ и R–NH2 – сопряженными основаниями (т.е. акцепторами протонов) соответствующих кислот. Следовательно, структура аминокислоты, изображенная на рис. 1.1, не может существовать в растворе, поскольку одна из указанных групп в той или иной степени ионизирована.
Вполне понятно, что суммарный заряд (алгебраическая сумма всех положительных и отрицательных зарядов) аминокислоты зависит от величины рН, то есть от концентрации протонов в растворе. Значение рН, при котором суммарный заряд аминокислоты равен нулю и она не перемещается в постоянном электрическом поле, называется ее изоэлектрической точкой (рI). Такая в целом незаряженная форма аминокислоты носит название цвиттериона. Для алифатических аминокислот цвиттерион имеет следующий вид:
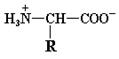
При увеличении или уменьшении рН по отношению к изоэлектрической точке происходит «перезарядка» аминокислоты и она утрачивает форму цвиттериона. В случае подкисления раствора, степень ионизации карбоксильной группы резко падает и аминокислота выступает в роли основания, присоединяя протоны.
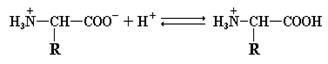
При повышении рН происходит обратный процесс: аминокислота, выступая в качестве кислоты, протоны отдает.