Аминокислоты. пептиды. белки
БИОХИМИЯ КАК НАУКА. ЭТАПЫ РАЗВИТИЯ БИОХИМИИ. МЕТОДЫ БИОХИМИЧЕСКИХ ИССЛЕДОВАНИЙ
Биологическая химия – это фундаментальная биомедицинская наука, которая изучает химический состав живых организмов и химические превращения биомолекул.
Изучение в курсе биохимии молекулярной организации клетки, механизмов регуляции биохимических реакций, которые лежат в основе физиологических функций организма человека в норме и патологии, имеет огромное значение для разработки способов и методов фармакологической коррекции нарушенных метаболических процессов.
Оновные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
1. Предмет и задачи биологической химии
1.1. Место биохимии среди других медико-биологических дисциплин.
1.2. Объекты изучения и задачи биохимии
2. Основные этапы развития биологической химии как науки
3. Разделы биохимии:
4. Современные направления развития биохимии
4.1. Достижения и перспективы развития биохимии, теоретической и молекулярной биологии, биотехнологии, генной инженерии и их значение для диагностики и лечения основных заболеваний человека – сердечно-сосудистых, онкологических, инфекционных и других.
4.2. Роль биохимии в выяснении молекулярно-генетических механизмов патогенеза заболеваний, выяснения значения наследственных и экологических факторов в возникновении патологических состояний и их влияния на продолжительность жизни населения.
5. Биохимические лабораторные исследования
5.1. Цель биохимических исследований
5.2. Критерии оценки использованного метода лабораторных исследований
5.3. Материал для диагностических исследований, принципы забора материала
5.4. Ошибки, имеющие место во время проведения лабораторных исследований
Граф логическая структура

Основные термины и их значение:
Статическая биохимия (связь с биоорганической химией, молекулярной биологией) исследует химический состав организмов.
Динамическая биохимияизучает превращение химических соединений и взаимосвязанных с ними превращений энергии в процессе жизнедеятельности.
Функциональная биохимиявыясняет связи между строением химических соединений и процессами их видоизменения, с одной стороны, и функцией субклеточных частиц специализированных клеток, тканей или органов, включающих в свой состав упомянутые вещества, с другой.
Медицинская биохимия (биохимия человека).
Клиническая биохимия как раздел медицинской биохимии
Биоэнергетика – раздел динамической биохимии, который изучает закономерности освобождения, аккумуляции и использования энергии в биологических системах.
Молекулярная генетика – раздел биохимии, раскрывающий закономерности сохранения и реализации генетической информации путем изучения структуры и функционирования информационных молекул – ДНК и РНК.
Электрофорез – физико-химический метод анализа, применяемый в биохимии для разделения белковых фракций.
ОБЩИЕ ЗАКОНОМЕРНОСТИ МЕТАБОЛИЗМА. МЕТАБОЛИЗМ УГЛЕВОДОВ, ЛИПИДОВ, БЕЛКОВ И ЕГО РЕГУЛЯЦИЯ
ВВЕДЕНИЕ
Обмен веществ представляет собой сложную систему химических реакций, связанных между собой через пластические компоненты, энергетическое обеспечение и общие регуляторы. Целями этих реакций является извлечение энергии и синтез биологических макромолекул, структура которых отвечает индивидуальной генетической программе организма.
Биохимическая схема обмена веществ включает цепи, каскады и циклы химических преобразований, составляющих в совокупности метаболические пути. Для того чтобы эти метаболические пути функционировали согласованно и удовлетворяли потребностям индивидуальных клеток, органов или организма в целом, они должны подвергаться строгой регуляции. Для регуляции метаболизма эволюционно сформировались различные механизмы, которые влияют на инструменты метаболизма, то есть на каталитическую активность ферментов.
Для нормального метаболизма характерны адаптационные изменения в период голодания, при физической нагрузке, беременности и лактации. Нарушения метаболизма возникают, например, при неполноценности питания, нехватке витаминов, дефиците тех или иных ферментов или при дисбалансе гормонов. Поэтому знания общих закономерностей обмена веществ в норме необходимо будущему врачу для понимания причин многих заболеваний.
В основе возникновения и развития большинства патологических процессов лежат биохимические изменения. Главным образом это относится к изменению обмена веществ основных биологических макромалекул: белков, углеводов и липидов. Понимание процессов обмена веществ включает знание структуры и функций макромолекул, а также особенностей их переваривания, всасывания, транспорта и непосредственно тех химических преобразований, которые происходят с данными веществами в живом организме. При этом важно рассматривать каждый метаболический процесс не изолированно, как искусственную схему, а учитывать особенности его протекания в различных тканях и органах, возможности его регуляции и, безусловно, его взаимосвязь с другими метаболическими путями.
Целью изучения модуля «Общие закономерности метаболизма. Метаболизм углеводов, липидов, белков и его регуляция»является: уметь интерпретировать общие закономерности обмена веществ, а также особенности метаболизма углеводов, липидов и белков в норме и при патологии для последующего использования этих данных в клинике внутренних болезней.
Общие закономерности метаболизма. Метаболизм углеводов, липидов, белков и его регуляция» включает следующие содержательные модули:
1. Метаболизм белков и его регуляция. Энзимопатии аминокислотного обмена
2. Роль ферментов и витаминов в обмене веществ
3. Метаболизм липидов и его регуляция
4. Обмен веществ и энергии
5. Метаболизм углеводов и его регуляция
АМИНОКИСЛОТЫ. ПЕПТИДЫ. БЕЛКИ
Введение
Аминокислоты рассматриваются как производные карбоновых кислот, в которых положение аминогруппы относительно карбоксильной принято указывать буквами: 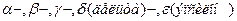 , что равносильно цифрам 2, 3, 4 и т. д. соответственно. Буквы греческого алфавита не употребляется в заместительной номенклатуре ИЮПАК.
, что равносильно цифрам 2, 3, 4 и т. д. соответственно. Буквы греческого алфавита не употребляется в заместительной номенклатуре ИЮПАК.
В природных объектах обнаружено около 300 разных аминокислот, но наиболее важными, постоянно встречающимися во всех пептидах и белках, являются 20 α –аминокислот (см. табл 1). Они кодируются генетическим кодом, и их принято называть протеиногенными (иногда каноническими).
Строение. Классификация и номенклатура. Стероизомерия
α -Аминокислоты — гетерофункциональные соединения, молекулы которых содержат аминогруппу и карбоксильную группу у одного и того же атома углерода.
 |
|
|


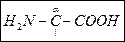
R
 |
 Заменимые и незаменимые аминокислоты
Заменимые и незаменимые аминокислоты
В зависимости от того, могут ли α –аминокислоты синтезироваться в организме или нет (т.е. должны поступать с пищей ), их делят на:
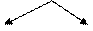 |


 |
| В | Валин | А | *Аргинин |
| Л | Лейцин | Л | Лизин |
| И | Изолейцин | Ф | Фенилаланин |
| Т | Треонин | Т | Триптофан |
| М | Метионин | Г | *Гистидин |
Для нормального роста детского организма необходимо обязательное поступление еще двух 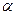 -аминокислот, хотя у взрослых они синтезируются в достаточных количествах. Эти аминокислоты называют частично заменимыми. Для синтеза тирозина и цистеина нужны незаменимые
-аминокислот, хотя у взрослых они синтезируются в достаточных количествах. Эти аминокислоты называют частично заменимыми. Для синтеза тирозина и цистеина нужны незаменимые 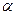 -аминокислоты, поэтому эти две кислоты называют условно заменимыми. Тирозин синтезируется в организме путем гидроксилирования фенилаланина, а для получения цистеина необходим метионин.
-аминокислоты, поэтому эти две кислоты называют условно заменимыми. Тирозин синтезируется в организме путем гидроксилирования фенилаланина, а для получения цистеина необходим метионин.
α -Аминокислоты необходимы для биосинтеза не только пептидов и белков, но и фосфолипидов, нуклеиновых оснований, порфириновых соединений, а также для выполнения таких специфических задач, как перенос аминогруппы, метильной группы, гуанидиновой группировки и др.
Основным источником α -аминокислот для человека и животных являются белки пищевых продуктов. В зависимости от содержания незаменимых аминокислот белки разделяют на полноценные и неполноценные. Например, белки молочных, рыбных, мясных продуктов, некоторых морепродуктов (мясо кальмара, краба), яиц, а также некоторые белки растительного происхождения (сои, гороха, фасоли) являются полноценными, так как они содержат все незаменимые аминокислоты в необходимых пропорциях. В основных группах пищевых продуктов среди незаменимых аминокислот преобладают лейцин и лизин, их содержание колеблется от 7,0 до 11% от общего содержания α -аминокислот (см. табл.). Относительно небольшое содержание в продуктах характерно для триптофана (не более 2%) и метионина (от 1.5 до 3.5%).
Таблица 2 Содержание белка в некоторых пищевых продуктах
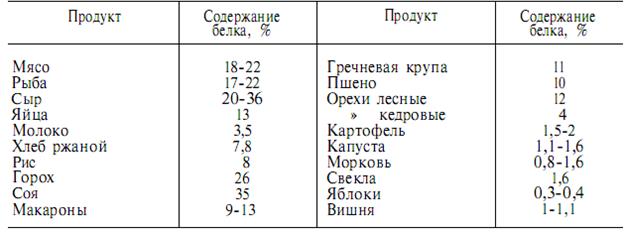
Смеси 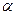 -аминокислот являются препаратами для парентерального питания (минуя желудочно-кишечный тракт) больных с тяжелыми патологическими осложнениями.
-аминокислот являются препаратами для парентерального питания (минуя желудочно-кишечный тракт) больных с тяжелыми патологическими осложнениями.
Номенклатура
Названия 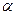 -аминокислот могут быть построены по заместительной номенклатуре, но практически всегда используются только их тривиальные названия, принятые номенклатурой ИЮПАК. Тривиальные названия
-аминокислот могут быть построены по заместительной номенклатуре, но практически всегда используются только их тривиальные названия, принятые номенклатурой ИЮПАК. Тривиальные названия 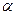 -аминокислот, как правило, связаны с источниками выделения. Простейшую аминокислоту, выделенную впервые из гидролизата желатины и имеющую сладкий вкус, назвали гликокол (от греч..glykys — сладкий и kolla — клей, т. е. «сладкий из клея»), позднее она получила название глицин.
-аминокислот, как правило, связаны с источниками выделения. Простейшую аминокислоту, выделенную впервые из гидролизата желатины и имеющую сладкий вкус, назвали гликокол (от греч..glykys — сладкий и kolla — клей, т. е. «сладкий из клея»), позднее она получила название глицин.
В названиях алифатических аминокислот по заместительной номенклатуре аминогруппа обозначается префиксом амино-, а карбоксильная группа как старшая — суффиксом -овая кислота. В названиях ароматических аминокислот в качестве родоначальной структуры используется бензойная кислота.
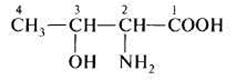 треонин 2-амино-З-гидроксибутановая кислота треонин 2-амино-З-гидроксибутановая кислота | 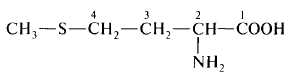 Метионин 2-амино-4-(метилтио)бутановая кислота Метионин 2-амино-4-(метилтио)бутановая кислота |
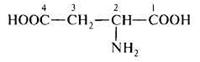 аспарагиновая кислота аминобутандиовая кислота аспарагиновая кислота аминобутандиовая кислота | 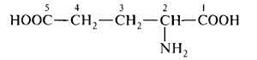 глутаминовая кислота 2-аминопентандиовая кислота глутаминовая кислота 2-аминопентандиовая кислота |
Стереоизомерия
Во всех (кроме глицина - ахиральна) природных 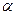 -аминокислотах
-аминокислотах 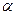 -углеродный атом асимметрический, причем у большинства этих соединений (кроме изолейцина и треонина) имеется только один хиральный центр. Поэтому они существуют в виде двух оптических изомеров (L- и D-энантиомеров) Почти все природные
-углеродный атом асимметрический, причем у большинства этих соединений (кроме изолейцина и треонина) имеется только один хиральный центр. Поэтому они существуют в виде двух оптических изомеров (L- и D-энантиомеров) Почти все природные 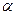 -аминокислоты имеют L-форму, а D-аминокислоты, как правило, не усваиваются живыми организмами. Интересно, что большинство аминокислот L-ряда имеют сладкий вкус, а аминокислоты D-ряда - горькие или безвкусные.
-аминокислоты имеют L-форму, а D-аминокислоты, как правило, не усваиваются живыми организмами. Интересно, что большинство аминокислот L-ряда имеют сладкий вкус, а аминокислоты D-ряда - горькие или безвкусные.
При написании проекционных формул Фишера стереоизомеров 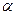 -аминокислот атом углерода центра хиральности переносят на пересечение вертикальной и горизонтальной прямых, при этом символ атома углерода не пишут. Старшую функциональную группу — карбоксильную группу — располагают наверху, а радикал — внизу. Энантиомер относят к L-стереохимическому ряду, если в стандартной проекционной формуле Фишера аминогруппа расположена слева, а положение NH2-группа справа соответствует D-ряду .
-аминокислот атом углерода центра хиральности переносят на пересечение вертикальной и горизонтальной прямых, при этом символ атома углерода не пишут. Старшую функциональную группу — карбоксильную группу — располагают наверху, а радикал — внизу. Энантиомер относят к L-стереохимическому ряду, если в стандартной проекционной формуле Фишера аминогруппа расположена слева, а положение NH2-группа справа соответствует D-ряду .

L-валин D-валин
Чистые L- или D-стереоизомеры могут за длительный срок самопроизвольно и неферментативно превращаться в эквимолярную смесь L- и D-изомеров. Этот процесс называют рацемизацией. Рацемизация каждой L-аминокислоты при данной температуре идёт с определённой скоростью. Это обстоятельство можно использовать для установления возраста людей и животных. Так, в твёрдой эмали зубов имеется белок дентин, в котором L-аспартат переходит в D-изомер при температуре тела человека со скоростью 0,01% в год. В период формирования зубов в дентине содержится только L-изомер, поэтому по содержанию D-аспартата можно рассчитать возраст обследуемого.
После смерти биохимические процессы прекращаются, и происходит медленная рацемизация аминокислот в результате химических превращений. Скорость рацемизации различна для отдельных аминокислот. Так, при температуре 25 °С и рН 7 аспарагиновая кислота рацемизуется в 4 раза быстрее, чем аланин. При понижении температуры скорость рацемизации существенно снижается, например, в случае аспарагиновой кислоты почти в 150 раз. Эти данные помогают определить, насколько древними являются биологические материалы, найденные во время археологических раскопок.
Стереоспецифичность характерна для реакций, протекающих только в живом организме.
Классификация аминокислот
Существуют разные подходы к классификации 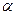 -аминокислот. Химическая классификация базируется на следующих основных признаках:
-аминокислот. Химическая классификация базируется на следующих основных признаках:
