Комплекс I – НАДН-KoQ-редуктаза, комплекс II – сукцинат-KoQ-редуктаза, но он существует отдельно от остальных комплексов
I комплекс цепи тканевого дыхания – НАДH∙H+-убихинон-оксидодуктаза.
Первый комплекс является самым большим в дыхательной цепи (представлен 23-30 субъединицами). Он катализирует перенос водорода от НАДH∙H+ на убихинон (рис. 5.1 и рис. 5.3). В его состав входят кофермент ФМН (флавинмононуклеотид) и железосерные белки, содержащие негеминовое железо. Функция этих белков заключается в разделении потока протонов и электронов: электроны переносятся от ФМН∙Н2 к внутренней поверхности внутренней мембраны митохндрий (обращенной к матриксу), а протоны – к внешней поверхности внутренней мембраны и затем высвобождаются в митохондриальныйметрикс.
При транспорте протонов и электронов редокс-потенциал первого комплекса снижается на 0,38 v, что вполне достаточно для синтеза АТФ. Однако в самом комплексе АТФ не образуется, а высвобождающаяся в результате работы комплекса энергия аккумулируется (см. ниже образование электро-химического потенциала) и частично рассеивается в виде тепла.
По своему строению ФМН – мононуклеотид, в котором азотистое основание представлено изоаллоксазиновым ядром рибофлавина, а пентозой является рибитол (иными словами, ФМН – это фосфорилированная форма витамина В2).
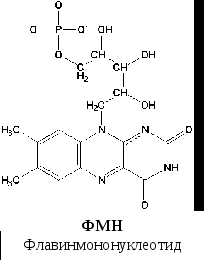
Функция ФМН заключается в акцепции 2 атомов водорода от НАДH∙H+ и передачи их железосерным белкам. Водород (2 электрона и 2 протона) присоединяется к атомам азота изоаллоксазинового кольца, при этом происходит внутримолекулярная перегруппировка двойных связей с образованием промежуточного семихинона – соединения свободнорадикальной природы (на схеме представлено суммарноеуравнение реакции, где R – остальная часть молекулы)
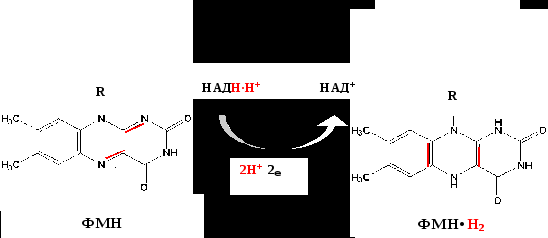
II комплекс цепи тканевого дыхания –сукцинат-убихинон-оксидоредуктаза.
Этот комплекс имеет меньшую молекулярную массу и также содержит железосерные белки. Сукцинат-убихинон-оксидоредуктаза катализирует перенос водорода от сукцината на убихинон. В состав комплекса входит кофермент ФАД (флавин-аденин-динуклеотид) и фермент сукцинатдегидрогеназа, который является одновременно ферментом цикла Кребса. Ацил~SКоА, 3-фосфо-глицерат и диоксиацетонфосфаттакже являются ФАД-зависимыми субстратами тканевого дыхания и с помощью этого кофермента контактируют со вторым комплексом.
Энергия включения водорода субстратов во II комплекс цепи тканевого дыхания рассеивается в основном в виде тепла, так как на этом участке цепи редокс-потенциал снижается незначительно и этой энергии для синтеза АТФ мало.
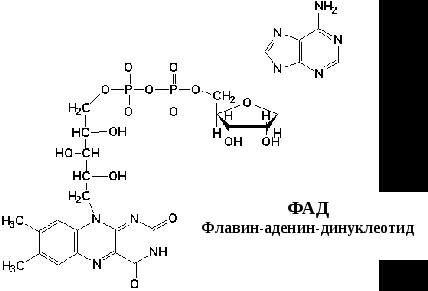
Процесс восстановления ФАД протекает аналогично таковому ФМН.
Кофермент Q или убихинон - гидрофобное соединение, является компонентом клеточных мембран, содержится в большой концентрации, относится к группе витаминов.относится к группе витаминов.
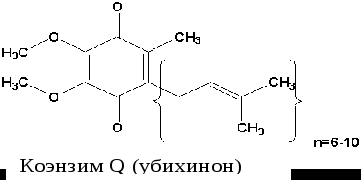
Убихинон (коэнзим Q). Убихинон – небольшая липофильная молекула, по химическому строению представляющая собой бензохинон с длинной боковой цепью (число изопреноидных единиц колеблется от 6 у бактерий до 10 у млекопитающих).
В дыхательной цепи коэнзим Q является своеобразным депо (пулом) водорода, который он получает от различных флавопротеинов. Липофильный характер молекулы убихинона обуславливает его способность свободно перемещаться в липидной фазе митохондриальной мембраны, перехватывая протоны и электроны не только от I и II комплексов дыхательной цепи, но и захватывая из митохондриального матрикса протоны. При этом убихинон восстанавливается с образованием промежуточного свободнорадикального продукта – семихинона .
Восстановленная форма убихинона – убихинол – передаёт протоны и электроны на III комплекс дыхательной цепи.
Цитохромоксидаза имеет высокую степень сродства к кислороду и может работать при его низких концентрациях.
аа3 - состоит из 6 субъединиц каждая из которых содержит гем и атом меди. 2 субъединицы составляют цитохром а, а остальные 4 относятся к цитохрому а3.
Коэффициент Р/О – это число молей неорганического фосфата, пошедшего на образование АТФ в расчете на каждый атом поглощенного кислорода.
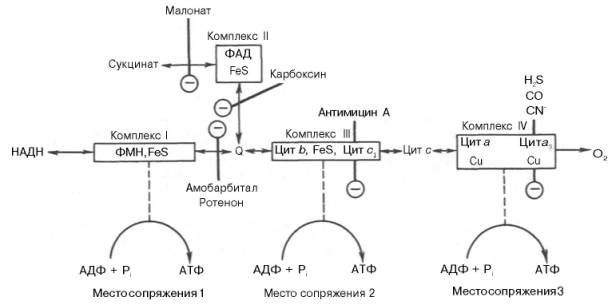
Взаимное расположение компонентов дыхательной цепи с указанием мест фосфорилирования и специфических ингибиторов.
Билет N 12
1.Ферментативный ингибитор — вещество, замедляющее протекание ферментативной реакции.
Обратимые ингибиторы связываются с ферментом слабыми нековалентными связями и при определённых условиях легко отделяются от фермента. Обратимые ингибиторы бывают конкурентными и неконкурентными
-Конкурентное ингибирование В этом случае ингибитор связывается в активном центре фермента и конкурирует за него с субстратом. Конкурентный ингибитор обычно структурно схож с субстратом, однако фермент не способен катализировать реакцию в присутствии ингибитора из-за отсутствия у последнего необходимых функциональных групп. Неконкурентное ингибирование
Неконкурентный ингибитор не мешает связыванию субстрата с ферментом. Он способен присоединяться как к свободному ферменту, так и к фермент-субстратному комплексу с одинаковой эффективностью. Ингибитор вызывает такие конформационные изменения, которые не позволяют ферменту превращать субстрат в продукт, но не влияют на сродство фермента к субстрату.
Необратимое ингибирование наблюдают в случае образования ковалентных стабильных связей между молекулой ингибитора и фермента. Чаще всего модификации подвергается активный центр фермента, В результате фермент не может выполнять каталитическую функцию.Пример лекарственного препарата, действие которого основано на необратимом ингибировании ферментов, - широко используемый препарат аспирин. Противовоспалительный нестероидный препарат аспирин обеспечивает фармакологическое действие за счёт ингибирования фермента циклооксигеназы, катализирующего реакцию образования простагландинов из арахидоновой кислоты. В результате химической реакции ацетильный остаток аспирина присоединяется к свободной концевой NH2-группе одной из субъединиц циклооксигеназы.Это вызывает снижение образования продуктов реакции простагландинов, которые обладают широким спектром биологических функций, в том числе являются медиаторами воспаления.
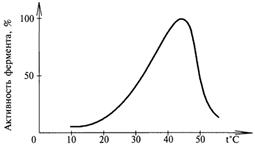
2. С повышением температуры ускоряется движение молекул, что приводит к повышению вероятности взаимодействия реагирующих веществ и повышению энергии веществ, за которым следует ускорение каталитической активности, но при высоких температурах происходит денатурация ферментов. Что приводит к снижению скорости катализа.
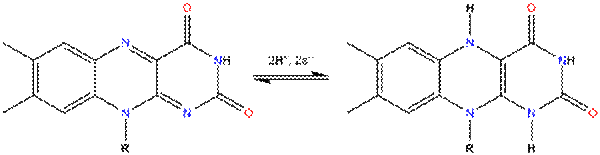
3. FAD может быть восстановлен до FADH2, при этом он принимает два атома водорода.
К числу ферментов дыхательной цепи относятся - флавинзависимые дегидрогеназы (флавопротеиды), у которых простетической группой служат ФМН и ФАД.
4.Амилаза слюны относится к классу гидролаз. Субстратом амилазы слюны является крахмал и гликоген Амилаза слюны катализирует 1,4 гликозидные связи.Специфичность амилазы слюны обусловлена особой формой молекулы фермента, точно соответствующей форме молекулы субстрата. Определить специфичность амилазы слюны можно.Для этого нужно взять 2 субстрата- крахмал и сахарозу и добавить туда разбавленную слюну и поставить в термостат, затем провести пробу Тромера. Пробирка в которой находится крахмал расщепляется амилазой слюны, а в пробирке с сахарозой расщепления не происходит, вследствие чего можно сказать. Что она не является спец. Субстратом для амилазы слюны.
5. Для объяснения механизма окислительного фосфорилирования выдвигалось много гипотез.
Общепринятой в настоящее время является хемиосмотическая теория, предложенная Митчеллом в 1961 году.
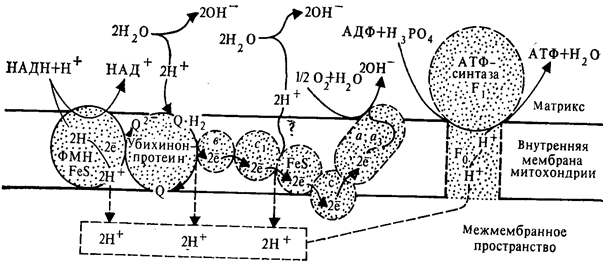
Рис. 3. Схема сопряжения дыхания и фосфорилирования согласно хемиосмотической теории.
1. Процесс протекает на внутренней мембране митохондрий, где располагается дыхательная цепь ферментов.
2. Внутренняя мембрана непроницаема для протонов (и большинства катионов). Это свойство обусловливает возможность неравномерного распределения заряженных частиц по обе стороны мембраны. Движение протонов и электронов имеет строго определенную направленность.
3. Ферменты-переносчики дыхательной цепи располагаются в мембране зигзагообразно. Они способны не только акцептировать атомарный водород от окисляемых субстратов, но и транспортировать его в поперечном направлении через мембрану. Достигая противоположного (внешнего) слоя мембраны, переносчик освобождает в водное пространство снаружи от нее протоны, а электроны при участии дополнительных переносчиков направляются обратно к внутреннему слою мембраны и передаются очередному ферменту дыхательной цепи. Для восстановления ферментам кроме электронов нужны протоны, которые поступают из внутреннего пространства за счет вынужденной диссоциации воды. Всего при переносе пары электронов (от НАД.2Н) по дыхательной цепи происходит выталкивание в межмембранное пространство трех пар протонов.Таким образом, протоны транспортируются от внутреннего слоя мембраны со стороны матрикса к наружному со стороны межмембранного пространства, а электроны передаются по цепи ферментов, достигая конечного акцептора электронов – кислорода
4. В результате такого перераспределения электрических зарядов со стороны матрикса внутренняя мембраны оказывается заряженной отрицательно и щелочной (в ней накапливается избыток ОН- -ионов за счет реакции (1) и остающихся ОН- от диссоциации воды в матриксе), а со стороны межмембранного пространства - заряженной положительно и более кислой (за счет транспорта протонов). Возникает электрохимический протонный градиент, в форме которого на замкнутой мембране и происходит концентрация энергии.
Из-за разницы в концентрации и электрическом потенциале на протоны, находящиеся в наружном пространстве, действует сила, стремящаяся перевести их через мембрану во внутреннее пространство.
5. ^ Возвращение протонов в матрикс осуществляется с помощью фермента аденозинтрифосфатазы (АТФ-азы или АТФ-синтазы). Этот фермент встроен во внутреннюю мембрану. Возникающие изменения в мембране (электрохимический потенциал) передаются АТФ-синтазе, которая активизируется и катализирует синтез АТФ. Таким образом, окислительное фосфорилирование – синтез АТФ из АДФ и неорганического фосфата за счет энергии электрохимического потенциала.
БИЛЕТ 13
Определение активности органоспецифических ферментов для диагностики заболеваний. Примеры.
Определение активности трипсина в сыворотке крови является надежнымферментным тестом при диагностике острого панкреатита.Субстратная специфичность трипсина ограничена разрывомтолько тех пептидных связей, в образовании которых участвуют карбоксильные группы лизина и аргинина. Определение активности трансаминаз
в сыворотке крови при заболеваниях сердца следует отнести к дифференциально-диагностическим лабораторным тестам. Повышение уровнятрансаминаз в сыворотке крови отмечено, при некоторыхзаболеваниях мышц, в частности при обширных травмах, гангрене конечностей и прогрессивной мышечной дистрофии. В диагностике инфаркта миокарда определение активности креатинкиназы,АсАТ и ЛДГ в сыворотке крови – наиболее чувствительные тесты. Повышение активности указанных ферментов, особенно креатинкиназы, является постоянным и наиболее высоким. Важно также исследование в сы-
воротке крови изоферментных спектров креатинкиназы (повышение ак-
тивности изофермента MB) и ЛДГ (увеличение активности изоферментов
ЛДГ1 и ЛДГ2).
2)Изобразить график зависимости скорости ферментативной реакции от концентрации субстрата? Почему существует такая зависимость? Физический смысл константы Михаэлиса?
Графики зависимости скорости ферментативной реакции от концентрации субстрата в присутствии конкурентного ингибитора.
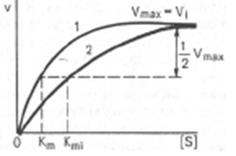 Vmax и Vi - максимальные скорости
Vmax и Vi - максимальные скорости
реакции; Кm и Kmi - константа Михаэлиса соответственно в отсутствие (1) и в присутствии (2)ингибитора.
При конкурентном типе ингибирования ингибитор увеличивает значение
Кm, не оказывая влияния на максимальную скорость Vmax. Этоозначает, что при достаточно высокой концентрации субстрата [S] ингибитор вытесняется молекулами субстрата из комплексаES.При неконкурентном ингибировании ингибитор снижает величину максимальной скорости. Если при этом величина Кm не уменьшается, то говорято полностью неконкурентном ингибировании.Физический смысл Км заключается в том, что она представляет собой константу равновесия между двумя реакциями, приводящими к распаду фермент-субстратного комплекса и той реакцией, которая ведет к образованию этого комплекса.
3)Механизмы переноса протонов и электронов через внутреннюю мембрану митохондрий на примере Q-цикла.
1)НАД-зависимая дегидрогеназарасположена на матриксной поверхности внутренней мембраны митохондрий отдает пару электронов водорода на ФМН-зависимую дегидрогеназу. При этом из матрикса пара протонов переходит также на ФМН и в результате образуется ФМН Н2. В это время пара протонов, принадлежащих НАД выталкивается в межмембранное пространство.
2)ФАД-зависимая дегидрогеназа отдает пару электронов на КоQ а пару протонов выталкивает в межмембранное пространство. Получив электроны КоQ принимает из матрикса пару протонов и превращается в КоQ Н2.
3)КоQ Н2 выталкивает пару протонов в межмембранное пространство, а пара электронов передается на цитохромы и далее на кислород с образованием молекулы воды.
В итоге при переносе пары электронов по цепи из матрикса в межмембранное пространство перекачивается 6 протонов (3 пары), что ведет к созданию разницы потенциалов и разницы рН между поверхностями внутренней мембраны.
4)Разница потенциалов и разница рН обеспечивают движение протонов через протонный канал обратно в матрикс.
5)Такое обратное движение протонов ведет к активации АТФ-синтазы и синтезу АТФ из АДФ и фосфорной кислоты. При переносе одной пары электронов (т.е. трех пар протонов) синтезируется 3 молекулы АТФ.
4)К какому классу ферментов относится каталаза крови? Какую реакцию она катализирует? Какова ее биологическая роль? Чему равны показатели каталазы и каталазное число в норме?
Каталаза относится к классу оксиредуктаз. Широко распространена в природе. Особенно высокая концентрация ее найдена в печени и эритроцитах крови. Каталаза является сложным белком, простетическая группа ее идентична окисленномугему. Фермент содержит 0,09%железа.Катализирует расщепление перекиси водорода, образующийся при тканевом дыхании, и тем самым препятствует накоплению ее в токсических для организма количествах. Перекись водорода разлагается каталазой на воду и молекулярный кислород.
Биологическая роль каталазы состоит в защите организма от ядовитого действия перекиси водорода и ее производных, образующихся в живых тканях в результате функционирования флавопротеиновых оксидаз.Каталазное число в норме варьирует от 12 до 22. Показателем каталазы называют отношение каталазного числа к количеству миллионов красных кровяных телец в одном мкл исследуемой крови.
5)Строение и функционирование митохондриальной АТФ-синтетазы(V-комплекс).
АТФ синтетаза – вещество которое обеспечивает синтез АТФ из АДФ и H3PO4 под действием энергии, полученной при переносе протонов и электронов вдоль дыхательной цепи. АТФ синтетаза состоит из двух единиц сопряжения.
F1 в сторону матрикса митоходрий.
F0 в мебране.
В молекуле имеется активная часть куда подходит АДФ и Н3РО4.Далее эти вещества плотно упаковываются и образуется АТФ(при этом актив. Центр закрыт).
АДФ+Н3РО4+энергия->АТФ +Н2О
Билет
1. А) Термолабильность ферментов.Скоростьхимическихреакцийзависитот
температуры, поэтомукатализируемые ферментами реакции также чувствительны к изменениям температуры. При температуре 100°С почти все ферменты утрачивают свою активность (исключение фермент мышечной ткани – миокиназа). Оптимальной для действия большинства ферментов теплокровных животных является температура 40°С; При низких температурах (0°С и ниже) ферменты не разрушаются, хотя активность их падает почти до нуля.Биохимические реакции повышаются в 2 раза при повышении температуры на 10°С и, наоборот - температурный коэффициент. Но из-за белковой природы фермента тепловая денатурация при повышении температуры будет снижать эффективную концентрацию фермента с соответствующим снижением скорости реакции.На термолабильность ферментов определенное влияние оказывает концентрация субстрата, рН среды и другие факторы.
. 
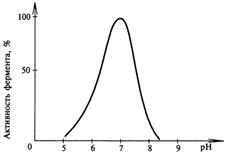
Б)Зависимость активности фермента от рН-среды. Большинство ферментов проявляет максимальную активность при значениях рН, близких к нейтральным. Лишь некоторые ферменты активны в сильно кислой или сильно щелочной среде. Например, активность пепсина - максимальна при рН 1,5 - 2,5. В щелочной среде активны ферменты, локализованные в кишечнике. Изменение оптимального для данного фермента значения рН-среды может привести к изменению третичной стурктуры фермента, что скажется на его активности. С другой стороны, при изменении рН может измениться
ионизация субстрата, что повлияет на образование фермент-субстратного комплекса.Имеет значение, кроме того, состояние ионизации субстратов и кофакторов.
В) Специфичность действия ферментов - одно из главных их свойств. Специфичность - это избирательность фермента по отношению к субстрату (или субстратам).Различают несколько видов специфичности.
Стереохимическая субстратная специфичность - фермент катализирует превращение только одного стереоизомера субстрата. Например, фумаратгидратаза катализирует присоединение молекулы воды к кратной связи фумаровой кислоты, но не к ее стереоизомеру - малеиновой кислоте.
Абсолютная субстратная специфичность - фермент катализирует превращение только одного субстрата. Например, уреаза катализирует гидролиз только мочевины.
Групповая субстратная специфичность - фермент катализирует превращение группы субстратов сходной химической структуры. Например, алкогольдегидрогеназа катализирует превращение этанола и других алифатических спиртов, но с разной скоростью.
Г)Влияние на активность ферментов активаторов и ингибиторов.К числу факторов, повышающих активность ферментов, относятся катионы металлов и некоторые анионы. Чаще всего активаторами ферментов являются катионы Mg2+, Zn2+, K+ и Со2+, а из анионов - Сl-.Ингибиторы тормозят действие ферментов. Ингибиторами могут быть как эндогенные, так и экзогенные вещества.
2. Изоферменты, или изоэнзимы,– это множественныеформыфермента, ка-
тализирующиеодну и тужереакцию, ноотличающиесядруготдругапо
физическим и химическимсвойствам, в частности по сродству к субстрату, максимальной скорости катализируемой реакции и регуляторным свойствам.
Изучение появления изоферментов ферментов в сыворотке крови может представлять интерес в диагностике органических и функциональных поражений органов и тканей. По изменению содержания изоферментов в сыворотке крови можно судить как о топографии патологического процесса, так и о степени поражения органа или ткани.
3.По строению ферменты делятся напростые (однокомпонентные) и сложные(двухкомпонентные). Простой фермент состоит только из белковой части; в состав сложного фермента входит белковая и небелковая составляющие. Иначе сложный фермент называют холоферментом. Белковую часть в его составе называют апоферментом, а небелковую - коферментом.Особенностью сложных ферментов является то, что отдельно апофермент и кофермент не обладают каталитической активностью.
Каталитический центр простого фермента представляет собой сочетание нескольких аминокислотных остатков, расположенных на разных участках полипептидной цепи. Образование каталитического центра происходит одновременно с формированием третичной структуры белковой молекулы фермента. Чаще всего в состав каталитического центра простого фермента входят остатки серина, цистеина, тирозина, гистидина, аргинина, аспарагиновой и глутаминовой кислот.В сложных ферментах роль каталитического центра выполняет кофермент, который связывается с апоферментом в определенном участке - кофермент связывающем домене.
Аллостерический центр представляет собой участок молекулы фермента, в результате присоединения к которому какого-то низкомолекулярного вещества изменяется третичная структура белковой молекулы фермента, что влечет за собой изменение его активности. Аллостерический центр является регуляторным центром фермента.
Адсорбционный центр- участок активного центра молекулы фермента, на котором происходит сорбция (связывание) молекулы субстрата. Он формируется одним, двумя, чаще тремя радикалами аминокислот, которые обычно расположены рядом с каталитическим центром. Главная его функция - связывание молекулы субстрата и передача этой молекулы каталитическому центру в наиболее удобном положении (для каталитического центра). Эта сорбция происходит только за счет слабых типов связей и потому является обратимой.
