Тема: Водневий показник. Гідроліз солей
Мета:розглянути суть процесу гідролізу; вміти складати молекулярні та йонні рівняння реакцій гідролізу; прогнозувати зміщення рівноваги гідролізу; обчислювати величину рН середовища; використовувати кількісні характеристики гідролізу для опису кислотно – основних властивостей біологічних рідин.
Забезпечення заняття: періодична система хімічних елементів Д.І. Менделєєва; таблиця розчинності кислот, основ і солей у воді; розчини: ZnCl2, Na2CO3, NaCl, (NH4)2CO3, CH3COONa; індикатори: універсальний індикаторний папірець, фенолфталеїн, метилоранж;пробірки, газовий пальник, пробіркотримач.
Конкретні цілі:
- робити висновки щодо кислотності біологічних рідин на підставі водневого показника;
- знати випадки гідролізу солей;
- складати молекулярні та йонні рівняння реакцій гідролізу;
- пояснювати вплив різних факторів на зміщення рівноваги гідролізу;
- вміти обчислювати та експериментально визначати рН;
- знати роль гідролізу в біохімічних процесах.
Зміст заняття
Чиста вода належить до слабких електролітів. Вона дуже погано проводить електричний струм. Незначне число молекул води розпадаються на йони:
H2O 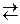 H+ + OH-
H+ + OH-
Kд = 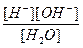
[H2O] – const.
[H2O] = [H+][OH-]
Кд[H2O] = Kw = [H+][OH-]
Kw – йонний добуток води.
При температурі 250С Кw = 1∙10-14, а [H+]=[OH-]=10-7моль/дм3.
Концентрація йонів Н+ характерезує кислотність середовища, яку для зручності виражають значенням водневого показника, або точніше, показника йонів Гідрогену рН.
За відомим значенням рН можна оцінити кислотність будь-якого розчину.
У водному розчині рН середовища практично змінюється в інтервалі від 0 до 14. Величину рН можна обчислити теоретично, якщо відома концентрація йонів Гідрогену, за формулою:
рН = - lg[H+],
або визначити експериментально за допомогою приладів, які називаються рН- метрами. Для приблизної оцінки рН розчинів використовують кислотно-основні індикатори.
Аналогічно, рОН називається гідроксильним показником:
рОН = -lg[OH-].
pH + pOH = 14.
Характеристика кислотності середовища за величиною рН
| Інтервал рН | Характеристика середовища | [H+], моль/дм3 |
| 0-3 4-6 8-10 11-14 | Сильнокислотне Слабкокислотне Нейтральне Слабколужне Сильнолужне | 10-1- 10-3 10-4 – 10-6 10-7 10-8 – 10-10 10-11 – 10-14 |
Величина рН є важливою характеристикою всіх фізіологічних рідин, від значення якої залежить функція клітин, тканин, органів та організму людини в цілому. Шлунковий сік, кров, слина, сік підшлункової залози та інші рідини характеризуються певним значенням рН, яке може змінюватись у вузькому інтервалі. Відхилення значення рН від норми (особливо це стосується крові) призводить до виникнення тяжких патологічних станів організму, оскільки йони Н+ і ОН- визначають структуру та біологічні функції білків, нуклеїнових кислот, активність ферментів та інших клітинних компонентів організму.
