Основания, их классификация и свойства на основе представлений об электролитической диссоциации, практическое применение.
Основания – сложные вещества, состоящие из атомов металлов и одной или нескольких гидроксильных групп.
Ме+1(ОН)n
Классификация:
| Основания | ||||
| По растворимости в воде | Растворимые (щёлочи) NaOH, Ba(OH)2 и ещё 6 щелочей | Нерастворимые Cu(OH)2, Fe(OH)2, Fe(OH)3 | ||
| По количеству ОН-групп | Одиокислотные NaOH, KOH | Двухкислотные Cu(OH)2, Fe(OH)2 | Многокислотные Al(OH)3, Fe(OH)3 | |
| По характеру | Основной ZnOH, Cu(OH)2 | Амфотерный Al(OH)3, Zn(OH)2 | ||
Основания – это электролиты, при диссоциации которых в качестве анионов образуется только гидроксид – ионы.
NaOH ⇄ Na+ + OH– ; Ba(OH)2
Химические свойства:
1) Диссоциируют на ионы NaOH ⇄ Na+ + OH– — изменяют окраску индикатора.
2) С кислотами:
NaOH + HCl → NaCl + H2O
Na+ + OH– + H+ + Cl– → Na+ + Cl– + H2O
OH– + H+ → H2O
3) С кислотными оксидами:
CO2 + 2NaOH → Na2CO3 + H2O
CO2 + 2Na+ + 2OH– → 2Na+ + CO32– + H2O
CO2 + 2OH– → CO32– + H2O
4) С солями:
2NaOH + CuSO4 → Na2SO4 + Cu(OH)2↓
5) При нагревании разлагаются:
Cu(OH)2 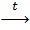 CuO + H2O
CuO + H2O
6) Амфотерные основания:
Zn(OH)2 + 2NaOH 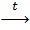 Na2ZnO2 + 2H2O
Na2ZnO2 + 2H2O
Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
Применение:
1) в химической промышленности;
2) в производстве сахара и т.п.;
3) в производстве мыла и моющих средств;
Билет №15 (2)
Глюкоза – представитель моносахаридов, строение, физические и химические свойства, применение.
Глюкоза относится к классу углеводов. Она входит в число моносахаридов с общей формулой C6H12O6, являясь одним из изомеров этого типа моносахаридов (другой изомер – фруктоза).
Молекула глюкозы может иметь циклическое строение (в твёрдом состоянии) или линейное (в водных растворах). В растворах устанавливается равновесие:
Исходя из строения линейной формы, можно заключить, что глюкоза является альдегидом (альдегидная функциональная группа) и многоатомным спиртом (пять групп ОН).
В природе глюкоза образуется в результате фотосинтеза и содержится во всех органах зелёных растений (особенно в винограде, фруктах, ягодах). Животные и человек получают глюкозу из растений, которые они используют в пищу.
Глюкоза играет огромную роль в живом организме. В ходе химических превращений, протекающих внутри живых тканей, освобождается необходимая для жизнедеятельности энергия.
Глюкоза – бесцветное, твёрдое вещество, сладкое на вкус и хорошо растворимая в воде.
Химические свойства:
1) Реакции гидроксильной группы
а) C6H12O6 + Cu(OH)2 → соединение глюкозы с медью (раствор синего цвета)
б) C6H12O6 + Cu(OH)2 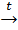 глюконовая кислота + Cu2O↓
глюконовая кислота + Cu2O↓
2) Реакции альдегидной группы:
3) Специфическое свойство – брожение:
а) спиртовое брожение
C6H12O6 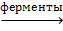 2C2H5OH + 2CO2↑
2C2H5OH + 2CO2↑
б) молочнокислое брожение в) маслянокислое брожение
Применение: в кондитерской промышленности, в медицине. Широко используются продукты брожения глюкозы.
Билет №16 (1)
