Исследование состава общих липидов методом тонкослойной хроматографии
Наиболее эффективным и широко применяемым методом фракционирования сложных смесей липидов является хроматография. Главную роль при аналитическом фракционировании играет адсорбционная хроматография в тонком слое сорбента. Этот метод также применяется в препаративных целях, когда разделению подвергается небольшое количество липидов (50—300 мг). Если масса липидов превышает 300 мг, используют колоночную хроматографию, хотя по разделяющей способности и времени разделения этот метод часто уступает тонкослойной и газовой хроматографии.
Разделение веществ при тонкослойной хроматографии происходит благодаря различию в способности адсорбироваться на поверхности сорбента, что определяется характером функциональных групп, входящих в структуру отдельных липидов.
Техника ТСХ значительно отличаются от колоночной хроматографии. В последнем случае перед началом разделения колонка тщательно промывается подвижной фазой (элюентом). При ТСХ проба (до 10-20 мкл) наносится на сухой адсорбент (чаще всего силикагель). После высыхания стартового пятна пластину помещают в герметично закрытую камеру и один ее конец погружают в подходящий растворитель (подвижную фазу). Капиллярные силы обуславливают движение растворителя по сорбенту, в результате чего образец на старте растворяется и его компоненты движутся в направлении движения растворителя. Как только фронт растворителя приблизится к противоположному краю пластины, ее вынимают и сушат. В общем случае необходимо проведение дополнительной операции, позволяющей обнаружить разделившиеся пятна компонентов пробы (опрыскивание реагентами для химического окрашивания, просмотр под ультрафиолетовым облучением и т.д.). Обычно для окраски используют следующие реагенты: нингидрин для аминокислот, родамин В для липидов, хлорид сурьмы для стероидов и терпенов, серную кислоту с последующим нагреванием практически для всех органических соединений (происходит обугливание), перманганат калия в серной кислоте для углеводородов, анисовый альдегид в серной кислоте для углеводов, пары брома для олефинов и т.д.Отношение расстояний, пройденных пятном и растворителем, обозначается Rf. Величина Rf зависит не только от свойств вещества, но и от условий проведения хроматографии (вида сорбента, растворителя).
ТСХ обладает рядом преимуществ перед хроматографией на бумаге или в колонках: большая разрешающая способность, большая скорость разделения, более широкий выбор сорбентов, простое обнаружение пятен и легкость выделения вещества с хроматограмм.
Большую разрешающую способность ТСХ обеспечивают два фактора. Во-первых, отношение массы разделяемого вещества к массе сорбента составляет от 1:103 до 1:104, тогда как при колоночной хроматографии это отношение обычно близко к 1:50. Во-вторых, частицы сорбента при ТСХ могут быть очень мелкими (менее 0,1 мм). Меньший размер пятен означает также, что концентрация вещества в пятнах выше, что повышает чувствительность анализа в 10-100 раз по сравнению с хроматографией на бумаге.
ТСХ позволяет осуществлять двумерную хроматографию. В этом случае после проведения хроматографии в одном направлении пластину высушивают и повторно хроматографируют под прямым углом к направлению первоначального движения растворителя с использование отличного от первого элюирующего раствора (рисунок 17). При этом часто происходит разделение веществ, не разделившихся первым растворителем.
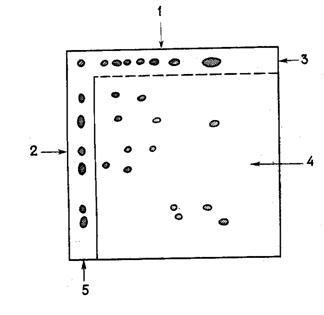
Рисунок 17. Двумерная тонкослойная хроматография.
1 - направление движения первого растворителя; 2 – направление движения второго растворителя; 3 – разделение при применении только второго растворителя; 4 – разделение при последовательном применении обоих растворителей; 5 – разделение при применении только первого растворителя.
Хроматография на силикагеле. Силикагель является продуктом полимеризации ортокремниевой кислоты (H4SiO4). Он выпускается рядом фирм в виде зерен различной величины. Адсорбционные свойства силикагеля обусловлены присутствием на поверхности зерен гидро-ксильных групп, которые за счет водородных связей взаимодействуют друг с другом и водой. Гидратированный силикагель мало активен как адсорбент. При нагревании от 50 до 150°С происходит дегидратация, которая приводит к значительному увеличению адсорбционной способности силикагеля. Нагревание при температуре свыше 150°С способствует образованию силоксановых связей (Si—О—Si), что снижает адсорбционную способность силикагеля. Такой силикагель уже нельзя реактивировать путем присоединения воды. Лучший способ избежать образования силоксановых групп — активация силикагеля нагреванием в вакууме при температуре 50°С.
Отечественный силикагель КСК с успехом может быть использован как для тонкослойной, так и для колоночной хроматографии Его измельчают в шаровой мельнице с фарфоровыми шарами. Обычно 1 кг силикагеля размалывают в течение 5 ч. Затем просеивают через капроновое сито, отбирая фракцию с размером частиц 100—200 МЕШ. Размолотый и просеянный силикагель обрабатывают кислотой для удаления примесей железа и других тяжелых металлов. 100 г адсорбента нагревают при 100°С в течение 10 ч при помешивании с 1,5 л 10%-го раствора азотной кислоты. Кислоту декантируют, силикагель промывают 5 л дистиллированной воды, 1 л 0,5%-го водного раствора аммиака, снова 5 л дистиллированной воды и 1 л метанола. Затем сушат на воздухе в течение 6-8 ч и активируют 24 ч при температуре 110- 115°С. Хранят в герметически закрытом сосуде.
Пластинки тонкого закрепленного слоя силикагеля готовят заранее следующим образом.
Стеклянные пластинки тщательно моют свежеприготовленной хромовой смесью и ополаскивают много раз водопроводной водой, затем 3-5 раз дистиллированной, вытирают чистой марлей, протирают спиртом и хранят в чистом полиэтиленовом пакете в отдельной коробке.
Для нанесения на пластины используют смесь силикагеля марки КСК и химически чистого гипса CaSO4. Гипс предварительно просушивают в течение 24 ч при температуре 115-120°С. Оба адсорбента измельчают и просеивают через сито с числом 200 меш.
Для приготовления сорбционной массы 6 г силикагеля и 0,35 г гипса энергично встряхивают 3-5 мин в колбочке (можно с резиновой пробкой, защищенной пленкой). Смесь высыпают в ступку и постепенно, при тщательном растирании, небольшими порциями по 3-5 мл добавляют дистиллированную воду — всего 15-17 мл. Смешивание силикагеля и гипса с водой заканчивают в течение 1,5-2 мин (следить по секундомеру!). Полученная масса должна быть однородна и без пузырьков воздуха.
Готовую смесь тонкой непрерывной струей выливают в центр пластинки и покачиванием пластинки распределяют ее ровным слоем по всей поверхности. Пластинку сушат при комнатной температуре 24 ч на столике с уровнем, а затем активируют в сушильном шкафу при температуре 105°С в течение 40 мин. Если пластинки не используют сразу, их хранят в эксикаторе над СаС12.
Материалы и оборудование: камера для проведения тонкослойной хроматографии, подогреваемый столик для нанесения проб, шприц гамильтоновский емкостью 5-10 мкл, пульверизатор, пластины для ТСХ с нанесенным силикагелем, хлороформенные растворы (20 мг/м л) фосфолипида, холестерина, моно-, ди- и триацилглицерина, жирной кислоты, анализируемый экстракт липидов, «проявляющий раствор» - смесь гексана, диэтилового эфира и уксусной кислоты в соотношении 70:30:2.
Ход работы
На пластине с силикагелем мягким простым карандашом нанести стартовую линию на расстоянии 1,5 см от края пластины. Отметить точки нанесения проб.
Нанести на отметки по 5 мкл исследуемых растворов:
1. Исследуемый хлороформенный экстракт;
2. Раствор фосфолипида в хлороформе (20 мг/мл);
3. Раствор холестерина в хлороформе(20 мг/мл);
4. Раствор моноацилглицерина в хлороформе;
5. Раствор диацилглицерина в хлороформе;
6. Раствор триглицерида в хлороформе;
7. Раствор жирной кислоты в хлороформе.
Все работы с органическими растворителями проводить только в вытяжном шкафу. Пары органических растворителей взрывоопасны! Хлорсодержащие растворители – гепатотропные яды!
При нанесении необходимо получить возможно меньший диаметр пятна, не нарушая слой силикагеля. Для этого растворы наносить дробно, дожидаясь подсыхания каждой нанесенной порции. Для ускорения высыхания нанесение проб проводить на пластины, помещенные на подогретый до температуры 500С столик.
После нанесения проб на пластину поместить ее под углом в камеру со смесью растворителей, количество которой должно обеспечивать слой жидкости на дне камеры в 0,8-1,0 см.
Хроматографирование производить до достижения фронта растворителей верхнего края пластины.
Пластину извлечь из камеры и высушить в вытяжном шкафу до исчезновения запаха растворителей.
Для проявления отдельных липидных фракций пластины поместить в камеру, насыщенную парами йода. Йод, растворяясь в липидах, окрашивает их в темно-желтый цвет (интенсивность окраски зависит от длительности проявления).
На проявленных хроматограммах фракции липидов располагаются в порядке возрастания величин Rf следующим образом: фосфолипиды, холестерин, моноацилглицерины, диацилглицерины, свободные жирные кислоты, триглицериды, эфиры холестерина.
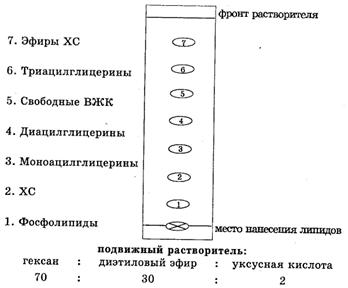
Измерить расстояния от линии фронта до пятен отдельных фракций и рассчитать Rf..
По сравнению с контрольными пробами идентифицировать липиды, содержащиеся в исследуемой пробе.
Контрольные вопросы
24. Классификация хроматографических методов по сродству к неподвижной фазе.
25. Особенности хроматографии биологических макромолекул.
26. Почему в большинстве случаев в процессе хроматографического процесса используется изменение силы элюента? Преимущества и недостатки непрерывных и ступенчатых градиентов силы элюентов.
27. Каким образом можно повысить силу элюента при ионообменной хроматографии? При распределительной хроматографии? При аффинной хроматографии?
28. Почему для ионообменной хроматографии белков используют, главным образом, слабые иониты?
29. Как влияет скорость элюции на разрешение хроматографии.
30. Какие факторы влияют на разрешение хроматографического процесса?
31. Какой хроматографический метод вы выбрали бы для очистки сывороточных иммуноглобулинов? Почему?
32. Сравните преимущества и недостатки колоночной и тонкослойной хроматографии.
ЛИТЕРАТУРА
6. Остерман Л.А.Методы исследования белков и нуклеиновых кислот: Пособие для студентов. - М.: МЦНМО, 2002.
7. Скоупс Р. Методы очистки белков. М., 1985.
8. Остерман Л.А. Хроматография белков и нуклеиновых кислот. М., 1985.
9. Якубке Х.-Д., Ешкайт X. Аминокислоты, пептиды, белки. М., 1985.
10. Виноградова Р.П., Цудзевич Б.А., Храпунов Б.А. Физико-химические методы в биохимии. – Киев, Вища Школа. Головное из-во, 1983. – 287 с.
11. Лабораторное руководство по хроматографическим и смежным методам/ Под ред.О. Микеша. М., 1982. Т. 1.
12. Фрайфелдер Д. Физическая биохимия. М., 1980.
13. Жидкостная колоночная хроматография/ Под ред. 3. Дейла, К. Мацека, Я. Янака. М., 1978. Т. 1; Т. 2.
Приложение № 1.
ПРОТОКОЛ ЛАБОРАТОРНОЙ РАБОТЫ № ... от "___" ______200_ г.
1. НАЗВАНИЕ РАБОТЫ
2. ЦЕЛЬ РАБОТЫ
3. МАТЕРИАЛЫ И МЕТОДЫ
В данном разделе приводятся перечень использованных в работе реактивов, приборов, оборудования и материалов; описание методик.
Цель написания раздела – учесть все особенности работы (квалификация реактивов, класс точности измерительных приборов и мерной посуды и т.д.), которые могут сказаться на полученных результатах. Не следует включать материалы, перечисленные в методичке, но не использованные в работе.
4. ХОД И РЕЗУЛЬТАТЫ РАБОТЫ
В данном разделе приводятся особенности проведения работы, в том числе отклонения от общепринятых методик, обусловленные ошибками в постановке, погрешностями при приготовлении растворов и реактивов и т.д., а также описание результатов работы.
5. ОБОБЩЕНИЕ РЕЗУЛЬТАТОВ РАБОТЫ
В данном разделе приводятся калибровочные графики, расчеты, обсуждение полученных результатов.
6. ВЫВОДЫ
ПОДПИСЬ, ДАТА
[1] Если в работе используют два типа гелей (концентрирующий и разделяющий), то в кассету сначала на высоту 85-95 мм от дна заливают раствор для полимеризации разделяющего геля. На него осторожно наслаивают воду и кассету оставляют в вертикальном положении до полимеризации геля. Воду удаляют, на поверхность разделяющего геля наносят смесь для полимеризации концентрирующего геля до полного заполнения кассеты и вставляют шаблон-гребенку.
[2] Для аналитических целей рекомендуется отношение длины к диаметру колонки 10:1 или 20:1. При обессоливании используют более короткие и широкие колонки.
[3] Объем наносимого образца при аналитическом разделении должен быть по возможности небольшим (2-3% от общего объема колонки — Vt). При обессоливании его можно увеличить до 20-30%. Рекомендуемая концентрация белка — 1%. При анализе высокомолекулярных белков концентрацию уменьшают до 0,1-0,5%.
[4] На всех стадиях обработки ионита фильтрование может быть заменено декантацией или центрифугированием.
[5] Если ДЭАЭ-целлюлозу используют не сразу, ее заливают водой и хранят при температуре 40С с добавлением следовых количеств толуола.
