Состояние равновесия. Принцип Ле-Шателье.
Состояние равновесия. Принцип Ле-Шателье.
Принцип Ле Шателье — Брауна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
1. Влияние температуры. В каждой обратимой реакции одно из направлений отвечает экзотермическому процессу, а другое - эндотермическому.

Прямая реакция - экзотермическая, а обратная реакция - эндотермическая. Влияние изменения температуры на положение химического равновесия подчиняется следующим правилам:
При повышении температуры химическое равновесие смещается в направлении эндотермической реакции, при понижении температуры - в направлении экзотермической реакции.
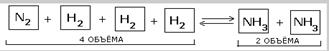
2. Влияние давления. Во всех реакциях с участием газообразных веществ, сопровождающихся изменением объема за счет изменения количества вещества при переоходе от исходных веществ к продуктам, на положение равновесия влияет давление в системе.
Влияние давления на положение равновесия подчиняется следующим правилам:
При повышении давления равновесие сдвигается в направлении образования веществ (исходных или продуктов) с меньшим объемом;
при понижении давления равновесие сдвигается в направлении образования веществ с большим объемом
3. Влияние концентрации. Влияние концентрации на состояние равновесия подчиняется следующим правилам:
При повышении концентрации одного из исходных веществ равновесие сдвигается в направлении образования продуктов реакции;
при повышении концентрации одного из продуктов реакции равновесие сдвигается в направлении образования исходных веществ.
Дисперсные системы могут быть бесструктурными (свободнодисперсными) и структурированными (связнодисперсными). Структурированные Дисперсные системы пронизаны сеткой-каркасом из соединённых между собой частиц (капель, пузырьков) дисперсной фазы, вследствие чего обладают некоторыми механическими свойствами твёрдых тел (подробнее см. Дисперсная структура, Гели). Характерная особенность Дисперсные системы - высокая свободная энергия как следствие сильно развитой межфазной поверхности; поэтому Дисперсные системы обычно (кроме лиофильных Дисперсные системы) термодинамически неустойчивы. Они обладают повышенной адсорбционной способностью, химической, а иногда и биологической активностью. Дисперсные системы - основной объект изученияколлоидной химии
.
Смачивание
Смачивание — это поверхностное явление, заключающееся во взаимодействии жидкости с поверхностью твёрдого тела или другой жидкостью при условии, что присутствует третья (обычно, но не обязательно, газовая) фаза, причём происходит одновременный контакт всех этих трёх не смешивающихся фаз. Смачивание ответственно за растекание жидкости по твёрдой поверхности, за форму лежащих на ней капель, за пропитывание порошков и пористых веществ (капиллярные явления) и др.Смачивание бывает двух видов:1) Иммерсионное (вся поверхность твёрдого тела контактирует с жидкостью) 2) Контактное (состоит из 3х фаз-твердая, жидкая, газообразная). Смачивание зависит от соотношения между силами сцепления молекул жидкости с молекулами (или атомами) смачиваемого тела (адгезия) и силами взаимного сцепления молекул жидкости (когезия).
ПАВ
Пове́рхностно-акти́вные вещества́ (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела фаз, вызывают снижение поверхностного натяжения.
Поверхностно-активные вещества (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела фаз, вызывают снижение поверхностного натяжения.
Первым и самым популярным ПАВ, которому уже многие тысячи лет, является мыло. И ежегодно, несмотря на конкуренцию новых моющих и чистящих средств, сперва на основе алкилбензолсульфоната, а теперь и других, в мире потребляется более 9 млн. т. мыла. Именно мыло остается наиболее распространенным в мире ПАВ.
Благодаря моющим, смачивающим, эмульгирующим, диспергирующим и другим ценным свойствам ПАВ находят широкое применение в производстве моющих и чистящих средств, косметических и фармацевтических препаратов. А также для производства латекса, каучука, полимеров, в добыче, транспортировке и переработке нефти и др.
Пав- ы - это химические чистящие, моющие, а также средства защиты растений, текстиля, кожи и бумаги, строительных материалов, ингибиторов коррозии. Большая часть ПАВ (порядка 60 %) приходится на производство моющих средств (СМС - синтетические моющие средства).
Основным сырьем для производства ПАВ служат продукты нефтепереработки и нефтехимического синтеза: низкомолекулярные и высшие парафины, олефины, синтетические жирные кислоты, высшие жирные спирты, алкилпроизводные бензола и фенола и др.
Адсорбция
Газы редко растворяются в твердых телах, т. е. редко проникают внутрь кристаллов. Зато существует иной способ поглощения газов твердыми телами. Молекулы газа скапливаются на поверхности твердого тела - это своеобразное прилипание называется адсорбцией[3]. Итак, адсорбция происходит тогда, когда молекула не может проникнуть внутрь тела, но зато успешно цепляется за его поверхность.
Адсорбция широко используется в химической промышленности. Молекулы различных газов, адсорбируясь на поверхности, приходят в тесное соприкосновение одна с другой и легче вступают в химические реакции.
Для ускорения химических процессов что используют как уголь, так и мелко раздробленные металлы - никель, медь и другие.
Вещества, ускоряющие химическую реакцию, называются катализаторами.
Осмос
Среди животных тканей есть своеобразные пленки, которые обладают способностью пропускать через себя молекулы воды, оставаясь непроницаемыми для молекул растворенных в воде веществ.
Свойства этих пленок являются причиной физических явлений, носящих название осмотических (или просто осмоса).
Представьте себе, что такая полупроницаемая перегородка делит на две части трубкуt изготовленную в форме перевернутой буквы П. В одно колено трубки наливается раствор, а в другое колено - вода или другой растворитель. Налив в оба колена одинаковое количество жидкостей, мы с удивлением установим,; что при равенстве уровней равновесия нет. Через короткое время жидкости устанавливаются на разных уровнях. При этом повышается уровень в том колене, где находится раствор. Вода, отделенная от раствора полупроницаемой перегородкой, стремится разбавить раствор. Это явление и носит название осмоса, а разность высот называется осмотическим давлением.
В чем же причина, вызывающая осмотическое давление? В правом колене сосуда (рис. 5.2) давление осуществляется одной лишь водой. В левом колене полное давление складывается из давления воды и давления растворенного вещества. Но сообщение открыто только для воды, и равновесие при наличии полупроницаемой перегородки устанавливается не тогда, когда давление справа равно полному давлению слева, а тогда, когда давление чистой воды равно "водяной" доле давления раствора. Возникающая разница полных давлений равна давлению растворенного вещества.
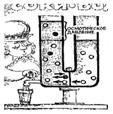
Рис. 5.2
Этот избыток давления и есть осмотическое давление. Как показывают опыты и расчет, осмотическое давление равняется давлению "газа", состоящего из растворенного вещества, занимающего тот же объем. Неудивительно поэтому, что осмотическое давление измеряется, внушительными числами. Осмотическое давление, возникающее в 1 л воды при растворении 20 г сахара, уравновесило бы столб воды высотой в 14 м.
Рискуя возбудить у читателя неприятные воспоминания, разберем теперь, как -связано с осмотическим давлением слабительное действие растворов некоторых солей. Стенки кишечника полупроницаемы для ряда растворов. Если соль через стенки кишечника не проходит (такова глауберова соль), то в кишечнике возникает осмотическое давление, которое отсасывает воду через ткани из организма в кишечник.
Почему очень соленая вода не утоляет жажды? Оказывается, и в этом виновато осмотическое давление. Почки не могут выделять мочу с осмотическим давлением, которое больше, чем давление в тканях организма. Поэтому организм, получивший соленую морскую воду, не только не отдает ее тканевым жидкостям, но напротив выделяет с мочой воду, отнятую у тканей.
Индикаторы
Индикаторы − органические вещества, принимающие характерную окраску в нейтральной, кислотной и щелочной среде, в зависимости отзначения рН.
Метилоранж, или метиловый оранжевый (индикатор на кислотную среду) становится розовым в сильнокислотном растворе, а фенолфталеин(индикатор на щелочную среду) − малиновым в сильнощелочном растворе.
гидролиза) а наоборот, влево, из-за связывания ионов меди в практически нерастворимый сульфид меди.
Уравнение Нернста
Зависимость окислительно-восстановительного потенциала, отвечающего полуреакции восстановления перманганат-иона в кислой среде (и, как уже отмечалось, одновременно полуреакции окисления катиона Mn2+ до перманганат-иона в кислой среде) от перечисленных выше определяющих его факторов количественно описывается уравнением Нернста
φ(MnO4–, H+ / Mn2+) = φo(MnO4–, H+ / Mn2+) + RT / 5Fln[MnO4–][H+]8 / [Mn2+].
В общем случае уравнение Нернста принято записывать в условной форме
φ(Ox/Red) = φo(Ox/Red) + RT/(nF) ln [Ox]/[Red],
отвечающей условной записи полуреакции восстановления окислителя
Ox + ne- = Red
Каждая из концентраций под знаком натурального логарифма в уравнении Нернста возводится в степень, соответствующую стехиометрическому коэффициенту данной частицы в уравнении полуреакции, n – число принимаемых окислителем электронов, R – универсальная газовая постоянная, T – температура, F – число Фарадея.
Измерить окислительно-восстановительный потенциал в реакционном сосуде во время протекания реакции, т.е. в неравновесных условиях, невозможно, так как при измерении потенциала электроны должны передаваться от восстановителя к окислителю не непосредственно, а через соединяющий электроды металлический проводник. При этом скорость передачи электронов (силу тока)нужно поддерживать очень малой за счет приложения внешней (компенсирующей) разности потенциалов. Иначе говоря, измерение электродных потенциалов возможно только в равновесных условиях, когда прямой контакт между окислителем и восстановителем исключен.
Поэтому квадратными скобками в уравнении Нернста обозначены, как обычно, равновесные (в условиях измерения) концентрации частиц. Хотя потенциалы окислительно-восстановительных пар во время протекания реакции нельзя измерить, их можно вычислить, подставляя в уравнение Нернста текущие, т.е. отвечающие данному моменту времени концентрации.
Если рассматривается изменение потенциала по мере протекания реакции, то сначала это начальные концентрации, затем концентрации, зависящие от времени, и, наконец, после прекращения реакции, равновесные.
По мере протекания реакции вычисляемый по уравнению Нернста потенциал окислителя уменьшается, а отвечающий второй полуреакции потенциал восстановителя, напротив, увеличивается. Когда эти потенциалы выравниваются, реакция прекращается, и система приходит в состояние химического равновесия.
Электрохимическая коррозия
Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов называют электрохимической коррозией. Не следует путать с электрохимической коррозией коррозию однородного материала, например, ржавление железа или т.п. При электрохимической коррозии (наиболее частая форма коррозии) всегда требуется наличие электролита (Конденсат, дождевая вода и т. д.), с которым соприкасаются электроды - либо различные элементы структуры материала, либо два различных соприкасающихся материала с различающимися окислительно-восстановительными потенциалами. Если в воде растворены ионы солей, кислот, или т.п., электропроводность ее повышается, и скорость процесса.
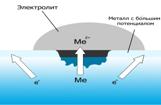
При соприкосновении двух металлов с различными окислительно-восстановительными потенциалами и погружении их в раствор электролита, например, дождевой воды с растворенным углекислым газом CO2, образуется гальванический элемент, так называемый коррозионный элемент. Он представляет собой не что иное, как замкнутую гальваническую ячейку. В ней происходит медленное растворение металлического материала с более низким окислительно-восстановительным потенциалом; второй электрод в паре, как правило, не корродирует. Этот вид коррозии особо присущ металлам с высокими отрицательными потенциалами. Так, совсем небольшого количества примеси на поверхности металла с большим редокспотенциалом уже достаточно для возникновения коррозионного элемента. Особо подвержены риску места соприкосновения металлов с различными потенциалами, например, сварочные швы или заклёпки.
Если растворяющийся электрод коррозионно-стоек, процесс коррозии замедляется. На этом основана, например, защита железных изделий от коррозии путём лужения или оцинковки - олово или цинк имеют более отрицательный потенциал, чем железо, поэтому в такой паре железо восстанавливается, а олово или цинк должны корродировать. Однако в связи с образованием на поверхности олова или цинка оксидной плёнки процесс коррозии сильно замедляется.
Электрохимическая коррозия протекает интенсивнее, если в катод вкраплён металл, менее активный, чем корродирующий. Например, если корродирует сталь (а сталь - это сплав железа и углерода в котором частично образуется карбид железа) роль таких участков играет карбид железа (FeC).
Атмосферная коррозия
- протекает во влажном воздухе при обычной температуре. Поверхность металла покрывается плёнкой влаги, содержащей растворённый кислород. Интенсивность разрушения металла возрастает с ростом влажности воздуха, а также содержанием в нём газообразных оксидов углерода, серы, при наличиив металле шероховатостей, трещин облегчающих конденсацию влаги.
Почвенная коррозия
- её подвержены трубопроводы, кабели, подземные сооружения. В этом случае металлы соприкасаются с влагой почвы, содержащей растворённый кислород. Во влажной почве, с повышенной кислотностью трубопроводы разрушаются в течение полугода после их укладки (конечно, если не принять меры по их защите).
Электрическая коррозия
- происходит под дейстивем блуждающих токов, возникающих от посторонних источников (линии электропередач,электрические железные дороги, различные электроустановки, работающие на постоянном электрическом токе). Блуждающие токи вызывают разрушение газопроводов, нефтепроводов,электрокабелей, различных сооружений. Под действием электрического тока на находящихся на земле металлических предметах появляются участки входа и выхода электронов - катоды и анады. На анодных участках наблюдается наиболее интенсивное разрушение.
Использование ингибиторов стало возможным только по одной причине, они при взаимодействии с металлом создают на его поверхности пленку, которая состоит из трудно растворимых соединений. Тем самым создается покрытие, которое отличается высокой прочностью. Кстати, толщина ингибиторного покрытия намного меньше, чем толщина любого искусственного антикоррозионного покрытия.Такая защита часто используется в котельных, где внутри котлов всегда агрессивная среда.
В настоящее время еще в стадии проектирования строительные компании стараются собрать всю информацию, касающуюся характера агрессивных воздействий и условия эксплуатации металлических конструкций. От собранной информации будут зависеть проектные решения, то есть сегодня во главу угла ставятся в основном показатели, которые будут влиять на срок эксплуатации здания или сооружения.
Лабораторные исследования и современные разработки сегодня принимаются во внимание в первую очередь при проведении антикоррозионных работ. А использование новейших материалов является залогом успешной защиты металлических конструкций от коррозии.
Особенно большое значение придается натурным обследованиям уже существующих зданий и сооружений. Именно на их примере можно с большой вероятностью определить качество и долговечность антикоррозийных материалов. Кстати, в этой области накоплен достаточно большой опыт.
Сегодня говорить о том, что коррозия металла как процесс его разрушения практически побежден, преждевременно. И проблем здесь хватает. Но ученые прилагают все усилия, чтобы коррозия металла как можно меньше доставляла неудобств в процессе эксплуатации металлических конструкций.
Все больше появляется методов борьбы с этим процессом, все больше появляется материалов, которые гарантируют эффективную защиту. На исследования тратятся большие финансовые средства, поэтому коррозия металла должна отступить в будущем, а точнее сказать, сдать свои позиции. Коррозия металлов и меры борьбы с ней – это одна из главных задач, которую ставят перед собой строители, начиная поднимать новый объект.
силикатов, являются Si, O, Al, Fe2+, Fe3+, Mg, Mn, Ca, Na, K, а также Li, B, Be, Zr, Ti, F, H, в виде (OH)1− или H2O и др.
Сегодня природные силикатные материалы широко используются в строительстве и промышленности - как в качестве сырья, так и конечного продукта.
Кремнезем служит сырьем для цементной промышленности - базовой в производстве современных строительных материалов. Силикатные глины - основное сырье для изготовления строительной керамики - кирпича и черепицы.
Кварцевый песок также издревле используют для изготовления стекла и керамики, в качестве различных добавок и в чистом виде. Негорючий гидросиликат асбест широко применяется для изготовления теплозащитных изделий и покрытий.
Минералы алюминия
Состояние равновесия. Принцип Ле-Шателье.
Принцип Ле Шателье — Брауна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
1. Влияние температуры. В каждой обратимой реакции одно из направлений отвечает экзотермическому процессу, а другое - эндотермическому.

Прямая реакция - экзотермическая, а обратная реакция - эндотермическая. Влияние изменения температуры на положение химического равновесия подчиняется следующим правилам:
При повышении температуры химическое равновесие смещается в направлении эндотермической реакции, при понижении температуры - в направлении экзотермической реакции.
2. Влияние давления. Во всех реакциях с участием газообразных веществ, сопровождающихся изменением объема за счет изменения количества вещества при переоходе от исходных веществ к продуктам, на положение равновесия влияет давление в системе.
Влияние давления на положение равновесия подчиняется следующим правилам:
При повышении давления равновесие сдвигается в направлении образования веществ (исходных или продуктов) с меньшим объемом;
при понижении давления равновесие сдвигается в направлении образования веществ с большим объемом

3. Влияние концентрации. Влияние концентрации на состояние равновесия подчиняется следующим правилам:
При повышении концентрации одного из исходных веществ равновесие сдвигается в направлении образования продуктов реакции;
при повышении концентрации одного из продуктов реакции равновесие сдвигается в направлении образования исходных веществ.
Дисперсные системы могут быть бесструктурными (свободнодисперсными) и структурированными (связнодисперсными). Структурированные Дисперсные системы пронизаны сеткой-каркасом из соединённых между собой частиц (капель, пузырьков) дисперсной фазы, вследствие чего обладают некоторыми механическими свойствами твёрдых тел (подробнее см. Дисперсная структура, Гели). Характерная особенность Дисперсные системы - высокая свободная энергия как следствие сильно развитой межфазной поверхности; поэтому Дисперсные системы обычно (кроме лиофильных Дисперсные системы) термодинамически неустойчивы. Они обладают повышенной адсорбционной способностью, химической, а иногда и биологической активностью. Дисперсные системы - основной объект изученияколлоидной химии
.Смачивание
Смачивание — это поверхностное явление, заключающееся во взаимодействии жидкости с поверхностью твёрдого тела или другой жидкостью при условии, что присутствует третья (обычно, но не обязательно, газовая) фаза, причём происходит одновременный контакт всех этих трёх не смешивающихся фаз. Смачивание ответственно за растекание жидкости по твёрдой поверхности, за форму лежащих на ней капель, за пропитывание порошков и пористых веществ (капиллярные явления) и др.Смачивание бывает двух видов:1) Иммерсионное (вся поверхность твёрдого тела контактирует с жидкостью) 2) Контактное (состоит из 3х фаз-твердая, жидкая, газообразная). Смачивание зависит от соотношения между силами сцепления молекул жидкости с молекулами (или атомами) смачиваемого тела (адгезия) и силами взаимного сцепления молекул жидкости (когезия).
ПАВ
Пове́рхностно-акти́вные вещества́ (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела фаз, вызывают снижение поверхностного натяжения.
Поверхностно-активные вещества (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела фаз, вызывают снижение поверхностного натяжения.
Первым и самым популярным ПАВ, которому уже многие тысячи лет, является мыло. И ежегодно, несмотря на конкуренцию новых моющих и чистящих средств, сперва на основе алкилбензолсульфоната, а теперь и других, в мире потребляется более 9 млн. т. мыла. Именно мыло остается наиболее распространенным в мире ПАВ.
Благодаря моющим, смачивающим, эмульгирующим, диспергирующим и другим ценным свойствам ПАВ находят широкое применение в производстве моющих и чистящих средств, косметических и фармацевтических препаратов. А также для производства латекса, каучука, полимеров, в добыче, транспортировке и переработке нефти и др.
Пав- ы - это химические чистящие, моющие, а также средства защиты растений, текстиля, кожи и бумаги, строительных материалов, ингибиторов коррозии. Большая часть ПАВ (порядка 60 %) приходится на производство моющих средств (СМС - синтетические моющие средства).
Основным сырьем для производства ПАВ служат продукты нефтепереработки и нефтехимического синтеза: низкомолекулярные и высшие парафины, олефины, синтетические жирные кислоты, высшие жирные спирты, алкилпроизводные бензола и фенола и др.
