Средние соли кислородсодержащих кислот
Номенклатура солей.
Средние соли кислородсодержащих кислот
Названия средних солей состоят из традиционных названий ка-тионов и анионов. Если элемент в образуемых им оксоанионах про-являет одну степень окисления, то название аниона оканчивается на -ат:
(NH4)2CO3 - карбонат аммония; K4SiO4 - ортосиликат калия;
NaBiO3 - висмутат натрия; LiBO2 - метаборат лития.
В случае двух степеней окисления ещё используют окончание -ит:
BaSeO4 - селенат бария; FeAsO4 - ортоарсенат железа(III);
BaSeO3 - селенит бария; Fe(AsO2)2 - метаарсенит железа(II).
Если степеней окисления элемента в анионах может быть более двух, то для самой низкой (обычно +1) применяют приставку гипо-с окончанием -ит:
Na2N2O2 - гипонитрит натрия; Ca(H2PO2)2 - гипофосфит кальция.
Последнее вещество является средней солью, поскольку в этом анионе два атома водорода присоединены непосредственно к атому фосфора и не проявляют кислых свойств.
Названия анионов, образованных элементом в степени окисления +7, имеют приставку пер-и окончание -ат:
H3OClO4 - перхлорат оксония; KMnO4 - перманганат калия;
Ag5IO6 - ортопериодат серебра; SrIO4 - метапериодат стронция.
Соли поли- тио- и пероксокислот называются по тем же прави-лам, сохраняя соответствующую приставку от названия кислоты:
Mg2P2O7 - дифосфат магния; Cs3PO2(O2)2 - дипероксофосфат цезия; К2SO3(О2) - пероксосульфат калия; Rb2S2O2 - тиосульфит рубидия.
Кислые и основные соли
Если в состав соли входят атомы водорода, которые при диссо-циации проявляют кислотные свойства и могут быть замещены на катионы металлов, то такие соли называются кислыми. Названия таких солей образуют, добавляя к названию аниона соответствую-щей средней соли приставку гидро-, по необходимости добавляя числовую приставку:
CoHSO4 - гидросульфат кобальта(II);
Ba(HS)2 - гидросульфид бария;
Ba(HO2)2 - гидропероксид бария;
CrH2P2O7 - дигидродифосфат хрома(II);
Cr(H3P2O7)3 - тригидродифосфат хрома(III);
CrHP2O7 - гидродифосфат хрома(III).
В случаях, когда соль, помимо кислотного остатка содержит гид-роксид-ионы, такие соли называются основными. Их названия по-лучают к названию аниона приставку гидроксо-, также с числовой приставкой по необходимости:
(CuOH)2CO3 - гидроксокарбонат меди;
FeOHNO3 - гидроксонитрат железа(II);
Al(OH)2Сl - дигидроксохлорид алюминия.
Основные соли можно рассматривать как соли и гидроксиды од-новременно, тогда это необходимо отражать и в формуле, и в названии; такие названия строятся с применением числовых приставок. Если в названии аниона уже есть приставка или необходимо избежать двусмысленности, применяют умножающие числовые приставки (бис-, трис-, тетракис-, пентакис-и т.д.):
Cu3CO3(OH)2 - дигидроксид-карбонат тримеди;
Ca5(PO4)3OH - гидроксид-трис-(фосфат) пентакальция;
KAl3(SO4)2(OH)6 - гексагидроксид-бис-(сульфат) триалюминия-калия
Способы получения солей:
1. Взаимодействие простых веществ
2. Взаимодействие оксидов
3. Взаимодействие кислот и оснований (нейтрализация)
4. Взаимодействие соли и кислоты
5. Взаимодействие соли и щелочи
6 Взаимодействие двух солей (обменная реакция)
7 Взаимодействие оксида с кислотой
8 Замещение водорода
9 Замещение металла
10 Термолиз кислых солей
11 Взаимодействие двух солей (присоединение)
12 Взаимодействие двух солей (комплексообразование)
3. Элементы химической термодинамики. Термодинамические системы.
Термодинамические характеристики. Функции состояния системы
Химическая термодинамика изучает изменения энергии в результате процессов в материальных системах, приводящих к изменению состава и свойств физических тел, из которых построена данная система.
Термодинамической системой называется комплекс взаимодействующих между собой физических тел, мысленно обособленный от окружающей среды.
Термодинамические системы бывают трех видов:
1. Изолированные (нет обмена ни веществом, ни энергией с окружающей средой).
2. Замкнутые (нет обмена веществом с окружающей средой).
3. Открытые (есть и энерго- и массообмен с окружающей средой).
Параметры состояния определяют функции состояния, тем или иным образом однозначно характеризующие энергию этого состояния. Однозначность проявляется в том, что функции состояния не зависят от истории системы, т.е. от того, как она попала в данное состояние.
внутренняя энергия является однозначной функцией состояния вещества (или совокупности вещества) и зависит только от параметров состояния, тогда как по отдельности каждая из величин, определяющих внутреннюю энергию (теплота Q, работа W) зависит от пути процесса, переводящего реагенты в продукты.
Другой функцией состояния системы является энтальпия – тепловой эффект реакции при постоянном давлении (dН).
4. Термохимия. Тепловые эффекты химических реакций. Тепловые эффекты в изобарных и изохорных процессах. Термохимические характеристики: внутренняя энергия и энтальпия.
Термохимия – это раздел химической термодинамики изучающий взаимные превращения химической и тепловой энергии. Всякая химическая реакция сопровождается определенным энергетическим эффектом( кол-во энергии, которое должно быть подведено к продуктам реакции или отведено от них, чтобы они имели такую же температуру, как исходные вещества. Если энергия выделяется во внешнюю среду, то такая реакция экзотермическая, а если поглощается, то эндотермическая.
Термохимия изучает тепловые эффекты.
При химической реакции теплота выделяется или поглощается теплота. Реакции, протекающие с выделением теплоты, называются экзотермическими реакциями, а сопровождающиеся поглощением теплоты - эндотермическими.
Количество теплоты, выделяющееся или поглощающееся при химической реакции, называется тепловым эффектом реакции. Эти процессы изучает термохимия. Химические уравнения с тепловыми эффектами реакций называются термохимическими уравнениями.
Тепловой эффект характеризуется знаком - некоторым количеством выделившейся или поглощенной теплоты. Существует две системы определения теплового эффекта: термохимическая, в которой тепловой эффект обозначается буквой Q и принимается за положительный при экзотермических реакциях, и термодинамическая, в которой изменение энергии обозначается символом DН (изменение энтальпии - теплосодержания системы). Выражается тепловой эффект реакции в джоулях. Тепловой эффект дается в расчете на моль вещества, поэтому в термохимических уравнениях допустимы дробные коэффициенты.
Оба способа записи термохимического уравнения химической реакции одинаковы и показывают, что при химическом взаимодействии поглощается или выделяется теплота, что приводит к увеличению или уменьшению теплосодержания системы.
I-ый закон термодинамики: тепло, подведенное к системе идет на совершение системой работы и изменение внутренней энергии.
Q = ΔE + A -запись закона сохранения энергии
Изобарный процесс (Р - const)
Qр = ΔE + A = ΔE + pΔV
(E2 – E1) – (V1 – V2) = (E2 + pV2) – (E1 + pV1) = Н2 – Н1 = ΔH
Q = ΔH
H – энтальпия (теплосодержание системы)
Q = H > 0 Тепловой эффект реакции положителен –
Тепло поглощается – эндотермический процесс
Q = H < 0 Тепловой эффект реакции отрицателен –
Тепло выделяется – экзотермический процесс
Изохорный процесс
Qv = ΔE + A = ΔE + pΔV = ΔE (ΔV = 0, ΔVp = 0)
Q = ΔE
ΔE – внутренний эффект реакции, протекающей при постоянном V.
Тепловой эффект реакции, протекающей при постоянном давлении, больше теплового эффекта реакции при постоянном объеме на величину работы расширения pΔV.
Внутренняя энергия вещества (или системы) — это полная энергия частиц, составляющих данное вещество. Она слагается из кинетической и потенциальной энергий частиц. Внутренняя энергия зависит от состояния вещества.
Внутренняя энергия зависит от природы, массы, от условий в которых находится.
Различие внутренних энергий исходных веществ и продуктов реакций и обусловили тепловые эффекты. При этом в случае изохорных процессов, поглощенная теплота расходится на изменение внутренней энергии системы. Но чаще всего в лабораториях и в промышленности химические процессы проходят не при постоянном объеме, а при постоянном давлении. При изобарных процессах тепловой эффект связан с изменением энтальпии системы.
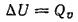
Давление = const
Энтальпия
Это термодинамическая функция состояния системы, отвечающая тепловому эффекту реакции в этой системе при постоянном давлении. Энтальпия связана с внутренней энергией уравнения. Научное и практическое значение имеет не абсолютное значение энтальпии (H) , которое измерить невозможно, а лишь разность
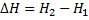
т.е. изменение энтальпии в ходе реакции. Если реакция протекает с выделением теплоты(экзотермическая), то изменение энтальпии системы отрицательно. В противоположном случае(эндотермическая) положительная.
Уравнения реакции содержащие значения дельта Н называют термохимическими уравнениями.
5. Закон Гесса и следствия из него. Стандартная энтальпия образования веществ, единица измерения. Энтальпия химической реакции. Термохимические расчеты.
Закон Гесса утверждает: тепловой эффект реакции не зависит от промежуточных стадий, а определяется лишь начальными и конечными состояниями веществ, если единственной работой является работа расширения, и объем (или давление) в ходе реакции остается неизменным. Таким образом, если возможно проведение реакций несколькими способами, то при совпадении состояний реагентов и продуктов реакции тепловой эффект ее должен быть одним и тем же.
Первое следствие закона Гесса. Энтальпия химической реакции равна сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ. Энтальпия образования вещества это энтальпия реакции образования 1 моль соединения из простых веществ, устойчивых при стандартных условиях. Например. энтальпия образования нитрата натрия равна энтальпии реакцииNa(кр) + ½N2(г) + 3/2О2(г) = NaNO3(кр), 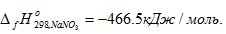 Энтальпия образования простых веществ при стандартных условиях принята равной нулю. Энтальпия является свойством вещества, также как и масса, объем и т.д. Энтальпия _ функция состояния системы, т.е. ее изменение не зависит от пути процесса, а определяется только состоянием системы в конце и начале процесса.
Энтальпия образования простых веществ при стандартных условиях принята равной нулю. Энтальпия является свойством вещества, также как и масса, объем и т.д. Энтальпия _ функция состояния системы, т.е. ее изменение не зависит от пути процесса, а определяется только состоянием системы в конце и начале процесса.
Энтальпия химической реакции в общем виде аА + bB = dD + eE (2.10)
определяется по уравнению 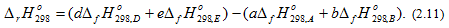
Второе следствие закона Гесса.Энтальпия химической реакции равна сумме энтальпий сгорания исходных веществ за вычетом суммы энтальпий сгорания продуктов реакции.
Энтальпия сгорания вещества В 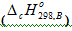 это энтальпия реакции окисления кислородом 1 моль соединения до образования высших оксидов. Например энтальпия реакции сгорания метанола есть изменение энтальпии следующей реакции: СН3ОН + 3/2О2 = СО2 + 2Н2О
это энтальпия реакции окисления кислородом 1 моль соединения до образования высших оксидов. Например энтальпия реакции сгорания метанола есть изменение энтальпии следующей реакции: СН3ОН + 3/2О2 = СО2 + 2Н2О
Энтальпия химической реакции в общем виде (2.10) определяется по уравнению
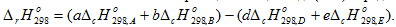
Энтальпия образования (теплота образования), энтальпия реакции образования данного вещества (или раствора) из заданных исходных веществ. Энтальпией образования химических соединения называют энтальпию реакции образования данного соединения из простых веществ. В качестве простых веществ выбирают химические элементы в их естественном фазовом и химическом состоянии при данной температуре.
Энтальпия образования может быть определена при любой температуре. Стандартные энтальпии образования 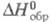 соответствуют реакциям образования, при которых и простые вещества, и получающееся соединение находятся при давлении 1 атм (1,01 x 105 Па). По определению, для всех простых веществ при любой температуре
соответствуют реакциям образования, при которых и простые вещества, и получающееся соединение находятся при давлении 1 атм (1,01 x 105 Па). По определению, для всех простых веществ при любой температуре 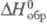 = 0. Для большинства хим. соед. энтальпия образования- отрицат. величины.
= 0. Для большинства хим. соед. энтальпия образования- отрицат. величины.
Единицы измерения энтальпии образования - Дж/г, Дж/моль.
Энтальпия химической реакции ΔH - это тепловой эффект реакции при постоянном давлении
| ΔH = ΔU + pΔV |
Единица энтальпии в СИ джоуль (Дж); в химии и справочных таблицах чаще используется кратная единица - килоджоуль (кДж).
Энтальпия имеет размерность энергии (кДж). Ее величина пропорциональна количеству вещества; энтальпия единицы количества вещества (моль) измеряется в кДж∙моль–1.
В термодинамической системе выделяющуюся теплоту химического процесса условились считать отрицательной (экзотермический процесс, ΔH < 0), а поглощение системой теплоты соответствует эндотермическому процессу, ΔH > 0.
Уравнения химических реакций с указанием энтальпии процесса называют термохимическими. Численные значения энтальпии ΔH указывают через запятую в кДж и относят ко всей реакции с учетом стехиометрических коэффициентов всех реагирующих веществ.
Термохимические расчеты:
Основной принцип, на котором основываются все термохимические расчеты, установлен в 1840 г. русским химиком акад. Г. И. Гессом. Этот принцип, известный под названием закона Гесса и являющийся частным случаем закона сохранения энергии, можно сформулировать так:
Тепловой эффект реакции зависит только от начального и конечного состояния веществ и не зависит от промежуточных стадий процесса.
Рассмотрим пример, поясняющий закон Гесса. Раствор сульфата натрия можно приготовить из растворов серной кислоты и гидроксида натрия двумя способами:
1. Смешать раствор, содержащий два моля  , с раствором, содержащим один моль
, с раствором, содержащим один моль  .
.
2. Смешать раствор, содержащий один моль 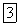 , с раствором, содержащим один моль
, с раствором, содержащим один моль  , и к полученному раствору кислой соли
, и к полученному раствору кислой соли 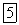 добавить раствор, содержащий еще один моль
добавить раствор, содержащий еще один моль  .
.
Запишем термохимические уравнения этих реакций.
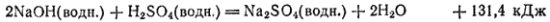
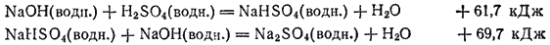
15 Понятие об энтропии. Термодинамическая вероятность состояния системы. Стандартная энтропия вещест,ва, единицы измерения. Изменение энтропии при химических реакциях и фазовых переходах. Расчет ее изменения.
Состояние любой системы может быть охарактеризовано значениями непосредственно измеряемых параметров (р, Т и др.). Это характеристика макросостояния системы. Состояние системы может быть описано также характеристиками каждой частицы системы (атома, молекулы): координаты, частота колебания, частота вращения и т.д. Это характеристика микросостояния системы. Системы состоят из очень большого числа частиц, поэтому одному макросостоянию будет отвечать огромное число различных микросостояний. Это число называется термодинамической вероятностью состояния и обозначается (W).
Термодинамическая вероятность связана с другим свойством вещества – энтропией (S) –формулой Больцмана
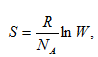 (2.13)
(2.13)
где R - универсальная газовая постоянная, а NA – постоянная Авогадро. Измеряется энтропия в Дж/(моль.К).
Физический смысл: энтропия является мерой неупорядоченности состояния системы. Энтропия системы увеличивается во всех процессах, когда возрастает неупорядоченность (нагревание, растворение, испарение, реакции разложения и т.п.) и уменьшается в процессах, идущих с увеличением упорядоченности (охлаждение, кристаллизация, сжатие и т.п.).
Энтропия является функцией состояния, но в отличие от большинства других термодинамических функций возможно экспериментальное определение абсолютного значения энтропии вещества. Эта возможность основана на постулате М.Планка, согласно которому «при абсолютном нуле энтропия идеального кристалла равна нулю»(третий закон термодинамики).
Температурная зависимость энтропии вещества представлена качественно на рис.2.1.
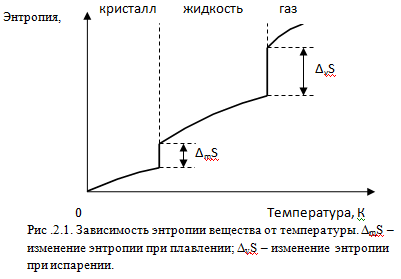
На рис.2.1 видно, что при нуле Кельвина энтропия вещества равна нулю. При повышении температуры энтропия плавно увеличивается, а в точках фазовых переходов имеет место скачкообразное увеличение энтропии, определяемое соотношением
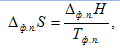 (2.14)
(2.14)
где Δ ф..п.S, Δф.п.Н и Тф.п. изменение энтропии, энтальпии и температура фазового перехода, соответственно.
Энтропию вещества B в стандартном состоянии обозначают 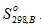 . Для многих веществ абсолютные значения стандартных энтропий определены и приводятся в справочных изданиях.
. Для многих веществ абсолютные значения стандартных энтропий определены и приводятся в справочных изданиях.
Энтропия, также как внутренняя энергия и энтальпия, является функцией состояния, поэтому изменение энтропии системы в процессе не зависит от его пути и определяется только начальным и конечным состоянием системы. Изменение энтропии в ходе химической реакции (2.10) может быть найдено, как разность суммы энтропий продуктов реакции и суммы энтропий исходных веществ
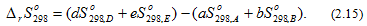
Понятие энтропии используется в одной из формулировок второго закона термодинамики: в изолированных системах могут самопроизвольно протекать только процессы, идущие с увеличением энтропии (ΔS>0). Под изолированными системами понимаются системы, не обменивающиеся с окружающей средой ни веществом, ни энергией. Системы, в которых протекают химические процессы, к изолированным системам не относятся, т.к. они обмениваются с окружающей средой энергией (тепловой эффект реакции).
6. Понятие об энтропии. Термодинамическая вероятность состояния системы. Стандартная энтропия вещества, единицы измерения. Изменение энтропии при химических реакциях и фазовых переходах. Расчет ее изменения. Направление реакции в изолированных системах.
Состояние любой системы может быть охарактеризовано значениями непосредственно измеряемых параметров (р, Т и др.). Это характеристика макросостояния системы. Состояние системы может быть описано также характеристиками каждой частицы системы (атома, молекулы): координаты, частота колебания, частота вращения и т.д. Это характеристика микросостояния системы. Системы состоят из очень большого числа частиц, поэтому одному макросостоянию будет отвечать огромное число различных микросостояний. Это число называется термодинамической вероятностью состояния и обозначается(W).
Термодинамическая вероятность связана с другим свойством вещества – энтропией (S) –формулой Больцмана
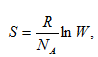 (2.13)
(2.13)
где R - универсальная газовая постоянная, а NA – постоянная Авогадро. Измеряется энтропия в Дж/(моль.К).
Физический смысл: энтропия является мерой неупорядоченности состояния системы. Энтропия системы увеличивается во всех процессах, когда возрастает неупорядоченность (нагревание, растворение, испарение, реакции разложения и т.п.) и уменьшается в процессах, идущих с увеличением упорядоченности (охлаждение, кристаллизация, сжатие и т.п.).
Энтропия является функцией состояния, но в отличие от большинства других термодинамических функций возможно экспериментальное определение абсолютного значения энтропии вещества. Эта возможность основана на постулате М.Планка, согласно которому «при абсолютном нуле энтропия идеального кристалла равна нулю»(третий закон термодинамики).
Температурная зависимость энтропии вещества представлена качественно на рис.2.1.

На рис.2.1 видно, что при нуле Кельвина энтропия вещества равна нулю. При повышении температуры энтропия плавно увеличивается, а в точках фазовых переходов имеет место скачкообразное увеличение энтропии, определяемое соотношением
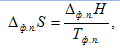 (2.14)
(2.14)
где Δ ф..п.S, Δф.п.Н и Тф.п. изменение энтропии, энтальпии и температура фазового перехода, соответственно.
Энтропию вещества B в стандартном состоянии обозначают 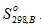 . Для многих веществ абсолютные значения стандартных энтропий определены и приводятся в справочных изданиях.
. Для многих веществ абсолютные значения стандартных энтропий определены и приводятся в справочных изданиях.
Энтропия, также как внутренняя энергия и энтальпия, является функцией состояния, поэтому изменение энтропии системы в процессе не зависит от его пути и определяется только начальным и конечным состоянием системы. Изменение энтропии в ходе химической реакции (2.10) может быть найдено, как разность суммы энтропий продуктов реакции и суммы энтропий исходных веществ
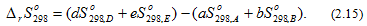
Понятие энтропии используется в одной из формулировок второго закона термодинамики: в изолированных системах могут самопроизвольно протекать только процессы, идущие с увеличением энтропии (ΔS>0). Под изолированными системами понимаются системы, не обменивающиеся с окружающей средой ни веществом, ни энергией. Системы, в которых протекают химические процессы, к изолированным системам не относятся, т.к. они обмениваются с окружающей средой энергией (тепловой эффект реакции).
7. Энергия Гиббса. Энергия Гиббса образования веществ. Направление химических реакций неизолированных системах. Расчет энергии Гиббса. Влияние энтальпийного и энтропийного факторов на изменение энергии Гиббса.
Свободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на вопрос о принципиальной возможности протекания химической реакции; это термодинамический потенциал следующего вида:
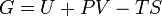
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.)
Понятие энергии Гиббса широко используется в термодинамике и химии.
Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (ΔH), и энтропийным T ΔS, обусловленным увеличением беспорядка в системе вследствие роста её энтропии. Разность этих термодин0амических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж)
Классическим определением энергии Гиббса является выражение
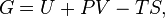
где 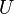 — внутренняя энергия,
— внутренняя энергия, 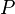 — давление,
— давление, 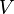 — объём,
— объём, 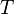 — абсолютная температура,
— абсолютная температура, 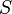 — энтропия.
— энтропия.
Принцип Ле-Шателье
Номенклатура солей.
Средние соли кислородсодержащих кислот
Названия средних солей состоят из традиционных названий ка-тионов и анионов. Если элемент в образуемых им оксоанионах про-являет одну степень окисления, то название аниона оканчивается на -ат:
(NH4)2CO3 - карбонат аммония; K4SiO4 - ортосиликат калия;
NaBiO3 - висмутат натрия; LiBO2 - метаборат лития.
В случае двух степеней окисления ещё используют окончание -ит:
BaSeO4 - селенат бария; FeAsO4 - ортоарсенат железа(III);
BaSeO3 - селенит бария; Fe(AsO2)2 - метаарсенит железа(II).
Если степеней окисления элемента в анионах может быть более двух, то для самой низкой (обычно +1) применяют приставку гипо-с окончанием -ит:
Na2N2O2 - гипонитрит натрия; Ca(H2PO2)2 - гипофосфит кальция.
Последнее вещество является средней солью, поскольку в этом анионе два атома водорода присоединены непосредственно к атому фосфора и не проявляют кислых свойств.
Названия анионов, образованных элементом в степени окисления +7, имеют приставку пер-и окончание -ат:
H3OClO4 - перхлорат оксония; KMnO4 - перманганат калия;
Ag5IO6 - ортопериодат серебра; SrIO4 - метапериодат стронция.
Соли поли- тио- и пероксокислот называются по тем же прави-лам, сохраняя соответствующую приставку от названия кислоты:
Mg2P2O7 - дифосфат магния; Cs3PO2(O2)2 - дипероксофосфат цезия; К2SO3(О2) - пероксосульфат калия; Rb2S2O2 - тиосульфит рубидия.
Кислые и основные соли
Если в состав соли входят атомы водорода, которые при диссо-циации проявляют кислотные свойства и могут быть замещены на катионы металлов, то такие соли называются кислыми. Названия таких солей образуют, добавляя к названию аниона соответствую-щей средней соли приставку гидро-, по необходимости добавляя числовую приставку:
CoHSO4 - гидросульфат кобальта(II);
Ba(HS)2 - гидросульфид бария;
Ba(HO2)2 - гидропероксид бария;
CrH2P2O7 - дигидродифосфат хрома(II);
Cr(H3P2O7)3 - тригидродифосфат хрома(III);
CrHP2O7 - гидродифосфат хрома(III).
В случаях, когда соль, помимо кислотного остатка содержит гид-роксид-ионы, такие соли называются основными. Их названия по-лучают к названию аниона приставку гидроксо-, также с числовой приставкой по необходимости:
(CuOH)2CO3 - гидроксокарбонат меди;
FeOHNO3 - гидроксонитрат железа(II);
Al(OH)2Сl - дигидроксохлорид алюминия.
Основные соли можно рассматривать как соли и гидроксиды од-новременно, тогда это необходимо отражать и в формуле, и в названии; такие названия строятся с применением числовых приставок. Если в названии аниона уже есть приставка или необходимо избежать двусмысленности, применяют умножающие числовые приставки (бис-, трис-, тетракис-, пентакис-и т.д.):
Cu3CO3(OH)2 - дигидроксид-карбонат тримеди;
Ca5(PO4)3OH - гидроксид-трис-(фосфат) пентакальция;
KAl3(SO4)2(OH)6 - гексагидроксид-бис-(сульфат) триалюминия-калия
Способы получения солей:
1. Взаимодействие простых веществ
2. Взаимодействие оксидов
3. Взаимодействие кислот и оснований (нейтрализация)
4. Взаимодействие соли и кислоты
5. Взаимодействие соли и щелочи
6 Взаимодействие двух солей (обменная реакция)
7 Взаимодействие оксида с кислотой
8 Замещение водорода
9 Замещение металла
10 Термолиз кислых солей
11 Взаимодействие двух солей (присоединение)
12 Взаимодействие двух солей (комплексообразование)
3. Элементы химической термодинамики. Термодинамические системы.
Термодинамические характеристики. Функции состояния системы
Химическая термодинамика изучает изменения энергии в результате процессов в материальных системах, приводящих к изменению состава и свойств физических тел, из которых построена данная система.
Термодинамической системой называется комплекс взаимодействующих между собой физических тел, мысленно обособленный от окружающей среды.
Термодинамические системы бывают трех видов:
1. Изолированные (нет обмена ни веществом, ни энергией с окружающей средой).
2. Замкнутые (нет обмена веществом с окружающей средой).
3. Открытые (есть и энерго- и массообмен с окружающей средой).
Параметры состояния определяют функции состояния, тем или иным образом однозначно характеризующие энергию этого состояния. Однозначность проявляется в том, что функции состояния не зависят от истории системы, т.е. от того, как она попала в данное состояние.
внутренняя энергия является однозначной функцией состояния вещества (или совокупности вещества) и зависит только от параметров состояния, тогда как по отдельности каждая из величин, определяющих внутреннюю энергию (теплота Q, работа W) зависит от пути процесса, переводящего реагенты в продукты.
Другой функцией состояния системы является энтальпия – тепловой эффект реакции при постоянном давлении (dН).
4. Термохимия. Тепловые эффекты химических реакций. Тепловые эффекты в изобарных и изохорных процессах. Термохимические характеристики: внутренняя энергия и энтальпия.
Термохимия – это раздел химической термодинамики изучающий взаимные превращения химической и тепловой энергии. Всякая химическая реакция сопровождается определенным энергетическим эффектом( кол-во энергии, которое должно быть подведено к продуктам реакции или отведено от них, чтобы они имели такую же температуру, как исходные вещества. Если энергия выделяется во внешнюю среду, то такая реакция экзотермическая, а если поглощается, то эндотермическая.
Термохимия изучает тепловые эффекты.
При химической реакции теплота выделяется или поглощается теплота. Реакции, протекающие с выделением теплоты, называются экзотермическими реакциями, а сопровождающиеся поглощением теплоты - эндотермическими.
Количество теплоты, выделяющееся или поглощающееся при химической реакции, называется тепловым эффектом реакции. Эти процессы изучает термохимия. Химические уравнения с тепловыми эффектами реакций называются термохимическими уравнениями.
Тепловой эффект характеризуется знаком - некоторым количеством выделившейся или поглощенной теплоты. Существует две системы определения теплового эффекта: термохимическая, в которой тепловой эффект обозначается буквой Q и принимается за положительный при экзотермических реакциях, и термодинамическая, в которой изменение энергии обозначается символом DН (изменение энтальпии - теплосодержания системы). Выражается тепловой эффект реакции в джоулях. Тепловой эффект дается в расчете на моль вещества, поэтому в термохимических уравнениях допустимы дробные коэффициенты.
Оба способа записи термохимического уравнения химической реакции одинаковы и показывают, что при химическом взаимодействии поглощается или выделяется теплота, что приводит к увеличению или уменьшению теплосодержания системы.
I-ый закон термодинамики: тепло, подведенное к системе идет на совершение системой работы и изменение внутренней энергии.
Q = ΔE + A -запись закона сохранения энергии
Изобарный процесс (Р - const)
Qр = ΔE + A = ΔE + pΔV
(E2 – E1) – (V1 – V2) = (E2 + pV2) – (E1 + pV1) = Н2 – Н1 = ΔH
Q = ΔH
H – энтальпия (теплосодержание системы)
Q = H > 0 Тепловой эффект реакции положителен –
Тепло поглощается – эндотермический процесс
Q = H < 0 Тепловой эффект реакции отрицателен –
Тепло выделяется – экзотермический процесс
Изохорный процесс
Qv = ΔE + A = ΔE + pΔV = ΔE (ΔV = 0, ΔVp = 0)
Q = ΔE
ΔE – внутренний эффект реакции, протекающей при постоянном V.
Тепловой эффект реакции, протекающей при постоянном давлении, больше теплового эффекта реакции при постоянном объеме на величину работы расширения pΔV.
Внутренняя энергия вещества (или системы) — это полная энергия частиц, составляющих данное вещество. Она слагается из кинетической и потенциальной энергий частиц. Внутренняя энергия зависит от состояния вещества.
Внутренняя энергия зависит от природы, массы, от условий в которых находится.
Различие внутренних энергий исходных веществ и продуктов реакций и обусловили тепловые эффекты. При этом в случае изохорных процессов, поглощенная теплота расходится на изменение внутренней энергии системы. Но чаще всего в лабораториях и в промышленности химические процессы проходят не при постоянном объеме, а при постоянном давлении. При изобарных процессах тепловой эффект связан с изменением энтальпии системы.
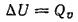
Давление = const
Энтальпия
Это термодинамическая функция состояния системы, отвечающая тепловому эффекту реакции в этой системе при постоянном давлении. Энтальпия связана с внутренней энергией уравнения. Научное и практическое значение имеет не абсолютное значение энтальпии (H) , которое измерить невозможно, а лишь разность
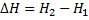
т.е. изменение энтальпии в ходе реакции. Если реакция протекает с выделением теплоты(экзотермическая), то изменение энтальпии системы отрицательно. В противоположном случае(эндотермическая) положительная.
Уравнения реакции содержащие значения дельта Н называют термохимическими уравнениями.
5. Закон Гесса и следствия из него. Стандартная энтальпия образования веществ, единица измерения. Энтальпия химической реакции. Термохимические расчеты.
Закон Гесса утверждает: тепловой эффект реакции не зависит от промежуточных стадий, а определяется лишь начальными и конечными состояниями веществ, если единственной работой является работа расширения, и объем (или давление) в ходе реакции остается неизменным. Таким образом, если возможно проведение реакций несколькими способами, то при совпадении состояний реагентов и продуктов реакции тепловой эффект ее должен быть одним и тем же.
Первое следствие закона Гесса. Энтальпия химической реакции равна сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ. Энтальпия образования вещества это энтальпия реакции образования 1 моль соединения из простых веществ, устойчивых при стандартных условиях. Например. энтальпия образования нитрата натрия равна энтальпии реакцииNa(кр) + ½N2(г) + 3/2О2(г) = NaNO3(кр), 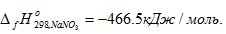 Энтальпия образования простых веществ при стандартных условиях принята равной нулю. Энтальпия является свойством вещества, также как и масса, объем и т.д. Энтальпия _ функция состояния системы, т.е. ее изменение не зависит от пути процесса, а определяется только состоянием системы в конце и начале процесса.
Энтальпия образования простых веществ при стандартных условиях принята равной нулю. Энтальпия является свойством вещества, также как и масса, объем и т.д. Энтальпия _ функция состояния системы, т.е. ее изменение не зависит от пути процесса, а определяется только состоянием системы в конце и начале процесса.
Энтальпия химической реакции в общем виде аА + bB = dD + eE (2.10)
определяется по уравнению 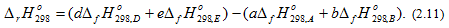
Второе следствие закона Гесса.Энтальпия химической реакции равна сумме энтальпий сгорания исходных веществ за вычетом суммы энтальпий сгорания продуктов реакции.
Энтальпия сгорания вещества В 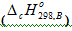 это энтальпия реакции окисления кислородом 1 моль соединения до образования высших оксидов. Например энтальпия реакции сгорания метанола есть изменение энтальпии следующей реакции: СН3ОН + 3/2О2 = СО2 + 2Н2О
это энтальпия реакции окисления кислородом 1 моль соединения до образования высших оксидов. Например энтальпия реакции сгорания метанола есть изменение энтальпии следующей реакции: СН3ОН + 3/2О2 = СО2 + 2Н2О
Энтальпия химической реакции в общем виде (2.10) определяется по уравнению
<
