Комплексообразующая способность d-элементов
Возможность создания химических связей с участием d-электронов и свободных d-орбиталей обуславливает ярко выраженную способность d-элементов к образованию устойчивых комплексных соединений.
При низких степенях окисления для d-элементов более характерны катионные, а при высоких – анионные октаэдрические комплексы ([ScF6]3–, [TiF6]2–, [VF6]–)
КЧ d-элементов непостоянны, это четные числа от 4 до 8, реже 10,12.
Используя незаполненные d-орбитали и неподеленные пары d-электронов на предвнешнем электронном слое, d-элементы способны выступать как донорами электронов – дативная связь, так и акцепторами электронов. Пример соединений с дативной связью: [HgI]Ї, [CdCl4]Ї.
Гидроксокомплексы – комплексные соединения, содержащие в качестве лигандов гидроксид-ионы OH-. Гидроксокомплексы образуются в реакциях протолиза из аквакомплексов:
[Al(H2O)6]3+ + H2O [Al(H2O)5(OH)]2+ + H3O+
либо при растворении амфотерных гидроксидов в водных растворах гидроксидов щелочных металлов:
Zn(OH)2 + 2 OH- = [Zn(OH)4]2-
Fe - ходит в состав гемоглобина, ферментов цитохромов, каталазы, пероксидазы
Co - входит в состав витамина В12
Cr - Биогенный элемент.
Mn - Входит в состав ферментов
Cu - Входит в состав ферментов окигеназ и гидролаз. Участвует в кроветворении.
Zn - Входит в состав ферментов катализирующих гидролиз пептидов, белков, некоторых эфиров и альдегидов
25. К р – блоку относятся 30 элементов IIIA-VIIIA групп периодической системы и входят во второй и третий малые периоды, а также в четвертый – шестой большие периоды. У элементов IIIA группы появляется первый электрон на р – орбитали. В других группах IVA-VIIIA происходит последовательное заполнение р – подуровня до 6 электронов. Строение внешних электронных оболочек атомов элементов р – блока ns2npa , где а = 1÷6.
На свойства р–элементов и их соединений оказывает влияние как появление новых подуровней на внешней электронной оболочке, так и заполнение внутренних электронных оболочек. р – Элементы второго периода (В, С, N, O, F) резко отличаются от элементов нижеследующих периодов, так как, начиная с р–элементов третьего периода, появляется низколежащий свободный d-подуровень, на который могут переходить электроны с р – подуровня при возбуждении атома. Полностью заполненный 3 d-подуровень у р–элементов четвертого периода (Ga, Ge, As, Se, Br) обуславливает отличие их свойств от элементов третьего периода. Максимальное заполнение 4f-подуровня в шестом периоде сказывается на различии свойств р–элементов шестого и пятого периодов.
Вдоль периода у р–элементов падает способность к образованию положительно заряженных ионов с зарядом, отвечающим номеру группы, и наоборот, способность к образованию отрицательных ионов с зарядом, равным (8 – № группы) возрастает.
р – элементы образуют двухатомные молекулы Э2, различающиеся по устойчивости. Наиболее устойчивы молекулы элементов второго периода (N2, O2, F2). При переходе от IIIA к IVA и VA группам устойчивость двухатомных молекул возрастает, а затем при переходе к VIIIА группе понижается. В группах сверху вниз прочность связи Э–Э уменьшается.
Постоянные пломбировочные (реставрационные) материалы предназначены для восстановления анатомической формы, функции и внешнего вида зуба, а также предотвращения развития кариеса. Один из разновидностей таких материалов цементы:
– цинк-фосфатные цементы;
– силикатные цементы;
– силикофосфатные цементы.
Твердокристаллические материалы
К этой группе слепочных материалов относятся гипс, цинкоксиэвгеноловые и цинкоксигваяколовые пасты. Характерной особенностью этих масс является то, что в отвердевшем состоянии они имеют четкое кристаллическое строение, лишены пластичности и упругих свойств.
26. Адсорбция- изменение концентрации вещества на границе раздел фаз. Происходит на любых межфазовых поверхностях и адсорбироваться могут любые вещества. Адсорбционное равновесие, т.е. равновесие распределения вещества между пограничным слоем и граничащими фазами, является динамическим равновесием и быстро устанавливаются. Адсорбция уменьшается с увеличением температуры и покидает поверхность. Поверхностное Натяжение есть величина, численно равная энергии Гиббса, приходящейся на единицу площади поверхностного слоя и численно равная работе, еоторую необходимо совершить для образования единицы поверхности раздела фаз при постоянной температуре. ПН зависит от природы жидкости и температуры(уменьшается с ростом t). Вода имеет самое высокое значение ПН. ПН сыворотки крови составляет 45,4*10-3Н/м.
Пове́рхностные явле́ния — совокупность явлений, обусловленных особыми свойствами тонких слоёв вещества на границе соприкосновения фаз. К поверхностным явлениям относятся процессы, происходящие на границе раздела фаз, в межфазном поверхностном слое и возникающие в результате взаимодействия сопряжённых фаз.
Если сигма вещества больше сигма растворителя, то это ПНВ. Такое вещество равномерно распределяется и мало влияет на поверхностное натяжение. ПНВ: соли, кислоты, углеводы. Для ПНВ g=0 Г=0
Если добавить вещество, у которого сигма < сигма растворителя, то поверхностное натяжение раствора резко уменьшится. Это ПАВ – дифильная молекула(одна часть любить воду, а другая нет) ПАВ: жиры. Для ПАВ g>0 Г >0
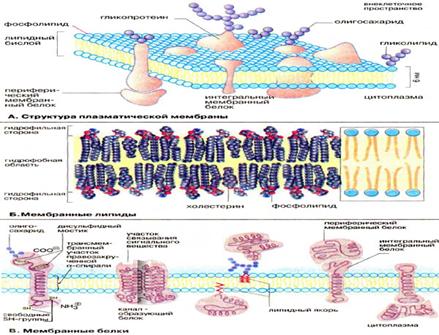
Биомембраны: структура и функции
А. Структура плазматической мембраны
Все биомембраны построены одинаково; они состоят из двух слоев липидных молекул толщиной около 6 нм, в которые встроены белки. Некоторые мембраны содержат, кроме того, углеводы, связанные с липидами и белками. Соотношение липиды : белки : углеводы является характерным для клетки или мембраны и существенно варьирует в зависимости от типа клеток или мембран (см. с. 218).
Компоненты мембран удерживаются нековалентными связями (см. с. 12), вследствие чего они обладают лишь относительной подвижностью, т. е. могут диффундировать в пределах липидного бислоя. Текучесть мембран зависит от липидного состава и температуры окружающей среды. С увеличением содержания ненасыщенных жирных кислот текучесть возрастает, так как наличие двойных связей способствует нарушению полукристаллической мембранной структуры. Подвижными являются и мембранные белки. Если белки не закреплены в мембране, они «плавают» в липидном бислое как в жидкости. Поэтому говорят, что биомембраны имеют жидкостно-мозаичную структуру.
В то время как «дрейф» в плоскости мембраны происходит достаточно легко, переход белков с внешней стороны мембраны на внутреннюю («флип-флоп») невозможен, а переход липидов происходит крайне редко. Для «перескока» липидов необходимы специальные белки транслокаторы. Исключение составляет холестерин, который может легко переходить с одной стороны мембраны на другую.
Б. Мембранные липиды
На рисунке схематически изображена биомембрана. В мембранах содержатся липиды трех классов: фосфолипиды, холестерин и гликолипиды. Наиболее важная группа, фосфолипиды, включает фосфатидилхолин (лецитин), фосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозит и сфингомиелин (см. с. 56). Холестерин присутствует во внутриклеточных мембранах животных клеток (за исключением внутренней мембраны митохондрий). Гликолипиды входят в состав многих мембран (например, во внешний слой плазматических мембран). В состав гликолипидов входят углеводные функциональные группы (см. с. 92), которые ориентируются в водную фазу.
Липиды мембран представляют собой амфифильные молекулы с полярной гидрофильной головкой (голубого цвета) и неполярным липофильным хвостом (желтого цвета). В водной среде они агрегируют за счет гидрофобных взаимодействий и вандерваальсовых сил (см. сс. 12, 34).
В. Мембранные белки
Протеины могут связываться с мембраной различным путем.
Интегральные мембранные белки имеют трансмембранные спирализованные участки (домены), которые однократно или многократно пересекают липидный бислой. Такие белки прочно связаны с липидным окружением.
Периферические мембранные белки удерживаются на мембране с помощью липидного «якоря» (см. с. 230) и связаны с другими компонентами мембраны; например, они часто бывают ассоциированы с интегральными мембранными белками.
У интегральных мембранных белков фрагмент пептидной цепи, пересекающий липидный бислой, обычно состоит из 21-25 преимущественно гидрофобных аминокислот, которые образуют правую α-спираль с 6 или 7 витками (трансмембранная спираль).
Дисперсные системы - гетерогенные системы из двух или большего числа фаз с сильно развитой поверхностью раздела между ними. Обычно одна из фаз образует непрерывную дисперсионную среду, в объеме которой распределена дисперсная фаза (или несколько дисперсных фаз) в виде мелких кристаллов, твердых аморфных частиц, капель или пузырьков.
