Ксенобиотики - чужеродные для организмов химические вещества, естественно не входящие в биотический круговорот и прямо или косвенно порожденные хозяйственной деятельностью человека.
23. Химия элементов s блока. К s-элементам относятся две группы Периодической системы: IА и IIА. В группу IА входят 8 элементов: литий, калий, натрий, рубидий, цезий, франций, водород, гелий. В группу IIА входят 6 элементов: бериллий, магний, кальций, стронций, барий, радий Общая характеристика элементов IА и IIА. Элементные вещества - типичные металлы, обладающие блеском, высокой электрической проводимостью и теплоповодимостью, химически весьма активны.s-элементы IА и IIА имеют относительно большие радиусы атомов и ионов. s-элементы IА и IIА групп легко отдают валентные электроны. Являются сильными восстановителями. С ростом радиуса атома в группах IА и IIА ослабевает связь валентных электронов с ядром, следовательно s-элементы этих групп имеют низкие значения Еи и Еср..сильных восстановителей. Восстановительные свойства возрастают закономерно с увеличением радиуса атома. Восстановительная способность увеличивается по группе сверху вниз. Для элементов IIА группы характерна большая, чем для элементов IА группы способность к комплексообразованию. s-элементы IА и IIА образуют соединения с ионным типом связи. Исключение составляет водород, для которого в соединениях даже с самыми электроотрицательными элементами характерна преимущественно ковалентная связь (например, фтороводород или вода.Сравнение свойств элементов IА и IIА (комплексообразование, образование осадков) на примере Na, K и Mg, Ca Атомы элементов IА группы имеют по одному валентному электрону на s подуровне внешнего энергетического уровня. Это обуславливает проявление степени окисления +1 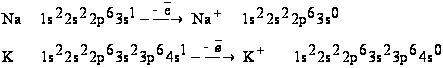 Химическая активность металлов IА группы возрастает закономерно с увеличением радиуса атома и уменьшением их способности к гидратированию (чем меньше способность к гидратированию, тем активнее металл). Так как радиус атома калия больше, чем радиус атома натрия, то способность к гидратации для катиона калия будет ниже, чем для катиона натрия, а, следовательно, химическая активность катиона калия выше, чем у катиона натрия. Вследствие незначительного поляризующего действия (устойчивая электронная структура, большие размеры, малый заряд ядра) комплексообразование для ионов щелочных металлов малохарактерно. Вместе с тем, они способны образовывать комплексные соединения с некоторыми биолигандами (КЧ для натрия и калия может принимать значения 4 и 6). Способность образовывать донорно-акцепторные связи с соответствующими лигандами едва намечается у натрия. У калия имеется значительная тенденция к использованию имеющихся в атоме вакантных d-орбиталей. Большинство солей щелочных металлов хорошо растворимы в воде (исключение составляют некоторые соли лития). Степени окисления больше +2 элементы IIА группы не проявляют. Несмотря на то, что число валентных s электронов у атомов IIА группы одинаково, свойства магния и кальция отличаются друг от друга. Это связанно с тем, что в атоме кальция, в отличие от атома магния, имеются свободные d-орбитали, близкие по энергии к ns орбиталям. Ионы натрия играют важную роль в обеспечении постоянства внутренней среды человеческого организма, участвуют в поддержании постоянного осмотического давления биожидкости (осмотического гомеостаза) Ионы натрия участвуют в регуляции водного обмена и влияют на работу ферментов.. Ионы калия играют важную роль в физиологических процессах - сокращении мышц, нормальном функционировании сердца, проведении нервных импульсов, обменных реакциях. Являются важными активаторами внутриклеточных ферментов. Формально магний относится к макроэлементам. В наибольшей степени магний концентрируется в дентине и эмали зубов, костной ткани. Накапливается в поджелудочной железе,скелетных мышцах. Ионы кальция принимают активное участие в передаче нервных импульсов, сокращении мышц, регулировании работы сердечной мышцы, механизмах свертывания крови. Химическое сходство и биологический антагонизм натрия, калия, кальция и магния.Сходство электронного строения ионов щелочных (натрий и калий) и щелочноземельных (магний и кальций) металлов и различия физико-химических характеристик определяет их действия на биологические процессы.Натрий и калий являются антагонистами. В ряде случаев близость многих физико-химических свойств обусловливает их взаимозамещение в живых организмах. Например, при увеличении количества натрия в организме усиливается выведение калия почками, наступает гипокалиемия.Магний и кальций являются антагонистами. Ионы кальция подавляют активность многих ферментов, активизируемых ионами магния. Антагонизм ионов кальция и магния проявляется еще и в том, что ион кальция является внеклеточным ионом. При длительном поступлении в организм избыточных количеств солей магния наблюдается усиленное выделение кальция из костной ткани.
Химическая активность металлов IА группы возрастает закономерно с увеличением радиуса атома и уменьшением их способности к гидратированию (чем меньше способность к гидратированию, тем активнее металл). Так как радиус атома калия больше, чем радиус атома натрия, то способность к гидратации для катиона калия будет ниже, чем для катиона натрия, а, следовательно, химическая активность катиона калия выше, чем у катиона натрия. Вследствие незначительного поляризующего действия (устойчивая электронная структура, большие размеры, малый заряд ядра) комплексообразование для ионов щелочных металлов малохарактерно. Вместе с тем, они способны образовывать комплексные соединения с некоторыми биолигандами (КЧ для натрия и калия может принимать значения 4 и 6). Способность образовывать донорно-акцепторные связи с соответствующими лигандами едва намечается у натрия. У калия имеется значительная тенденция к использованию имеющихся в атоме вакантных d-орбиталей. Большинство солей щелочных металлов хорошо растворимы в воде (исключение составляют некоторые соли лития). Степени окисления больше +2 элементы IIА группы не проявляют. Несмотря на то, что число валентных s электронов у атомов IIА группы одинаково, свойства магния и кальция отличаются друг от друга. Это связанно с тем, что в атоме кальция, в отличие от атома магния, имеются свободные d-орбитали, близкие по энергии к ns орбиталям. Ионы натрия играют важную роль в обеспечении постоянства внутренней среды человеческого организма, участвуют в поддержании постоянного осмотического давления биожидкости (осмотического гомеостаза) Ионы натрия участвуют в регуляции водного обмена и влияют на работу ферментов.. Ионы калия играют важную роль в физиологических процессах - сокращении мышц, нормальном функционировании сердца, проведении нервных импульсов, обменных реакциях. Являются важными активаторами внутриклеточных ферментов. Формально магний относится к макроэлементам. В наибольшей степени магний концентрируется в дентине и эмали зубов, костной ткани. Накапливается в поджелудочной железе,скелетных мышцах. Ионы кальция принимают активное участие в передаче нервных импульсов, сокращении мышц, регулировании работы сердечной мышцы, механизмах свертывания крови. Химическое сходство и биологический антагонизм натрия, калия, кальция и магния.Сходство электронного строения ионов щелочных (натрий и калий) и щелочноземельных (магний и кальций) металлов и различия физико-химических характеристик определяет их действия на биологические процессы.Натрий и калий являются антагонистами. В ряде случаев близость многих физико-химических свойств обусловливает их взаимозамещение в живых организмах. Например, при увеличении количества натрия в организме усиливается выведение калия почками, наступает гипокалиемия.Магний и кальций являются антагонистами. Ионы кальция подавляют активность многих ферментов, активизируемых ионами магния. Антагонизм ионов кальция и магния проявляется еще и в том, что ион кальция является внеклеточным ионом. При длительном поступлении в организм избыточных количеств солей магния наблюдается усиленное выделение кальция из костной ткани.
