Кинетика изучает скорость химической реакции, ее зависимость от различных факторов и механизмы реакций.
Основные понятия:
· Ограниченность термодинамического подхода(в термодинамике не определяется быстрота)
· Гомогенность и гетерогенность реакции
· Определяется по агрегатному состоянию реагентов в (одной фазе и в разных фазах)
Скорость реакции- изменение концентрации вещества в единицу времени. Ʊ=∆с/∆t.
Истинная скорость - положительна. Ʊист=dс/dt
Химическое равновесие-когда скорости прямой и обратной реакций сравниваются. Классификация реакций:
1)по механизму:
· простые- осуществляется посредством однотипных элементарных актов
· сложные- разнотипные элементарные акты
2) по агрегатному состоянию:
· гомогенные-все исходные вещ-ва в одной фазе, реакция идет по всему объему смеси
· гетерогенные - исх. вещ-ва в разных фазах, важна площадь соприкосновения реагирующих вещ-в.
Молекулярность реакции- число молекул, учавствующих в простой реакции.
Кинетические уравнения:
· первого порядка, V=kc (k-константа скорости реакции)
· второго порядка, V=kc2
Порядок реакции- сумма показателей степеней концентраций реагирующих вещ-в. Период полупревращений- промежуток времени, в течении которого начальное кол-во реагента или его концентрация уменьшаются в 2 раза. T1/2=ln2/k
Зависимость скорости химической реакции от концентрации реагентов. Кинетические уравнения реакция первого, второго и нулевого порядков.
Скорость гомогенной хим. реакции определяется изменением концентрации реагирующих веществ (или продуктов реакции) в единицу времени.
Скорость прямой реакции уменьшается по мере расходования исходных веществ, а скорость обратной реакции увеличивается по мере накопления продуктов реакции. Когда скорости прямой и обратной реакции сравняются, система перейдет в состояние химического равновесия.
Истинная скорость в любой момент времени является только положительной величиной и определяется первой производной концентрации по времени 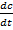 . Если измерение истинной скорости проводят по изменению концентрации исходных веществ, то перед производной ставят знак минус:
. Если измерение истинной скорости проводят по изменению концентрации исходных веществ, то перед производной ставят знак минус:
V= - 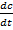
Средняя скорость : Vср = 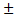
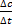
Зависимость скорости хим.реакции от концентрации описывается кинетическим уравнением.
Порядок реакции показывает, каким образом скорость реакции зависит от концентрации реагентов. Порядок кинетического уравнения может принимать значения 0,1,2 и 3; он может быть также дробным.
Уравнения нулевого порядка:
С0 – с1= kt ;
C0-0.5 C0=kt0.5 ;
T0.5= 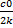 ;
;
Где с0 – начальная концентрация реагента;
с1 – концентрация реагента в момент времени t;
k – константа скорости реакции;
T0.5 – период полураспада.
Уравнения первого порядка:
ln= 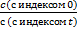 = - kt ;
= - kt ;
T0.5= 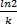 =
= 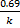 ;
;
Где ct=0.5 c0
Уравнения второго порядка:
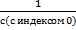 -
- 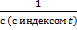 = kt;
= kt;
T0.5= 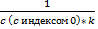 ;
;
Закон действующий масс(Закон Гульберта и Вааге): скорость химической реакции пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов. Т.е. чем больше концентрация, тем больше скорость хим.реакции.
