Детектор электронного захвата
В основе функционирования детектора электронного захвата лежит то положение, что молекулы многих веществ способны реагировать со свободными электронами с образованием стабильных отрицательных молекулярных ионов.
Принципиальная схема детектора электронного захвата:
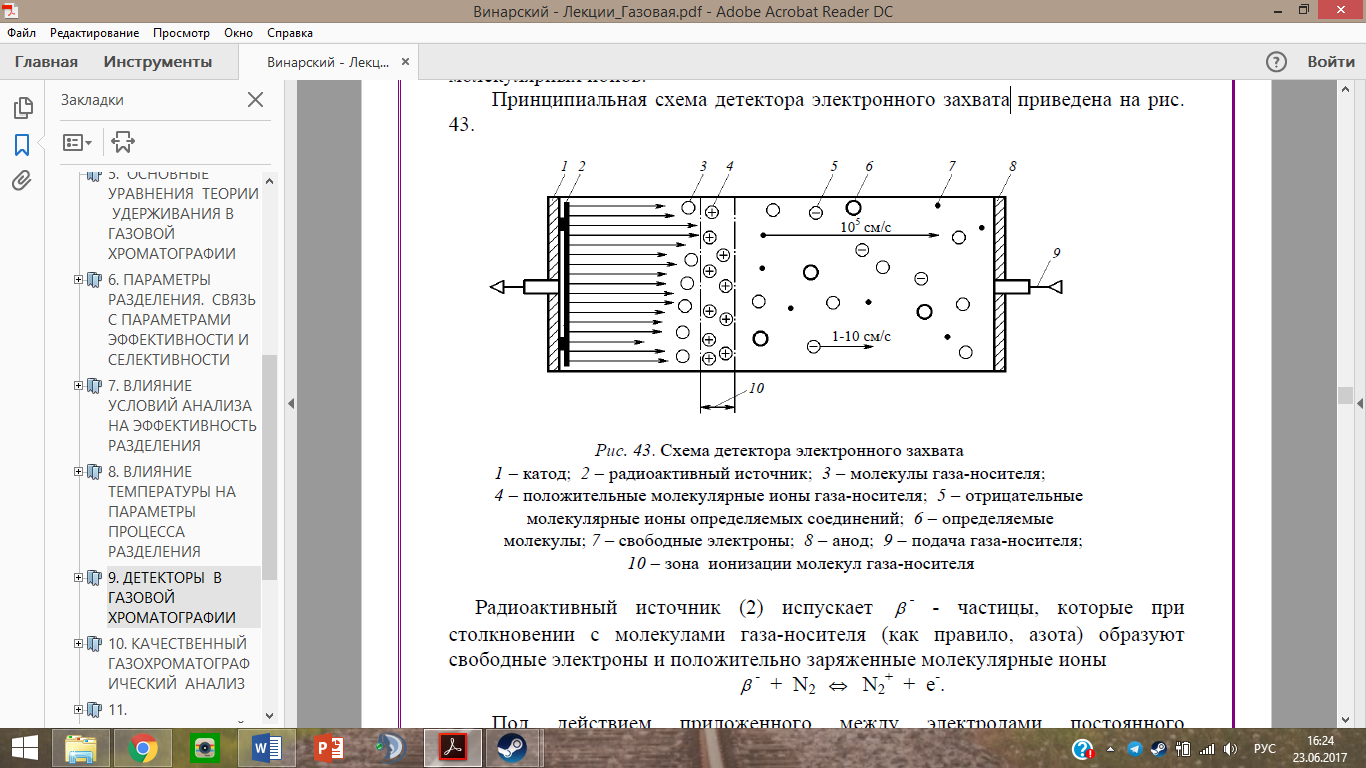
Под действием приложенного между электродами постоянного напряжения образовавшиеся в зоне ионизации свободные электроны движутся к аноду с очень высокой скоростью (порядка 105 см/c), несмотря на встречное движение потока газа-носителя. При этом в системе возникает электрический ток, который усиливается и регистрируется измерителем малых токов.
При практическом использовании детектора электронного захвата необходимо учитывать следующие его особенности:
• температура детектора должна быть несколько выше температуры термостата колонок с целью устранения конденсации пробы и неподвижной фазы в детекторе;
• для сильно захватывающих электроны веществ, следует использовать лишь небольшие количества проб. Большие по количеству пробы насыщают детектор в течение нескольких часов;
• многие органические растворители(кетоны, спирты, хлорсодержащие соединения) способны захватывать электроны. Введение большого количества таких растворителей приводит к быстрому насыщению детектора.
Детектор электронного захвата – потоковый детектор.
Детектор электронного захвата применяют для анализа:
• токсичных соединений в воздухе;
• остаточных количеств пестицидов, гербицидов, инсектицидов и некоторых других соединений, вредных для человека, в крови, в пищевых продуктах,
спиртных напитках, в биологии для анализа аминов, токсичных соединений, гормонов, канцерогенных веществ и метаболитов;
• для анализа летучих галогенсодержащих соединений в различных пробах;
• для анализа некоторых металлоорганических и неорганических соединений.
Основные недостатки детектора электронного захвата:
• чувствительность к изменению температуры;
• сравнительно невысокий верхний температурный предел использования;
• малая линейная область детектирования;
• возможность протекания следующих побочных процессов:
• возникновение пространственного заряда;
• возникновение контактных потенциалов;
• изменение энергии электронов в процессе детектирования, приводящих к искажению результатов анализа.
74. Капиллярная газовая хроматография. Устройство основных узлов газового хроматографа. Принципиальная схема. Капиллярный испаритель для введения образца с делением и без деления потока.
Хроматография – это метод разделения и определения веществ, основанный на распределении компонентов между двумя фазами – подвижной и неподвижной. Неподвижной (стационарной) фазой служит твердое пористое вещество (часто его называют сорбентом) или пленка жидкости, нанесенная на твердое вещество. Подвижная фаза представляет собой жидкость или газ, протекающий через неподвижную фазу, иногда под давлением.
Время удерживания tR - время от момента ввода анализируемой пробы до момента регистрации максимума хроматографического пика.По времени удерживания проводится идентификация разделяемых веществ.Время удерживания складывается из двух составляющих – времени пребывания веществ в подвижной фазе (tm) и времени пребывания в неподвижной фазе (ts).
Степень размывания хроматографического пика определяет эффективность колонки. Чем эффективнее колонка, тем уже пик, тем большее число компонентов можно разделить за более короткое время, т.е. время анализа сокращается. Количественно эффективность колонки может быть выражена числом теоретических тарелок N
Сопоставление площадей или высот хроматографических пиков позволяет оценить количественный состав смеси. В хроматографии используют три основных метода количественного анализа.
Метод абсолютной калибровки обычно предполагает построение градуировочного графика по стандартным смесям, как и в других физических методах.
В методе внутренней нормализации предполагается, что пики всех возможных компонентов смеси зафиксированы на хроматограмме, и сумма их площадей (S) равна 100%.
Метод внутреннего стандарта предусматривает введение в анализируемый образец известного количества эталонного соединения, хроматографирование полученной смеси.
Капиллярная хроматография – это вид хроматографии, в котором для разделения соединений используют капиллярные колонки. Сорбент (неподвижная фаза, жидкая пленка) в таких колонках расположен только на внутренних стенках капилляра, а центральная часть по сечению остается незаполненной (полые или открытые колонки). Движение газа - носителя (подвижная фаза) в колонках без наполнителя сопровождается значительно меньшими энергетическими потерями, чем в заполненных пористым материалом трубках, что повышает эффективность разделения веществ
Для приготовления капиллярных колонок используют стеклянные, кварцевые или металлические трубки, которые должны удовлетворять следующим требованиям:
– капилляр должен иметь нужную длину и постоянный диаметр по всей длине, причем эти параметры не должны изменяться под действием температуры и давления;
– внутренняя поверхность капилляра должна быть химически однородной, на ней не должно быть больших трещин и пор;
– поверхность должна адсорбировать сорбаты, жидкие неподвижные фазы и газ-носитель в минимальной степени;
– поверхность должна прочно и равномерно смачиваться неподвижной фазой, т.е. на поверхности должен быть гомогенный разделяющий слой неподвижной фазы;
– капилляры должны обладать необходимой механической прочностью.
Длина колонки 10-100 м
Внутренний диаметр 0,25-0,35 мм
Среднее число теоретических тарелок 150 000
Толщина пленки 0,005-0,5
Приготовление колонки состоит из ряда этапов:
изготовления капилляра;
подготовки внутренней поверхности капилляра – травлением или дезактивацией;
нанесения неподвижной фазы;
кондиционирования и испытания капиллярной колонки.
По сравнению с другими видами хроматографии К.х. позволяет:
а) увеличить удельную и общую эффективность разделения, а также скорость изменения температуры при ее программировании;
б) упростить сочетание газовой хроматографии с масс-спектрометрией;
в) снизить температуру хроматографической колонки и анализировать термически нестойкие соединения;
г) уменьшить расход подвижной фазы
д) (малые объемы вводимых проб для капиллярных калонок)
Существует несколько типов капиллярных колонок:
1. Капиллярные колонки с пленкой жидкой неподвижной фазой (WCOT) тонкая пленка неподвижной фазы нанесена непосредственно на внутреннюю поверхность колонки толщина пленки 0,01-1 мкм
2. Капиллярные колонки с пористым слоем, пропитанным жидкой фазой, (PLOT) на внутренних стенках расположен слой носителя, несущего неподвижную фазу толщина пленки 1 - 5 мкм
3. Капиллярные колонки с твердым носителем (SCOT) на внутренних стенках напылен слой твердого носителя толщина пленки 10 мкм
4. Капиллярные колонки с химически привитой неподвижной фазой
Особенности капиллярной хроматографии предъявляют весьма жесткие требования к детекторам. Они должны обладать высокой чувствительностью и скоростью регистрации сигнала и иметь небольшой объем измерительной камеры. В наибольшей степени удовлетворяет всем требованиям пламенно-ионизационный детектор.
Применение
Капиллярная хроматография позволяет решать целый ряд сложных аналитических задач, в том числе различать вещества, отличающиеся на 2-3 единицы молекулярной массы, проводить анализ биологических жидкостей на содержание стероидных гормонов, определять состав душистых веществ, контролировать содержание ароматических углеводородов в объектах окружающей среды.
Устройство основных узлов газового хроматографа
| газ - носитель |
| колонка |
| хроматограмма |
| устройство для ввода пробы |
| детектор |
| термостат |
| устройство регулировки давления |
| система управления прибором и обработки данных |
Капиллярный испаритель для введения образца с делением и без деления потока.
(Испарители предназначены для ввода жидких или газообразных проб с помощью шприца)
Введение с делением потока обычно применяется для анализа основных, концентрированных компонентов (при высоких концентрациях веществ в образце, и когда образцы не удаётся разбавить).
Введение без деления потока – для анализа микропримесей.
При работе в режиме с делением потока жидкий образец вводят в нагретый испаритель для введения образца 555555555555555555555555555555555555555555555555555555555555555555555555555555555555555555555555, где он быстро испаряется. При этом небольшая часть образованного пара поступает в колонку, а большая часть выходит наружу через канал сброса. Отношение протока через колонку к потоку на сброс (коэффициент деления потока) задается заранее.
При работе в режиме без деления потока клапан, управляющий сбросом, закрывается на время введения образца. Клапан остается закрытым, пока образец не будет перенесен в колонку. После завершения ввода образца клапан, управляющий сбросом, снова открывается, что дает возможность удалить из испарителя труднолетучие компоненты и подготовить его к следующему вводу пробы.
75. Капиллярная газовая хроматография. Капиллярные колонки и их характеристика. Термостат. Установка капиллярных колонок в термостат
Капиллярные колонки
Снаружи капиллярные колонки из плавленого кварца покрыты защитным полиимидным слоем, который предохраняет колонку от механических повреждений.
Различают 3 типа колонок: WCOT,SCOT, PLOT
· WCOT – неподвижная фаза представляет собой полимер (органополисилоксан или полиэтиленгликоль), нанесенный на внутреннюю поверхность капилляра.Эти колонки универсальны и наиболее часто применяются в газохроматографическом анализе.
· PLOT – содержат на внутренней поверхности капилляра тонкий слой пористого адсорбента (оксид алюминия, углеродистый материал).Колонки PLOT идеально подходят для разделения соединений, которые при комнатной температуре газообразны, для разделения реактивных газов и легколетучих полярных газов, благородных газов, легких углеводородов.
· SCOT– пористая поверхность внутренних стенок
(более подробно о колонках в 74 билете)
Термостат газового хроматографа предназначен для программированного нагревания помещенных в него колонок.Задание постоянной температуры термостата позволяет проводить хроматографический анализ в изотермическом режиме, а программирование термостата позволяет повышать температуру в процессе анализа согласно заданной температурной программе.
Программирование температуры может быть как односегментным, так и многосегментным.
При односегментном программировании температуры задаются температуры и длительности начального и конечного изотермических участков, а также скорость увеличения температуры между ними.
Многосегментное изменение температуры программируют аналогичным образом. Программируется изменение температуры от исходной до конечной, но с различными скоростями, временами выдержки и промежуточными температурами. При программировании предусмотрена возможность не только повышения, но и понижения температуры.
76. Капиллярная газовая хроматография. Типы полисилоксановых покрытий капиллярных колонок. Взаимодействие анализируемых веществ и неподвижной фазы. Характеристики селективности неподвижной фазы по Мак-Рейнольдсу.
1)Самыми распространенными НФ, используемыми для получения WCOT- колонок, являются диметилсиликоновые, фенилметилсиликоновые, смешанные фенилметилполисиликоновые цианопропилметилсиликоновые, цианопропилфенилсиликоновые, трифторпропилметилсиликоновые фазы, а также полиэтиленгликоли (карбовакс). Большинство высокоэффективных разделений в газовой хроматографии проводится с использованием этих фаз.
2)Взаимодействие анализируемого вещества и неподвижной фазы (НФ) представляет собой сумму неполярных дисперсионных и специфических полярных взаимодействий. К последним относятся диполь-дипольные взаимодействия и водородные связи.Поэтому, на основе преобладающего типа взаимодействий, предоставляемых аналиту НФ, фазы обычно подразделяют на два класса — полярные и неполярные.
3)Система для характеристики селективности НФ была предложена Мак-Рейнольдсом. Согласно этой системе, селективность оценивается как разность индексов удерживания Ковача для пяти выбранных стандартных соединений (бензол, н-бутанол, пентанон-2, нитропропан и пиридин), определенных на колонке с исследуемой НФ, и индексов удерживания Ковача, определенных на колонке со скваланом (неполярный высококипящий углеводород).
77. Капиллярная газовая хроматография. Характеристика детекторов. Пламенно-ионизационный детектор (ПИД или ДИП.). Детектор по теплопроводности (катарометр).
Детекторы предназначены для непрерывного измерения концентрации веществ на выходе из хроматографической колонки. Принцип действия детектора должен быть основан на измерении такого свойства аналитического компонента, которым не обладает подвижная фаза.
Детекторы бывают интегральные и дифференциальные
· Интегральные – регистрируют изменение во времени суммарного количества всех компонентов
· Дифференциальные – измеряют мгновенную концентрацию компонентов
1. Концентрационный детектор
2. Потоковый детектор
Пламенно – ионизационный детектор:
ДИП является детектором потокового типа, то есть его сигнал пропорционален общей массе аналита и не зависит от выбранной скорости потока газа носителя через колонку
Газ-носитель (пф) из колонки приносит компоненты образца в пламенно – ионизационный детектор. Эти компоненты попадают в пламя, получаемое при сжигании водорода с воздухом. При сгорании органических соединений в пламени образуются СНО* - радикалы.При их взаимодействии с молекулами воды в пламени генерируются положительно заряженные ионы (преимущественно, Н3О+).Эти ионы под действием постоянного напряжения движутся к коллектору, расположенному над горелкой детектора. При отсутствии компонентов образца число образуемых в пламени ионов мало. При сжигании органических веществ количество ионов увеличивается. Ток регистрируется электрометром, сигнал преобразуется в цифровой вид и направляется в систему управления прибором и обработки данных.
CnHm + O → n CHO+ + e-
CHO+ + nH2O → (H2O)nH+ + CO
