Непредельные одноосновные кислоты
Номенклатура
В молекулах непредельных кислот в радикале, связанном с карбоксильной группой, имеются кратные связи. Ненасыщенные кислоты с одной двойной связью в молекуле имеют общую формулу CnH2n-1COOH.
Простейшей из них является акриловая кислота – CH2= CH-COOH.
Способы получения
1. Из замещенных кислот путем образования в радикале двойной связи:
а) дегидрогалогенированием галогенозамещенных кислот:
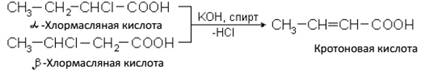
б) дегидратацией оксикислот:
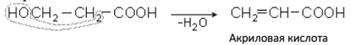
Особенно легко протекают реакции для соединений, содержащих отщепляемые группы в β-положении (Cl,OH и др.).
2. Из галогенсодержащих непредельных соединений синтезом через нитрилы:
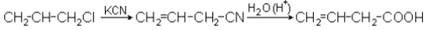
§ 75. Отдельные представители (акриловая кислота, метакриловая кислота)
Акриловая (пропеновая) кислота представляет собой жидкость с резким запахом, tкип = 140 ºС, tпл. = + 13 ºС, = 1,06 г/cм3. С водой смешивается во всех отношениях.
В промышленности ее получают гидролизом акрилонитрила:
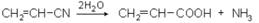
или из ацетилена реакцией карбонирования (реакция Peппе):
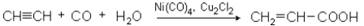
Сама кислота и ее производные (акрилонитрил, эфиры) легко полимеризуются и служат сырьем для получения разнообразных высокомолекулярных соединений.
Широко используется в промышленности метиловый эфир акриловой кислоты метилометакрилат, который легко полимеризуется с образованием прозрачных продуктов. Получают метилметакрилат из акрилонитрила и метилового спирта в присутствии серной кислоты:
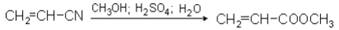
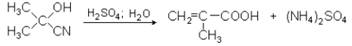
Метакриловая кислота – жидкость tкип.= 160 ºС, tпл. = + 15 ºС, = 1,05 г/cм3. В промышленности получают из ацетона и синильной кислоты:
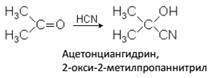
Ацетонциангидрин при нагревании с серной кислотой подвергается дегидратации и омылению с образованием метакриловой кислоты:
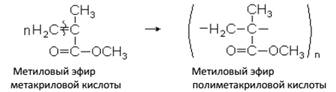
Этот эфир как и другие акрилаты при полимеризации образует стекловидные полимеры (органические стекла) с ценными техническими свойствами – плексиглас.
Плексиглас широко применяется в медицинском приборостроении.
ДВУХОСНОВНЫЕ ПРЕДЕЛЬНЫЕ КИСЛОТЫ
Двухосновными или дикарбоновыми кислотами называются производные углеводородов, которые можно рассматривать как продукт замещения двух атомов водорода двумя карбоксилами.
Общая формула двухосновых кислот:
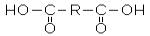
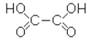
Простейшей двухосновной кислотой является соединение, состоящее из двух карбоксильных групп – щавелевая кислота:
Номенклатура
Как и в случае одноосновных кислот, для обозначения многих двухосновных кислот часто пользуются эмпирическими названиями.
Так, простейшая двухосновная кислота называется щавелевой кислотой, потому что впервые была найдена в щавеле.
Следующий представитель – с тремя углеродными атомами – называется молоноваякислота.
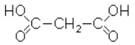
С четырьмя атомами углерода называется янтарная кислота, впервые была получена из янтаря.
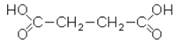
Иногда названия двухосновных кислот производят от названий углеводородов, радикалы которых содержатся в этих кислотах, прибавляя слова «дикарбоновая кислота». Так молоновую кислоту называют метандикарбоновой кислотой, янтарную – этандикарбоновой кислотой и. т. д.
По международной номенклатуре названия двухосновных кислот производят от названий углеводородов с тем же общим числом атомов углерода. Так щавелевая кислота называется этандиановая кислота, молоновая – пропандиновая кислота и янтарная – бутандионовая кислота.
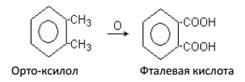
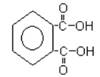
Важнейший представитель двухосновных ароматических кислот – О-фенилендикарбоновая кислота, называемая фталевой кислотой.
Способы получения
Общие методы получения двухосновных кислот аналогичны способам получения одноосновных кислот, например:
1. Окисление двупервичных гликолей:
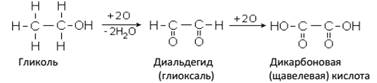
2. Гидролиз (омыление) динитрилов:
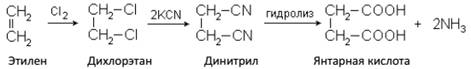
Двухосновные ароматические кислоты можно легко получить окислением ароматических углеводородов, имеющих боковые цепи: