Расчет равновесного состава газовой смеси
При протекании гомогенной обратимой реакции в газовой фазе после установления химического равновесия в системе будут присутствовать как продукты реакции, так и исходные вещества. Зная уравнение химической реакции, величину константы равновесия и начальные концентрации реагентов, можно рассчитать равновесные концентрации всех веществ. Их величины будут зависеть от температуры и давления.
Необходимо отметить, что в достаточно широкой области давлений и температур газовые смеси можно считать идеальными и проводить расчеты равновесного состава газовой смеси, считая коэффициент фугитивности gi @ 1.
Реакции в газовой фазе протекают в относительно широком интервале температур и давлений. Константы равновесия для каждой конкретной реакции, как правило, рассчитываются с использованием табличных значений термодинамических функций реагирующих веществ для определенных температури давлений.
Пусть протекает обратимая газовая реакция nAA + nBB ÛnDD + nEE. С использованием термодинамических характеристик реакции (DrG0(T),DrH0(T),DrS0(T)) рассчитывается стандартная константа равновесия К0(Т) для определенной температуры Т:
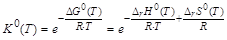 .
.
Из стандартной константы равновесия К0(Т) рассчитывают константы равновесия КX(Т, p) и Кр(Т). Отметим, что величина КX(Т, p) зависит от давления, а Кр(Т) не зависит:
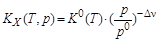 ,
, 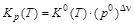 ,
,
где р0 = 1,013×105 Па – стандартное давление; Dn= (nD + nE)–(nA + nB) –изменение числа молей в ходе реакции.
Расчет равновесного состава продуктов реакции для изобарного процесса проводят с использованием мольных долей (Xi) и соответственно КX, а для изохорного процесса с использованием парциальных давлений реагентов (рi) и соответственно Кр.
Рассмотрим расчет равновесного состава продуктов реакции, протекающей при постоянном давлении.
Пусть в начальный момент времени в системе содержится соответственно nA, nB, nD, nE молей реагентов и к моменту наступления равновесия прореагирует x молей вещества А. Тогда в результате реакции число молей исходных веществ и продуктов изменится и станет равным соответственно nA- x, nB- 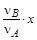 , nD+
, nD+ 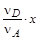 , nE+
, nE+ 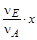 .
.
Мольная доля i-го вещества в равновесной смеси равна:
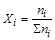 ,
,
где Sni – суммарное число молей всех веществ в системе в состоянии равновесия,
Sni =(nA- x)+( nB- 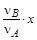 )+( nD+
)+( nD+ 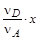 )+( nE+
)+( nE+ 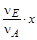 ).
).
Константа равновесия данной реакции
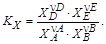
Подставив в константу равновесия соответствующие выражения для мольных долей реагентов, получим уравнение с одним неизвестным x. Его решение позволяет рассчитать равновесный состав газовой смеси.
Примеры.
1. Рассчитать состав равновесной газовой смеси, получающейся в результате взаимодействия эквивалентной смеси водорода и азота по реакции 3H2 + N2 Û 2NH3 при давлении р и температуре Т = 700 К. Рассчитать выход аммиака.
Решение.
А. Расчет константы равновесия KX (Т, р).
Определяем изменение энергии Гиббса при протекании реакции
3H2 + N2 Û 2NH3
DfH0298, кДж/моль 0 0 –45,94
S0298, Дж/моль×K 130,52 191,50 192,66
Изменение энергии Гиббса при температуре Т = 700 К DrG0(700) можно вычислить по энтальпии и энтропии реакции при Т=298 К,
DrG0(Т) »DrН0298– Т×DrS0298,
DrН0298=(å ni×DfН0298i)продукты–(å ni×DfН0298i)исх. вещества,
DrS 0298=(åni×S0298i)продукты– (åni×S0298i) исх. вещества,
DrН0298 = 2× (–45,94) – (3×0 +1×0) = –91,88 кДж,
DrS 0298 = 2× (192,66) – (3×130,52 +1×191,50)= –197,74 Дж/K,
DrG0298 = –91,88 ×103– 700×(–197,74) = 46540Дж.
Рассчитываем величину 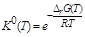 и
и 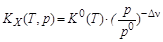 :
:
К0(700)=3,37×10-4, KX(700)= К0(700)×(p/p0)–Dn= К0(700)×( 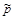 )–Dn,
)–Dn,
Dn =(2)–(3+1)= –2.
Б.) Расчет состава (мольные доли) газовой смеси в состоянии равновесия при 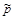 =1 атм (KX = К0).
=1 атм (KX = К0).
Поскольку водород и азот в начальный момент времени находятся в эквивалентных количествах, то на 3 моля водорода приходится 1 моль азота. Пусть к моменту прихода системы к равновесию израсходовалось x молей азота. Тогда в равновесной газовой смеси будет приходиться на nН2=3–3×x молей водорода в соответствии с уравнением реакции nN2=1–x молей азота и nNH3=2×x молей аммиака:
3H2 + N2 Û 2NH3
3-3×x 1-x +2×x
Суммарное число молей веществ в равновесной смеси
Sni = (3–3×x)+(1–x)+(2×x) =2× (2–x).
Тогда мольная доля i-го вещества будет равна соответственно:
XH2= 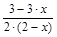 , XN2=
, XN2= 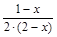 , XNH3=
, XNH3= 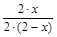 .
.
Константа равновесия KX будет равна:
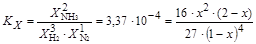 .
.
Условию задачи соответствует решение данного уравнения x= 0,0117.
Определив x,можно рассчитать мольные доли (Xi) компонентовв равновесной газовой смеси. Результаты расчета приведены в табл. 3.1.
Если бы реакция была необратима, то из 3 молей водорода и 1 моля азота образовалось бы 2 моля аммиака. Расчет показывает, что вследствие обратимости реакции в этих условиях образовалось только 2×x=0,00234 молей аммиака. Таким образом, выход целевого продукта составил величину (0,0234 /2)×100%=1,17%. Увеличить выход целевого продукта можно сместив равновесие, например изменив давление. Результаты расчета приведены в табл. 3.1.
Таблица 3.1
Состав (мольные доли компонентов Xi) равновесной газовой смеси реакции
3H2 + N2 Û 2NH3 при Т=700 К при различных давлениях
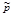 , атм , атм | H2 | N2 | NH3 | Выход NH3, % |
| 0,746 | 0,294 | 0,006 | 1,17 | |
| 0,663 | 0,221 | 0,116 | 20,8 | |
| 0,605 | 0,202 | 0,194 | 32,5 | |
| 0,528 | 0,176 | 0,296 | 45,6 |
Данные таблицы показывают, что увеличение давления приводит к увеличению выхода аммиака.
2. Расчет степени термической диссоциации тетрооксида диазота (N2О4) по реакции N2О4 Û 2 NО2 при температуре Т и давлении р.
Решение.
А. Расчет константы равновесия KX (Т, р).
Определяем изменение энергии Гиббса при протекании реакции
N2О4 Û 2 NО2
DfH0298, кДж/моль 11,11 34,19
S0298, Дж/моль×K 304,35 240,06
Изменение энергии Гиббса при температуре Т DrG0(Т) можно вычислить по энтальпии и энтропии реакции при Т=298 К:
DrG0(Т)» DrН0298– Т×DrS0298,
DrН0298= (å ni×DfН0298i)продукты–(å ni×DfН0298i)исх. вещества ,
DrS 0298=(åni×S0298i)продукты–(åni×S0298i) исх. вещества ,
DrН0298 = 2× (34,19) – (11,11) = 57,27 кДж,
DrS 0298 = (2×240,06) – 304,35 = 175,77 Дж/K,
DrG0298 = 57,27×103–323×175,77 = 496,29 Дж.
Рассчитываем величину 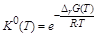 и
и 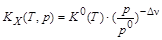 .
.
Поскольку для данной реакции Dn =(2)–(1)= +1, то
KX(T, р)= К0(T)×(p/p0)–1= К0(T)×( 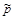 )–1
)–1
Б. Расчет состава (мольные доли) газовой смеси в состоянии равновесия.
Пусть к моменту равновесия из каждого моля N2О4 распалось x молей. Тогда в равновесной газовой смеси будет приходиться на nN2О4= 1–x молей тетрооксида диазота nNО2= 2×x молей диоксида азота:
N2О4 Û 2 NО2
1–x 2×x
Суммарное число молей N2О4 и NО2 в равновесной смеси:
Sni = (1–x) + (2×x) = 1+x.
Тогда мольная доля веществ в равновесной смеси Xi=ni/Sni будет равна:
XN2О4= 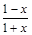 , XNО2=
, XNО2= 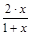 .
.
Для константы равновесия KX можно написать:
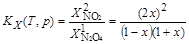
откуда x = 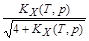 .
.
В. Расчет степени диссоциации N2О4.
Степень диссоциации (a) – это доля молекул вещества от их начального количества, которая подверглась диссоциации. Поскольку к моменту равновесия из одного моля N2О4 распалось на NО2 x молей, то x º a:
a(T, p)= 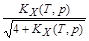 .
.
Таким образом, степень диссоциации N2О4 зависит от температуры и давления. Например, при Т=100°С и 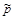 =1атм
=1атм
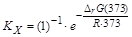 =14,50, a= 0,885, XN2O4= 0,061, XNO2= 0,939.
=14,50, a= 0,885, XN2O4= 0,061, XNO2= 0,939.
 Результаты аналогичных расчетов для реакции диссоциации N2О4 в графическом виде представлены на рис.3.2.
Результаты аналогичных расчетов для реакции диссоциации N2О4 в графическом виде представлены на рис.3.2.
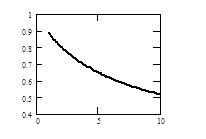

Рис. 3.2. Зависимость степени диссоциации N2О4 (a) от давления р при постоянной температуре Т=100°С (а) и от температуры Т при постоянном давлении р=1атм(б)
Степень диссоциации N2О4 является количественной характеристикой смещения равновесия реакции N2О4 Û 2 NО2. При a®1 равновесие в системе смещено в сторону образования продуктов диссоциации. Увеличение давления приводит к уменьшению a, а увеличение температуры – к увеличению a. Эти закономерности полностью соответствуют выводам анализа уравнений изобары и изотермы реакции.
Равновесия в растворах
Растворы
Раствор является гомогенной однофазной многокомпонентной системой переменного состава, образованной двумя или более веществами, которые, как правило, подразделяются на растворитель и растворенное вещество. Растворителем считается то вещество, которое в чистом виде находится в такой же фазе, что и раствор. Если раствор образуют два вещества в одной фазе (например, две жидкости), то растворителем обычно считается то вещество, которого больше (в мольных долях). Но если вода является одним из веществ, образующих раствор, то ее всегда считают растворителем. По агрегатному состоянию растворителя растворы делятся на газовые, жидкие и твердые.
Одним из способов получения растворов является растворение вещества в растворителе. Растворение – это процесс образования однофазной многокомпонентной системы из многофазной.
Различают физическое и химическое растворение.
Физическое растворение – это переход вещества в раствор, не сопровождающийся изменением химического состава. Вследствие этого растворенное вещество может быть вновь выделено из раствора путем изменения какого либо внешнего параметра. Например, понижение давления или повышение температуры приводит к выделению из жидкости растворенных газов.
Химическое растворение – это переход вещества в раствор, который сопровождается реакцией, приводящей к изменению химического состава растворенного вещества. В этом случае растворенное вещество не может быть выделено из раствора путем изменения внешних параметров системы. Например, при растворении металла в кислоте образуется раствор его соли. Изменением только температуры нельзя выделить металл из раствора.
Растворимостью вещества называется максимально возможная его концентрация в растворе при данных условиях (температура, давление). Она характеризует способность вещества переходить в растворитель с образованием раствора. Если не достигнута величина растворимости, то раствор называется ненасыщенным. При достижении растворимости между раствором и веществом устанавливается динамическое равновесие, раствор называется насыщенным.
Важную роль при образовании растворов играют химические связи как в растворителе, так и в растворяемом веществе. В газах межмолекулярные взаимодействия невелики, поэтому при невысоких давлениях они смешиваются друг с другом в любых соотношениях, их взаимная растворимость является неограниченной. В твердом состоянии вещества образуют растворы, если частицы растворяемого вещества могут заменять в узлах кристаллической решетки частицы растворителя. При этом необходимо выполнение по крайней мере двух условий. Во-первых, геометрические размеры частиц растворителя и растворенного вещества не должны сильно различаться. Во-вторых, частицы растворенного вещества должны образовывать химические связи с частицами растворителя. Эти условия выполняются, например, при образовании сплавов металлов.
В жидкости частицы связаны между собою силами межмолекулярного взаимодействия и водородными связями. При описании свойств жидких растворов необходимо учитывать взаимодействия между частицами растворителя, частицами растворенного вещества с частицами растворителя и между частицами растворенного вещества.
Образование раствора происходит, если изменение энергии Гиббса при растворении меньше нуля (термодинамическое условие протекания изобарного процесса DG0=DH0– T DS0< 0). При достижении растворимости устанавливается равновесие (DG0=0).
При физическом растворении происходит разрушение структуры растворяемого вещества (разрушение кристаллической структуры твердого вещества, диссоциация растворенных молекул и т.д.) и сольватация частиц растворенного вещества (в случае водных растворов – гидратация). Сольватация представляет собой образование химических связей между частицами растворителя и молекулами или ионами растворенного вещества. При этом каждая частица растворенного вещества оказывается окруженной частицами растворителя, образующими сольватную оболочку (в случае водных растворов – гидратную оболочку).
Тепловой эффект растворения (DН0) будет определяться суммой изменения энтальпий разрушения структуры растворяемого вещества (DдН0) и теплового эффекта сольватации (DсН0). Разрушение структуры растворяемого вещества является эндотермическим процессом (DдН0>0), а сольватация – экзотермическим (DгидрН0< 0).
В большинстве случаев при растворении газов энтропия системы понижается (DS0<0), а при растворении твердого вещества – повышается (DS0 >0).
Соотношение изменения энтальпий разрушения структуры растворяемого вещества (DдН0), теплового эффекта сольватации (DсН0) и энтропии растворения (DS0) позволяет определить термодинамическую возможность растворения, а так же растворимость и ее температурную зависимость.
Пример.
1. Растворение в воде газов, не образующих с ней химических соединений. Так как нет необходимости в разрушении структуры вещества, то DдН0»0. При растворении происходит гидратация молекул газа, и поэтому изменение энтальпии при растворении меньше нуля (DН0<0). Поскольку энтропия системы при растворении газов понижается (DS0<0), то энтропийный фактор не способствует процессу растворения. Поэтому самопроизвольное растворение газов происходит при низких температурах ( 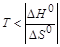 ). Растворимость газов растет при понижении температуры.
). Растворимость газов растет при понижении температуры.
2. Растворение твердых веществ в воде. Так как разрушение кристаллической решетки происходит с затратами энергии, тоDдН0>0. При растворении происходит гидратация частиц растворенного вещества (DсН0<0). Таким образом, изменение энтальпии при растворении DН0=DдН0 + DсН0может быть как отрицательным, так и положительным. Энтальпийный фактор может, как способствовать, так и препятствовать растворению. При растворении кристаллических веществ в жидкости DS0>0, поэтому повышение температуры способствует растворению.
Одной из важных характеристик раствора является концентрация, которая показывает относительное соотношение растворенного вещества и растворителя. Концентрация указывает количество растворенного вещества в единицах массы, молях, эквивалентах, объемах и др., содержащегося в массе или в объеме раствора, в массе или в объеме растворителя и т. д. Способов выражения концентрации может быть много. В химии и смежных областях науки и техники наиболее часто используются следующие.
1. Массовые концентрации – отношение количества растворенного вещества к общей массе раствора или растворителя:
· массовая доля растворенного вещества – отношение массы растворенного вещества к общей массе раствора. Массовая доля, выраженная в процентах (w %), численно равна массе растворенного вещества в граммах, содержащейся в 100 г раствора;
· моляльная концентрация (моляльность раствора) См – отношение количества растворенного вещества в молях (n) к массе растворителя. Моляльность раствора выражается в [моль/кг] и численно равна количеству вещества в молях, приходящемуся на 1 кг растворителя.
2. Объемные концентрации – отношение количества растворенного вещества к объему раствора:
· молярная концентрация (молярность раствора) – отношение количества растворенного вещества в молях (n) к объему раствора. Молярность раствора выражается в [моль/л] и численно равна количеству растворенного вещества в молях, содержащемуся в 1 литре раствора;
· нормальная концентрация (нормальность раствора) – отношение количества растворенного вещества в эквивалентах (nэ) к объему раствора. Нормальность раствора выражается в [экв/л] и численно равна количеству растворенного вещества в эквивалентах, содержащемуся в 1 литре раствора;
· массовая концентрация вещества в растворе – отношение массы растворенного вещества к объему раствора [г/л] – количество растворенного вещества в г, содержащееся в 1 литре раствора.
3. Мольная (молярная) доля показывает отношение числа молей растворенного вещества n к общему числу молей в растворе. Мольная доля выражается в долях единицы или в процентах (мольный процент – моль %).
