Сухая перегонка или пиролиз древесины - нагревание древесины до 5500C
Альдольная конденсация кетонов.
Кетоны значительно труднее вступают в реакции альдольной автоконденсации по сравнению с альдегидами. Структурные условия здесь неблагоприятны как с точки зрения скорости, так и сточки зрения равновесия. Однако если реакцию проводить при кислотном катализе, то образующийся продукт конденсации будет быстро дегидратироваться, превращаясь в мезитилоксид. Эта последняя стадия смещает равновесие в сторону полного превращения кетона. . Каталитическая гидратацией алкинов (кроме этина) (реакция Кучерова):
R−C≡CH−→−−+H2OR−C(=O)−CH3R−C≡CH→+H2OR−C(=O)−CH3.
24.Кислородосодержащие кислоты серы: H2SO4 - тяжелая маслянистая жидкость ,купоросное масло ,нелетучая, хорошо растворима в воде очень гигроскопична, обладает водоотнимающими свойствами (обугливание бумаги, дерева, сахара).окислитель.
Производство H2SO4:
1-я стадия. Обжиг пирита в печи для обжига в кипящем слое 4FeS2 + 11O2 =2Fe2O3 + 8SO2 + Q Процесс гетерогенный:
1) измельчение железного колчедана (пирита);
2) метод "кипящего слоя";
3) 800°С; отвод лишнего тепла;
4)увеличение конц-ции O2 в воздухе.
2-я стадия. После очистки, осушки и теплообмена сернистый газ поступает в контактный аппарат, где окисл-ся в серный ангидрид (450°С – 500°С; катализатор V2O5): 2SO2 + O2 -> 2SO3.
3-я стадия. Поглотительная башня: nSO3 + H2SO4(конц) -> (H2SO4 • nSO3)(олеум)
Применяют керамические насадки и принцип противотока.
Хим св-ва:
Свойства серной кислоты.
Свойства серной кислоты. Химически чистая серная кислота — тяжелая бесцветная маслянистая жидкость. Обладает сильными гигроскопическими свойствами, поэтому применяется для осушения газов. Она хорошо растворяет оксид серы(VI) и, как вы уже знаете, этот раствор называют олеумом. Вы также знаете правило разбавления концентрированной серной кислоты: нельзя приливать воду к кислоте, а следует осторожно, тоненькой струйкой вливать кислоту в воду, непрерывно помешивая раствор.
Слайд 13
Химические свойства серной кислоты
в значительной степени зависят от ее концентрации. Разбавленная серная кислота проявляет все характерные свойства кислот: взаимодействует с металлами, стоящими в ряду напряжений до водорода, с оксидами металлов (основными и амфотерными), с основаниями и солями. Поскольку серная кислота двухосновная, она образует два ряда солей: средние (сульфаты) и кислые (гидросульфаты). Реактивом на серную кислоту и сульфаты является хлорид бария: сульфат-ионыSО42- с ионами Ва2+ образуют белый нерастворимый сульфат бария: Ва2+ + SО42- = ВаSО4
Сульфаты — минералы, соли H2SO4. В их кристаллической структуре обособляются комплексные анионы SO42− .Р-ция с хлоридом бария даёт белый кристаллический осадок сульфата бария: 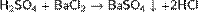 ПолучениеГидросульфаты получают при избытке серной кис-ты:Na2CO3 + H2SO4(изб.)= 2NaHSO4 + H2O + CO2↑Также умеренным нагреванием сульфатов с серной кис-той:K2SO4 + H2SO4 = 2KHSO4
ПолучениеГидросульфаты получают при избытке серной кис-ты:Na2CO3 + H2SO4(изб.)= 2NaHSO4 + H2O + CO2↑Также умеренным нагреванием сульфатов с серной кис-той:K2SO4 + H2SO4 = 2KHSO4
Кислородсодержащие кислоты азота
Из кислородсодержащих кислот азота наиболее известны азотистая НNО2 и азотная НNО3 кислоты. Азотистая кислота. Получается при растворении оксида азота (III) в воде: N2O3 + H2O = 2HNO2 Азотистая кислота неустойчива и легко разлагается: 3HNO2 = HNO3 + 2NO + H2O А вот ее соли — нитриты — более устойчивы. Нитриты щелочных металлов плавятся без разложения. В небольших дозах их используют при изготовлении колбас, однако большие дозы их ядовиты.
Азотная кислота.
Получение азотной кислоты. В промышленности азотную кислоту получают в три стадии. Контактное окисление аммиака до оксида азота (II): 4NH3 + 5O2 = 4NO + 6 H2O катализатором является платина. 2.Окисление оксида азота(II) до оксида азота(IV) кислородом воздуха: 2NO + O2 = 2NO2 Взаимодействие оксида азота(IV) с водой в избытке кислорода: 4NO2+ 2H2O+O2 = 4HNO3
Свойства азотной кислоты.
В разбавленных растворах азотная кислота полностью диссоциирует: 4NO2 + 2H2O + O2 = 4HNO3 HNO3 = H+ +NO3- Азотная кислота проявляет все типичные свойства кислот: взаимодействует с оксидами металлов, основаниями, солями: 2HNO3 +CuO = Cu(NO3)2 + H2O Ba(OH)2 + 2HNO3 = Ba(NO3)2 + 2H2O 2HNO3 + CaCO3 = Ca(NO3)2 + CO2 + H2O 2HNO3 + Na2SiO3 = H2SiO3 + 2 NaNO3
Азотную кислоту используют для производства азотных и комплексных удобрений, серной и фосфорной кислот, взрывчатых веществ, красителей, лекарств, пластмасс, пленок, нитролаков и нитроэмалей, искусственных волокон, как компонент нитрующей смеси, для травления и растворения металлов в металлургии.
25. Кислоты, их классификацияи свойствана основе представлений об электролитической диссоциации. 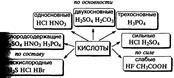 Соляная кислота — водный раствор газа хлоро-водорода в воде.
^ Химические свойства. Кислоты изменяют цвет индикаторов: лакмус
Соляная кислота — водный раствор газа хлоро-водорода в воде.
^ Химические свойства. Кислоты изменяют цвет индикаторов: лакмус
окрашивается в красный цвет, метилоранж — в желтый.
При реакции с основаниями образуется соль и вода (реакция нейтрализации). В реакцию вступают как растворимые, так и нерастворимые в воде основания:
При реакции с основными оксидами образуются со ли:
Кислоты реагируют с металлами, находящимися в ряду напряжений до водорода, при этом выделяется газообразный водород и образуется соль.
Получение кислот. Многие кислоты можно получить при реакции кислотных оксидов с водой:
^ Концентрированная серная кислота при обычной температуре не действует на многие металлы. По этой причине, например, безводная
концентрированная серная кислота действует почти на все металлы при нагревании. При этом образуются соли серной кислоты, однако водород не выделяется, а получаются другие вещества, например сернистый газ.
Так, при нагревании концентрированной серной кислоты с медью вначале серная кислота окисляет медь до окиси меди, а сама восстанавливается при этом до сернистой кислоты, которая тотчас же разлагается на сернистый газ и воду:
Образовавшаяся окись меди реагирует с избытком серной кислоты, образуя соль и воду:
Таким образом, окись меди является промежуточным веществом в этой реакции. Сложив эти уравнения, мы получим итоговое уравнение реакции, в которое входят только исходные и конечные вещества.
26. класс алкены общая формула и химическое строение гомологов. Алкены (олефины) – ненасыщенные ациклические углеводороды с одной двойной связью, общая формула гомологического ряда CnH2n. Название образуется от углеводорода с наиболее длинной цепью, содержащей двойную связь, с добавлением суффикса -ен. Цифрой указывается положение двойной связи. В табл. 12.3 приведены первые четыре алкена, число изомеров которых увеличивается не только из-за изомерии скелета, но также изомерии положения двойной связи и геометрической изомерии (цис-транс). Названия одновалентных радикалов получают добавлением -ил к названию соответствующего углеводорода.
Полиалкены бывают трех типов:
С изолированными двойными связями
CH2=CH—CH2—CH2—CH=CH2 1,5-гексадиен
С сопряженными двойными связями
CH2=CH-CH=CH2 1,3-бутадиен (используется при получении полимеров)
В полиалкенах с сопряженными (чередующимися) двойными связями происходит делокализация π-электронов. Соединения с двойными связями легко полимеризуются.
Этиле́н (по ИЮПАК: этен) — органическое химическое соединение, описываемое формулой С2H4. Является простейшим алкеном(олефином). В природе этилен практически не встречается. Это бесцветный горючий газ со слабым запахом. Частично растворим в воде (25,6 мл в 100 мл воды при 0°C), этаноле (359 мл в тех же условиях). Хорошо растворяется в диэтиловом эфире и углеводородах. Содержит двойную связь и поэтому относится к ненасыщенным или непредельным углеводородам. Играет чрезвычайно важную роль в промышленности, а также является фитогормоном. Этилен — самое производимое органическое соединение в мире[1]; общее мировое производство этилена в 2008 году составило 113 миллионов тонн и продолжает расти на 2—3 % в год[2].
Применение
Этилен является ведущим продуктом основного органического синтеза и применяется для получения следующих соединений (перечислены в алфавитном порядке):
Винилацетат;
Дихлорэтан / винилхлорид (3-е место, 12 % всего объёма);
Окись этилена (2-е место, 14—15 % всего объёма);
Полиэтилен (1-е место, до 60 % всего объёма);
Стирол;
Уксусная кислота;
Этилбензол;
Этиленгликоль;
Этиловый спирт.
Этилен в смеси с кислородом использовался в медицине для наркоза вплоть до середины 80-х годов ХХ века в СССР и на ближнем Востоке. Этилен является фитогормоном практически у всех растений[4], среди прочего[5] отвечает за опадание иголок у хвойных.
Основные химические свойства
Этилен — химически активное вещество. Так как в молекуле между атомами углерода имеется двойная связь, то одна из них, менее прочная, легко разрывается, и по месту разрыва связи происходит присоединение, окисление, полимеризация молекул.
Галогенирование:
CH2=CH2 + Cl2 → CH2Cl—CH2Cl
Происходит обесцвечивание бромной воды. Это качественная реакция на непредельные соединения.
Гидрирование:
CH2=CH2 + H - H → CH3 - CH3 (под действием Ni)
Гидрогалогенирование:
CH2=CH2 + HBr → CH3 - CH2Br
Гидратация:
CH2=CH2 + HOH → CH3CH2OH (под действием катализатора)
Эту реакцию открыл A.M. Бутлеров, и она используется для промышленного получения этилового спирта.
Окисление:
Этилен легко окисляется. Если этилен пропускать через раствор перманганата калия, то он обесцветится. Эта реакция используется для отличия предельных и непредельных соединений.
Окись этилена — непрочное вещество, кислородный мостик разрывается и присоединяется вода, в результате образуется этиленгликоль:
Горение:
Полимеризация.
27. Классификация органических соединений. В зависимости от строения углеродных цепей среди органических соединений выделяются следующие три ряда:
1) соединения с открытой цепью атомов углерода, которые также называются ациклическими, или соединения жирного ряда (это название возникло исторически: к первым соединениям с длинными незамкнутыми углеродными цепями принадлежали кислоты).
В зависимости от характера связей между атомами углерода эти соединения подразделяются на: а) предельные (или насыщенные), которые содержат в молекулах только простые (ординарные) связи; б) непредельные (или ненасыщенные), в молекулах которых имеются кратные (двойные или тройные) связи между атомами углерода;
2) соединения с замкнутой цепью атомов углерода, или карбоциклические. Эти соединения, в свою очередь, подразделяются:
а) на соединения ароматического ряда.
Они характеризуются наличием в молекулах особой циклической группировки из шести атомов углерода – бензольного ароматического ряда.
Эта группировка отличается характером связей между атомами углерода и придает содержащим ее соединениям особые химические свойства, которые называются ароматическими свойствами;
б) алициклические соединения – это все остальные карбоциклические соединения.
Они различаются по числу атомов углерода в цикле и в зависимости от характера связей между этими атомами могут быть предельными и непредельными;
3) гетероциклические соединения.
В молекулах этих соединений имеются циклы, которые включают, кроме атомов углерода, также гетероатомы.
В рядах ациклических (жирных) и карбоциклических соединений простейшими являются углеводороды. Все остальные соединения этих рядов рассматриваются как производные углеводородов, которые образованы замещением одного, двух или нескольких атомов водорода в углеводородной молекуле другими атомами или группами атомов.
Остатки углеводородов, которые образуются при отнятии от их молекул одного, двух или нескольких атомов водорода, называютсяуглеводородными радикалами.
Атомы или группы атомов, которые замещают водород в углеводородной основе, образуют функциональные или характеристические(этот термин разработан Международным союзом теоретической и прикладной химии) группы, обусловливающие общие химические свойства веществ, которые принадлежат к одному и тому же классу производных углеводородов.
Виды органических соединений:
1) галогенопроизводные углеводороды: а) фторпроизводные; б) хлорпроизводные; в)бромопроизводные, г) йодопроизводные;
2) кислородосодержащие соединения: а) спирты и фенолы; б) простые эфиры; в) альдегиды; г) кетоны.
28. Классификациихимическихреакцийв неорганической и органической химииКлассификация по составу исходных веществ и продуктов реакции.
Реакции соединения — из несколькихвеществ(простыхили сложных) образуется сложное вещество ^ Реакции разложения — сложноевеществопревращаетсяв несколько веществ (простых или сложных):
Реакциизамещения—изпростогоисложноговеществобразуется простое и сложное вещества:
Реакции обмена — издвухсложныхвеществобразуютсядвасложных вещества:
^ Классификация по изменению степени окисления.
Окислительно-восстановительные реакции — в ходереакции происходит изменение степеней окисления элементов:
^ Реакции ионного обмена — изменениястепенейокисленияне происходит.
41. Химическое равновесие. Константа равновесия. Химическое равновесие достигается, когда Vпрямой реакции=Vобратной реакции, т. е. в реакции aA+bB↔lL+dD Vпрямой реакции =kпрямой реакции[A] a[B] b=Vобратной реакции =kобратной реакции[L] l[D]d . Отсюда можно найти константу равновесия – произведение концентраций продуктов реакции, к произведению концентраций исходных веществ, в степенях равных коэффициенту перед формулами: kравновесия=([Ll][Dd])/([A]a[B]b)
Строение мицеллы коллоидов
Кол. частица состоит из ядра, адсорбирующего из окруж. среды иона другого вида, эти ионы наз-ся зарядообразующими. Ядро кол. частицы притягивает к себе из среды ионы противопол. знака. все сочетание, сост. из кол. частицы и эквивал-ой ей части дисперсной среды, наз-ся мицеллой.
Т.е, мицелла:
-ядро
-адсорбирующий слой
-слой противоионов
Кол. частица – это мицелла и диффузионный слой противоионов.
Оптич. св-во:
Если пропускать пучок света через совершенно прозрачный кол. раствор, то он станов. видимым.
Элект. св-во:
Частицы дисперсной фазы перемещаются к аноду при возд.пост.эл.тока, а частицы дисперсионной среды – к катоду. Дисп. фаза несет на себе заряд противоп.заряду среды.
