Обратимые и необратимые процессы.Энтропия
В изолированной термодинамической системе через некоторый промежуток времени устанавливается внутреннее равновесие, при котором рабочее тело по всей массе имеет одинаковую температуру и давление.
При равенстве давлений в системе и в окружающей среде изменение объема рабочего тела прекращается, и передача энергии в форме работы отсутствует (система находится в механическом равновесии со средой). Равенство температур рабочего тела и среды обеспечивает термическое равновесие. При этом между системой и окружающей средой не возникает передачи энергии в форме теплоты. Термодинамический процесс возможен только при нарушении механического или термического равновесия, и чем сильнее нарушается равновесие, тем быстрее протекает процесс. Все реальные термодинамические системы не изолированы от окружающей среды, которая выводит их из равновесия. Поэтому они являются неравновесными. Учитывая чрезвычайную сложность теплотехнических расчетов таких процессов, на практике их заменяют равновесными, то есть такими, при которых система проходит последовательно бесчисленное множество равновесных состояний. Эти равновесные процессы называют квазистатическими.
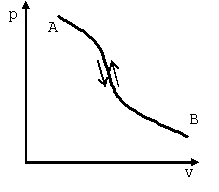
Рис. 5.1. Линии обратимых прямого A-B и обратного B-A процессов на pv-диаграмме
Для любой термодинамической системы можно представить два состояния, между которыми будет проходить два процесса: один от первого состояния ко второму и другой, наоборот, от второго состояния к первому. Первый процесс называют прямым, второй — обратным. Если после прямого процесса 1—2 следует обратный 2—1 и при этом термодинамическая система возвращается в исходное состояние, то такие процессы принято считать обратимыми. При обратимых процессах система в обратном процессе проходит через те же равновесные состояния, что и в прямом процессе. При этом ни в окружающей среде, ни в самой системе не возникает никаких остаточных явлений, то есть не имеет значения идет процесс А-В или В-А (рис. 5.1).
Рзличают механически и термически обратимые процессы.
В механически обратимом процессе обмен энергией между системой и окружающей средой протекает в форме работы при бесконечно малой разности давлений.
В термически обратимом процессе термодинамическая система обменивается с окружающей средой энергией в форме теплоты при бесконечно малой разности температур.
Любой равновесный термодинамический процесс изменения состояния рабочего тела будет всегда обратимым. Обратимые процессы являются идеальными.
Действительные термодинамические процессы совершаются при конечной разности давлений и температур рабочего тела и окружающей среды и поэтому являются неравновесными. Такие процессы необратимы.
Необратимый термодинамический процесс – это процесс, при котором система не возвращается в исходное состояние после обратного процесса. Все необратимые процессы протекают в направлении достижения в термодинамической системе равновесия, то есть выравнивания в ней давлений, температур, концентраций.
Энтропия:
Понятие энтропии было впервые введено в 1865 году Рудольфом Клаузиусом. Он определил изменение энтропии термодинамической системы при обратимом процессе как отношение изменения общего количества тепла ΔQ к величине абсолютной температуры T: ΔS=ΔQ/T
Рудольф Клаузиус дал величине S имя «энтропия», происходящее от греческого слова τρoπή, «изменение» (изменение, превращение, преобразование). Данное равенство относится к изменению энтропии, не определяя полностью саму энтропию.
Эта формула применима только для изотермического процесса (происходящего при постоянной температуре). Её обобщение на случай произвольного квазистатического процесса выглядит так: dS=ϬQ/T, где dS - приращение (дифференциал) энтропии, а δQ - бесконечно малое приращение количества теплоты.
Необходимо обратить внимание на то, что рассматриваемое термодинамическое определение применимо только к квазистатическим процессам (состоящим из непрерывно следующих друг за другом состояний равновесия).
Поскольку энтропия является функцией состояния, в левой части равенства стоит её полный дифференциал. Напротив, количество теплоты является функцией процесса, в котором эта теплота была передана, поэтому δQ считать полным дифференциалом нельзя.
Энтропия, таким образом, согласно вышеописанному, определена вплоть до произвольной аддитивной постоянной. Третье начало термодинамики позволяет определить её точнее: предел величины энтропии равновесной системы при стремлении температуры к абсолютному нулю полагают равным нулю.
