| Тема 12 | ФИЗИКА АТОМА | |
Строение атома · модель атома Томсона 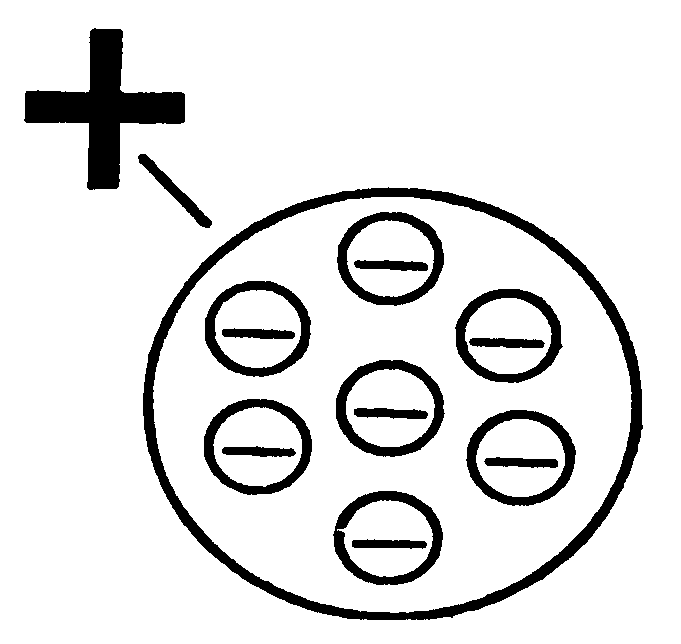 | ➨ английский ученый Томсон, открывший электрон (1897г.) и определивший (1898 г.) его заряд, на основе эксперимен-тальных данных (1903 г.) предложил первую модель атома – положительный заряд атома занимает весь объем атома и распределен в этом объеме с постоянной плотностью. Простейший атом (атом водорода) представляет собой по-ложительно заряженный шар радиусом около 10-8м, внутри которого находится электрон. У более сложных атомов в положительно заряженном ша-ре находится несколько электронов, так что атом подобен «булочке с изюмом», в котором роль изюминок играют электроны. Модель Томсона пользовалась признанием ученых до 1911 г. | |
· опыт Резерфорда по рассеянию 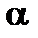 -частиц -частиц 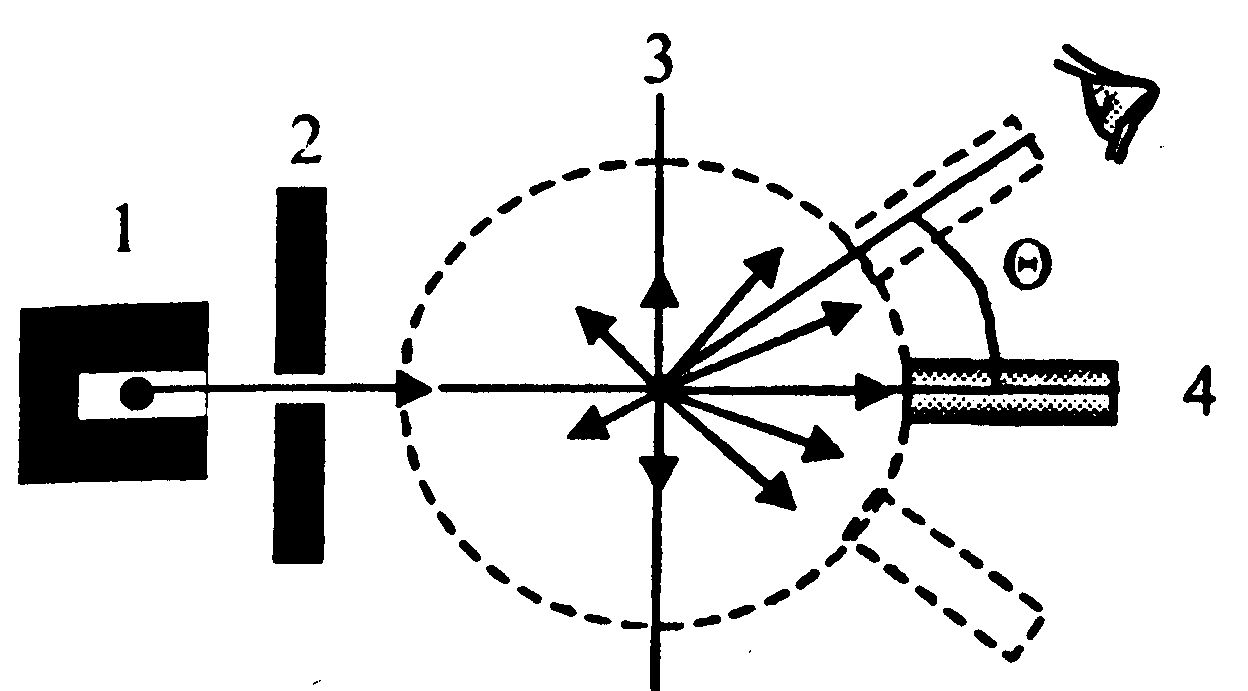 | ➨ английский физик Резерфорд, выполняя опыты по рассе-янию 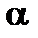 -частиц, пришел к выводу о несостоятельности мо-дели атома Томсона. Для изучения строения атома Резерфорд предложил зон-дирование атома с помощью -частиц, пришел к выводу о несостоятельности мо-дели атома Томсона. Для изучения строения атома Резерфорд предложил зон-дирование атома с помощью 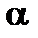 -частиц, которые испускались источником 1, помещенным внутри свинцовой полости, поглощающей все -частиц, которые испускались источником 1, помещенным внутри свинцовой полости, поглощающей все 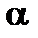 -частицы, кроме проходящих через ка-нал 2. Узкий пучок -частицы, кроме проходящих через ка-нал 2. Узкий пучок 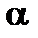 -частиц попадал на фольгу из золота 3. Рассеянные после взаимодействия с атомами золота -частиц попадал на фольгу из золота 3. Рассеянные после взаимодействия с атомами золота 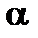 -час-тицы регистрировались под разными углами -час-тицы регистрировались под разными углами  визуально с помощью светочувствительного экрана и микроскопа 4. Угол отклонения некоторых частиц визуально с помощью светочувствительного экрана и микроскопа 4. Угол отклонения некоторых частиц  =1800 мог быть то-лько при лобовом столкновении положительно заряженной =1800 мог быть то-лько при лобовом столкновении положительно заряженной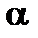 -частицы с положительно заряженным уплотнением в атоме. Резерфорд назвал его «ядро атома» и предложил в 1911 г. планетарную модель строения атома. -частицы с положительно заряженным уплотнением в атоме. Резерфорд назвал его «ядро атома» и предложил в 1911 г. планетарную модель строения атома. | |
· планетарная (ядерная) модель атома 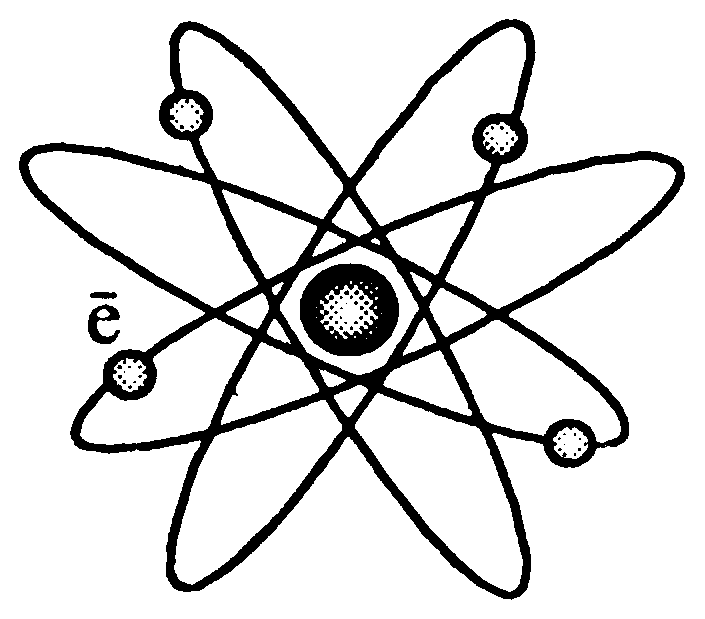 | ➨ Резерфорд предположил, что атом представляет собой ми-ниатюрную планетарную систему, в которой действуют элек-трические силы притяжения. В центре атома находится положительно заряженное ядро, в котором сосредоточена почти вся масса атома, но которое занимает ничтожно малую часть объема атома. Вокруг ядра по эллиптическим орбитам (как планеты вокруг Солнца) вращаются отрицательно заряженные электроны. Электронная оболочка занимает большую часть объема атома. Суммарный отрицательный заряд электронов равен положительному заряду атомного ядра. В целом атом ней-трален. Заряд ядра определяется порядковым номером хими-ческого элемента в периодической таблице Менделеева. Планетарная модель Резерфорда не смогла объяснить яв-ления испускания и поглощения атомами электромагнитных волн, опираясь на законы классической механики. | |
| · модель атома Бора | ➨ датский физик Н.Бор (1913 г.) утверждал, что законы дви-жения микрочастиц сильно отличаются от законов движения в макромире, что законы микромира – это квантовые законы, которые в то время еще не были установлены наукой. Поэтому Бор положил в основу своей теории постулаты. | |
| Постулаты Бора | ➨ ❶ Постулат стационарных состояний: электроны в атоме вращаются вокруг ядра по определенным стаци-онарным орбитам 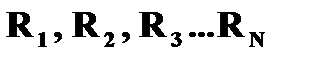 . Находясь на стаци-онарной орбите, электрон не излучает энергии. . Находясь на стаци-онарной орбите, электрон не излучает энергии. | |
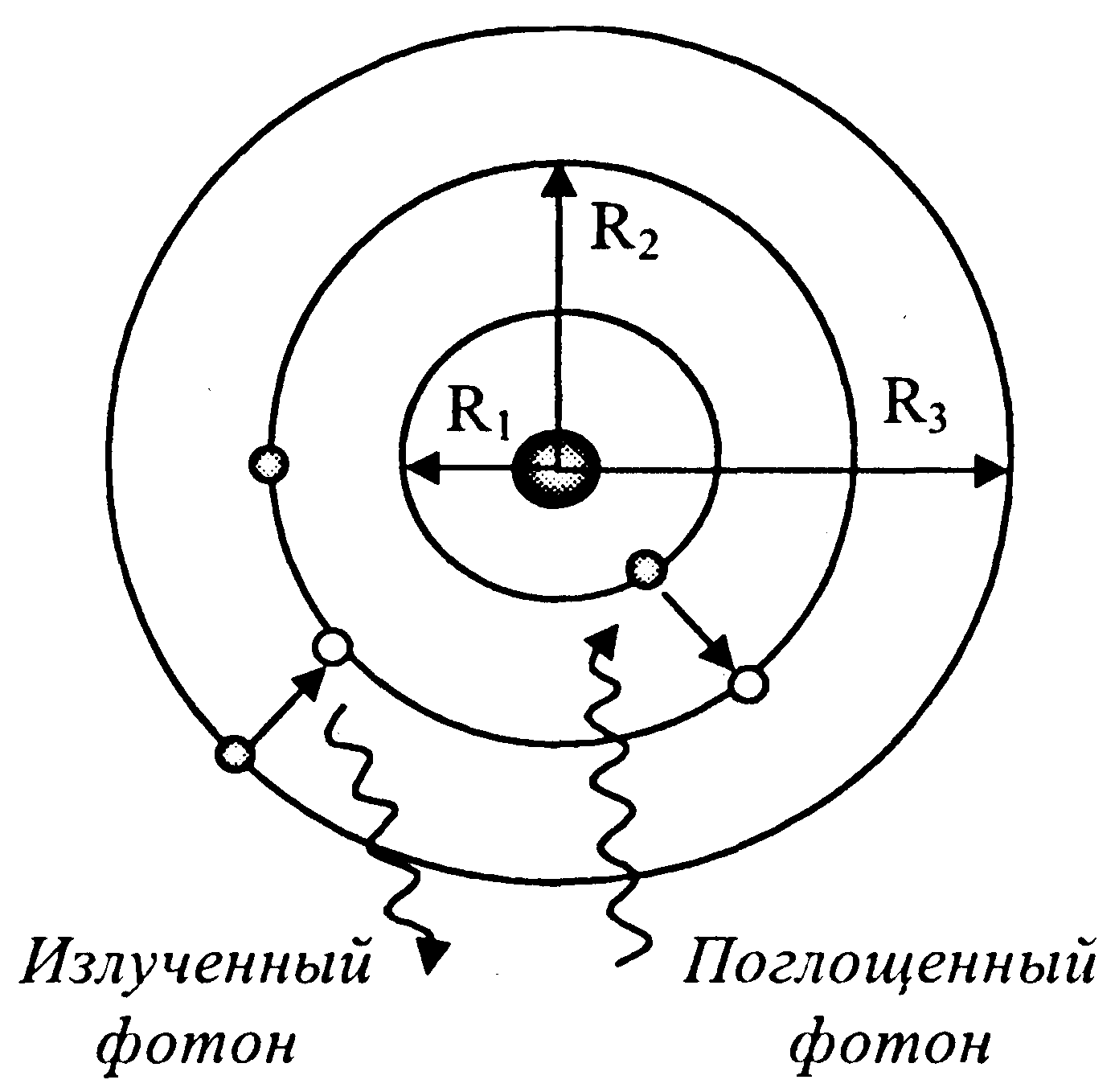 | |
❷ Условие квантования круговых орбит: каждому стационарному состоянию 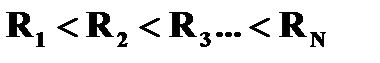 соответ-ствует строго определенная энергия соответ-ствует строго определенная энергия 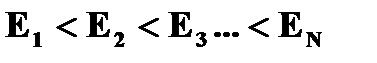 . Двигаясь по круговым орбитам электроны обладают квантованными значениями момента импульса: . Двигаясь по круговым орбитам электроны обладают квантованными значениями момента импульса: 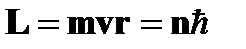 ( (  =1,2,3…) Квантованные значения – определенные дискретные значения, целые кратные постоянной Планка - =1,2,3…) Квантованные значения – определенные дискретные значения, целые кратные постоянной Планка - 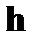 =6,63×10-34 Дж×с или =6,63×10-34 Дж×с или 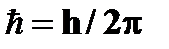 = 1,054×10-34 Дж×с. = 1,054×10-34 Дж×с. | |
❸ Правило частот: излучение или поглощение энергии атомом происходит при переходе электрона с одной стационарной орбиты 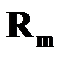 на другую на другую 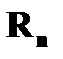 ; при этом излучается или поглощается квант световой энергии (фотон). Энергия фотона равна разности энергий электрона ; при этом излучается или поглощается квант световой энергии (фотон). Энергия фотона равна разности энергий электрона 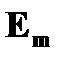 и и 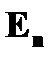 на соответствующих стационарных орбитах на соответствующих стационарных орбитах 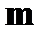 и и  : :  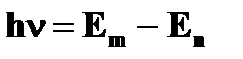 , где , где  - частота фотона. - частота фотона. | |
| Модель атома водорода по Бору | ➨ исходя из постулатов и используя планетарную модель строения атома, Бор разработал количественную теорию атома водорода. Он предположил, что стационарные кру-говые орбиты входят в число всевозможных атомных орбит, допускаемых классической механикой и электродинамикой. Поэтому сначала можно найти «классическое решение зада-чи, а затем использовать метод квантования круговых орбит. | |
| | |
| · строение атома водорода | ➨ атом водорода состоит из ядра (в состав которого входит один протон) и одного электрона, вращающегося вокруг ядра по круговой орбите. | 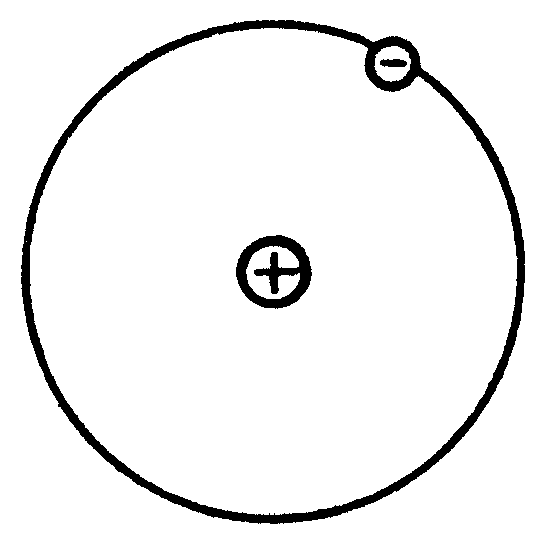 | |
| Стационарные орбиты и энергетические уровни | ➨ при движении по круговой орбите кулоновская сила притяжения к ядру обеспечивает электрону центростремительное ускорение: 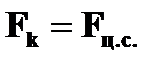 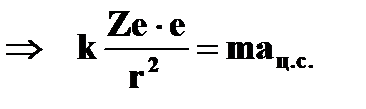 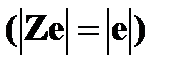 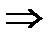 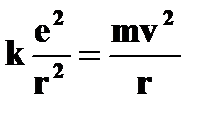 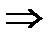 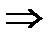 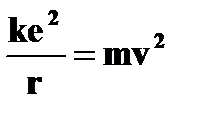 (или (или 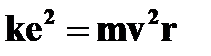 , или , или 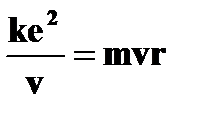 , но , но 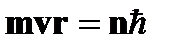 ) ) 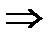 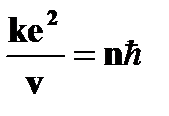 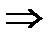 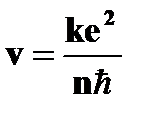 , где , где 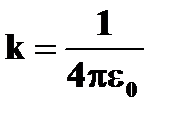 . Так как . Так как  =1,2,3…, то можно вычислить радиусы первой, второй и всех последующих стационарных круговых орбит электронов в атоме. =1,2,3…, то можно вычислить радиусы первой, второй и всех последующих стационарных круговых орбит электронов в атоме. | |
· скорость электрона на стационарных круговых орбитах 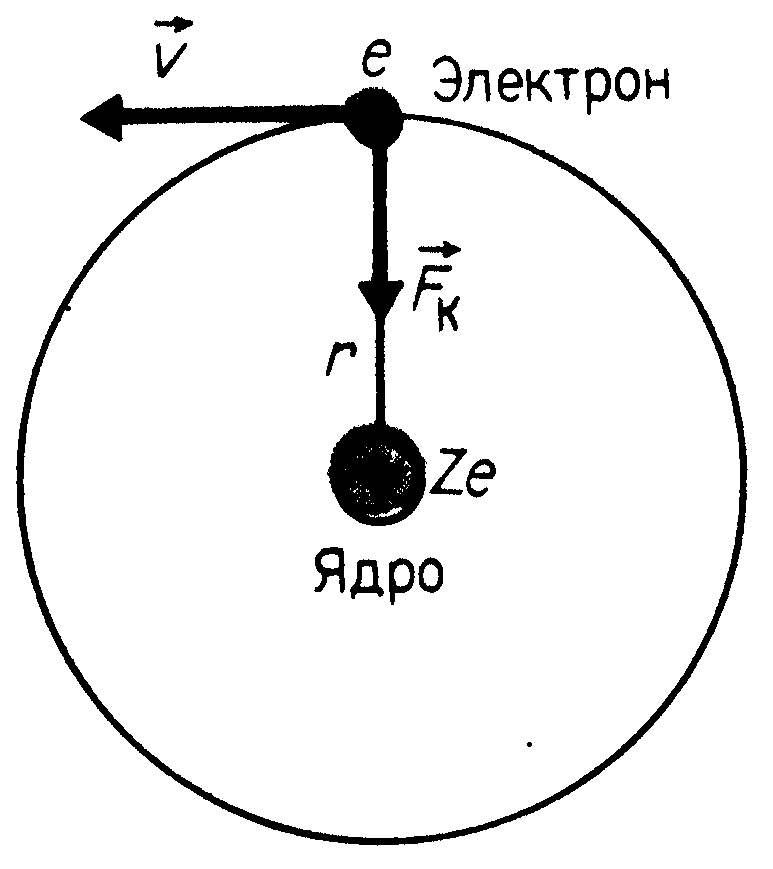 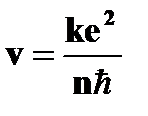 | |
· радиус стационарных круговых орбит 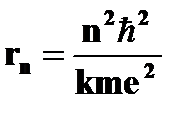 | ➨ 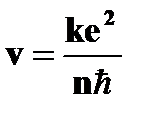 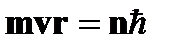 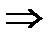 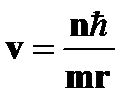 , , | } 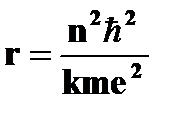 ,где ,где  =1,2,3…; =1,2,3…; 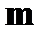 - масса электрона. - масса электрона. | |
· первый боровский радиус 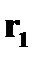 = 0,528×10-10м = 0,528×10-10м | ➨ радиус первой орбиты в атоме водорода при  =1. Первый боровский радиус служит единицей длины в атомной физике. =1. Первый боровский радиус служит единицей длины в атомной физике. | |
| Энергия электрона | ➨ двигаясь по каждой из разрешенных стационарных круговых орбит, электрон обладает определенным запа-сом кинетической энергии, а также и потенциальной энергией в электрическом поле атомного ядра. | |
· потенциальная энергия электрона на стационарной орбите 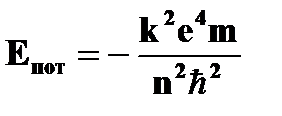 = = 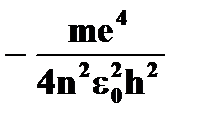 | ➨ 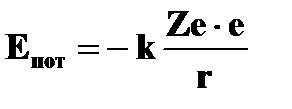 -потенциальная энергия системы двух зарядов (ядра и электрона); -потенциальная энергия системы двух зарядов (ядра и электрона); 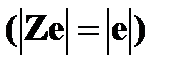 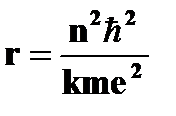 ; ; 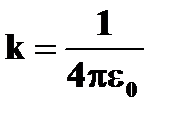 ; ; 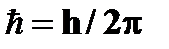 ; ( ; (  =1,2,3…). =1,2,3…). | |
· кинетическая энергия электрона на стационарной орбите 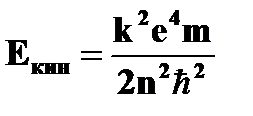 = = 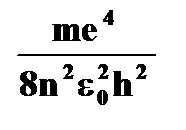 | ➨ 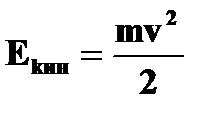 , , 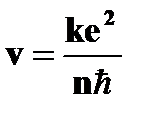 , , 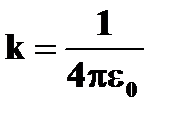 , , 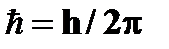 ; ( ; (  =1,2,3…). ➨ кинетическая энергия электрона на любой орбите составляет половину его потенциальной энергии: =1,2,3…). ➨ кинетическая энергия электрона на любой орбите составляет половину его потенциальной энергии: 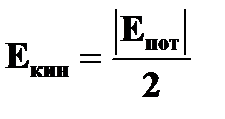 | |
· полная энергия электрона на стационарной орбите 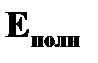 = = 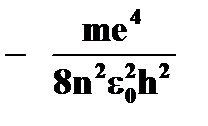 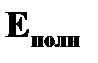 ~ ~ 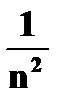 | ➨ 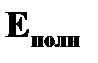 = = 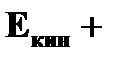 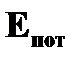 = = 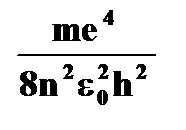 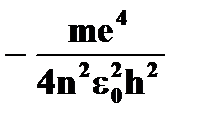  (приводим к общему знаменателю) (приводим к общему знаменателю)  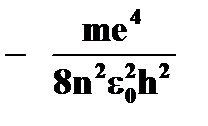 . После подстановки численных данных постоянных получаем: . После подстановки численных данных постоянных получаем: 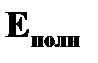 = = 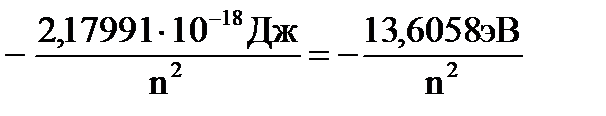 , т.е. полная энергия электрона на орбите обратно пропорциональна квадрату порядкового номера орбиты. , т.е. полная энергия электрона на орбите обратно пропорциональна квадрату порядкового номера орбиты. | |
· единицы энергии 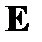 [Дж], [эВ] [Дж], [эВ] | ➨ 1 эВ = 1,6×10-19 Дж (заряд электрона) 1 Дж = 6,24×1018 эВ | |
· энергетические 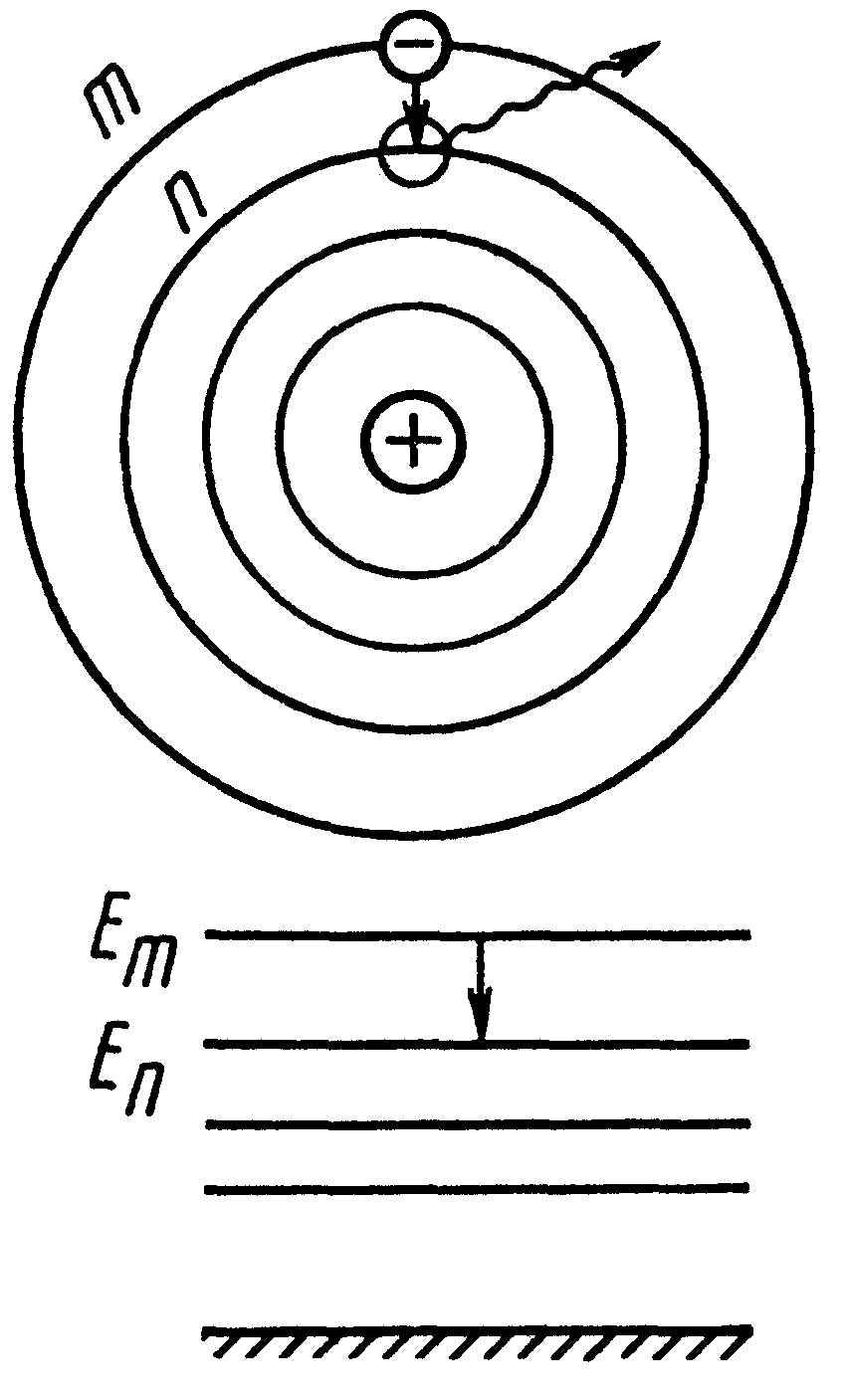 диаграммы диаграммы | ➨ используются для наглядного представления возмож-ных энергетических состояний атомов. На энергетической диаграмме каждое стационарное состояние отмечается горизонтальной линией, называ-емой энергетическим уровнем. Переходу электрона со стационарной орбиты под номером 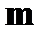 на стационарную орбиту под номером на стационарную орбиту под номером  соответствует переход атома из состояния с энергией соответствует переход атома из состояния с энергией 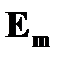 в состояние с энергией в состояние с энергией 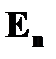 . На диаграмме этот переход обозначается вертикальной стрелкой от уровня . На диаграмме этот переход обозначается вертикальной стрелкой от уровня 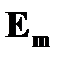 к уровню к уровню 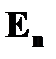 . . | |
| Излучение и поглощение энергии атомом | ➨ при переходе электрона с орбиты 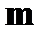 на более близкую к ядру орбиту на более близкую к ядру орбиту  в соответствии с третьим постулатом Бора испускается энергия: в соответствии с третьим постулатом Бора испускается энергия: 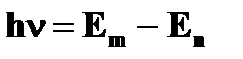 = =  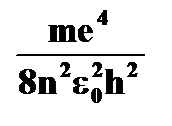 - - 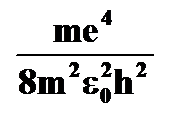 = = 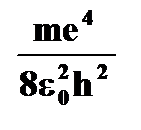 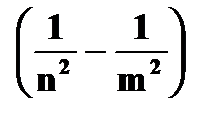  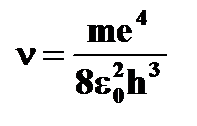 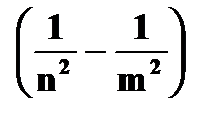 | |
· частота излучения 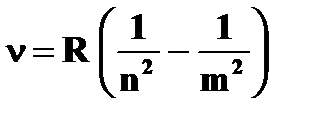 | |
· длина волны излучения 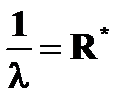 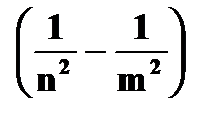 | ➨ т.к. 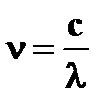 , то , то 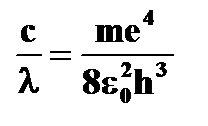 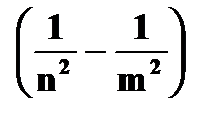 или или 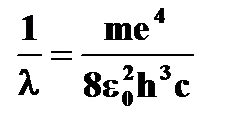 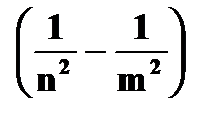 | |
| · постоянная Ридберга | ➨ 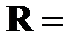 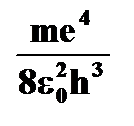 = 3,29×1015 с-1 = 3,29×1015 с-1 | |
➨ 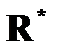 = =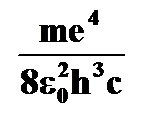 = 1,097×107 м-1 или = 1,097×107 м-1 или 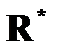 = = 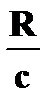 | |
| Линейчатые спектры испускания и поглощения атома | ➨ линейчатые спектры были экспериментальной основой третьего постулата Бора и объясняются излучением или пог-лощением атомом энергии при переходе электрона с одной стационарной орбиты на другую. Атомные спектры наблюдаются в инфракрасной, видимой и ультрафиолетовой областях спектра. Каждый химический элемент имеет индивидуальный линейчатый спектр атома. | |
| · линейчатый спектр испускания атома водорода | ➨ опытным путем было установлено, что при свечении во-дорода в газосветной трубке 1 и пропускании узкого пучка излучения через призму 2, на экране 3 отображается линей-чатый спектр излучения энергии водородом, состоящий из нескольких светлых линий на темном фоне. | |
| · линейчатый спектр поглощения атома водорода | ➨ если свет от источника 7 пропустить через трубку 6, наполненную водородом и призму 5, то на экране 4отображается линейчатый спектр поглощения энергии водородом, состоящий из нескольких темных линий на светлом фоне. | |
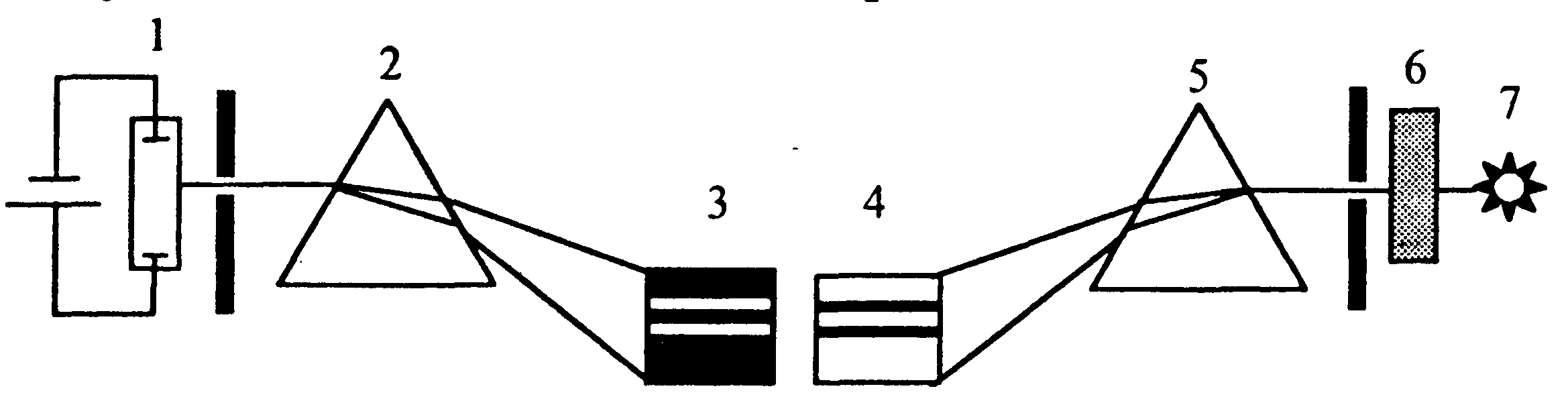 При равных температурах газа в трубках 1 и 6положения тем-ных линий в спектре испускания атома водорода совпадают с положениями светлых линий в спектре поглощения атома. При равных температурах газа в трубках 1 и 6положения тем-ных линий в спектре испускания атома водорода совпадают с положениями светлых линий в спектре поглощения атома. | |
| · закономерности в спектре излучения водорода | ➨ спектр излучения атомарного водорода состоит из отдельных спектральных линий, образующих пять спектральных серий. Длины волн спектральных линий, входящих в каждую серию, подчиняются закономерности, выражаемой формулой Бальмера. | |
· формула Бальмера 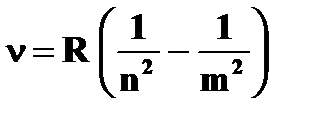 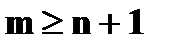 | ➨  - номер энергетического уровня, на который перешел электрон; - номер энергетического уровня, на который перешел электрон; 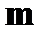 - номер энергетического уровня, с которого пришел электрон; - номер энергетического уровня, с которого пришел электрон; | |
| Спектральные серии атома водорода | ➨ подставляя для 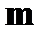 и и  значения 1,2,3… можно получить все частоты (длины) волн спектра водорода. значения 1,2,3… можно получить все частоты (длины) волн спектра водорода. | |
| | · серия Лаймана: | ➨ 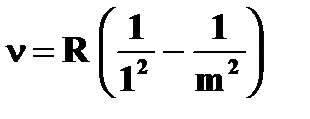 , , 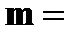 2,3,4,… 2,3,4,… | 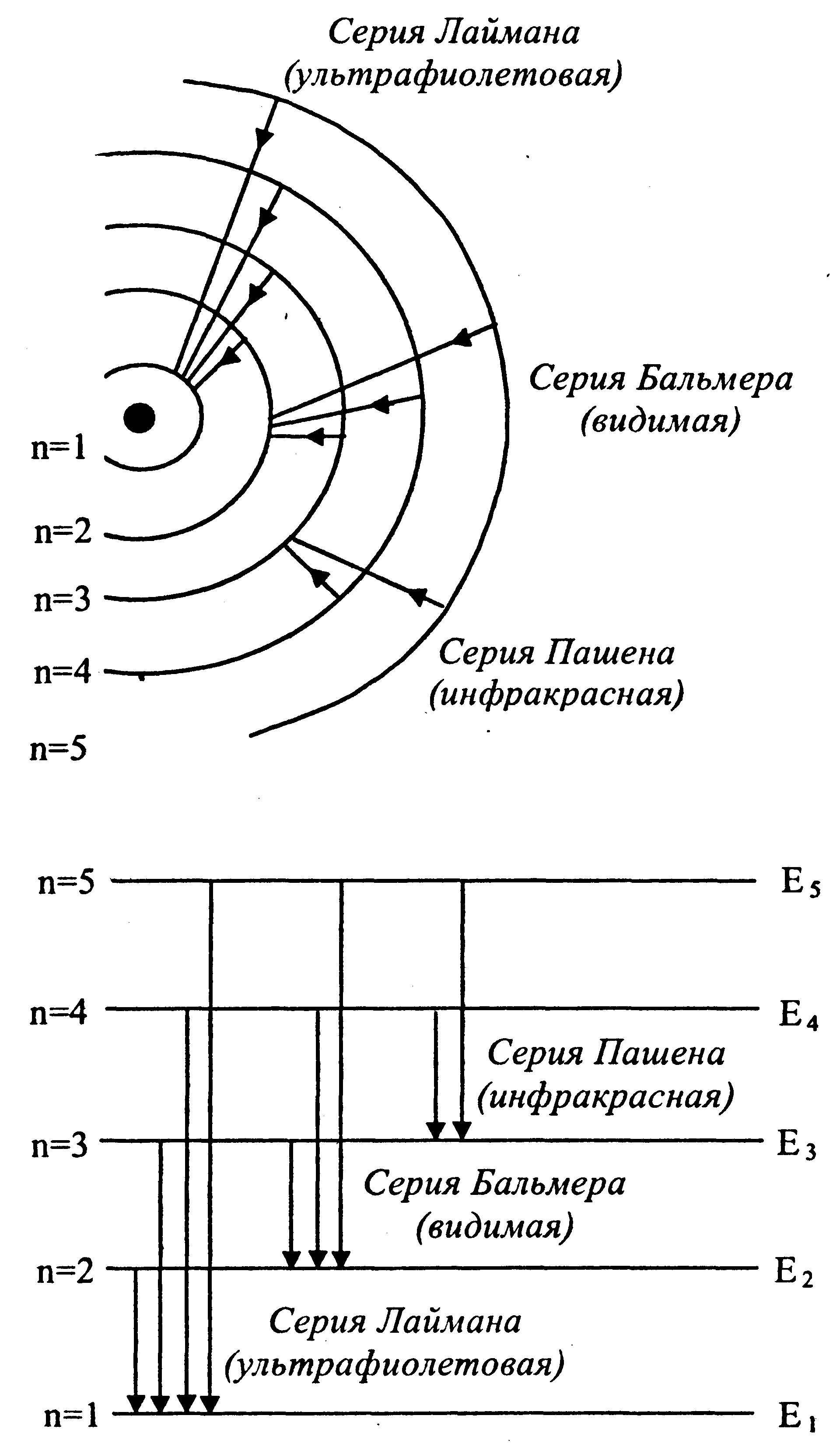 | |
| · серия Бальмера: | ➨ 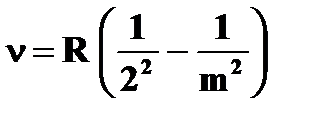 , , 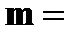 3,4,5,… 3,4,5,… | |
| · серия Пашена: | ➨ 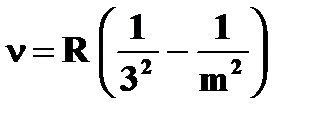 , , 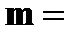 4,5,6,… 4,5,6,… | |
| · серия Брэкета: | ➨ 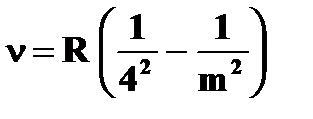 , , 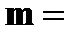 5,6,7,… 5,6,7,… | |
| · серия Пфунда: | ➨ 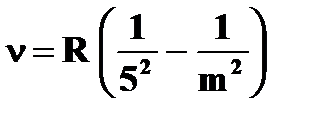 , , 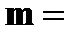 6,7,8,… 6,7,8,… | |
| Спектры | ➨ различают спектры испускания и поглощения. | |
| · спектры испускания | ➨ возникают от раскаленных тел. Делятся на: сплошные, линейчатые, полосатые. | |
сплошной (непрерывный ) спектр  | ➨ испускают раскаленные твердые и жидкие тела, а также газы, находящиеся под достаточно большим давлением. Такой спектр можно получить, пропуская солнечный свет через трехгранную призму. | |
| линейчатый спектр | 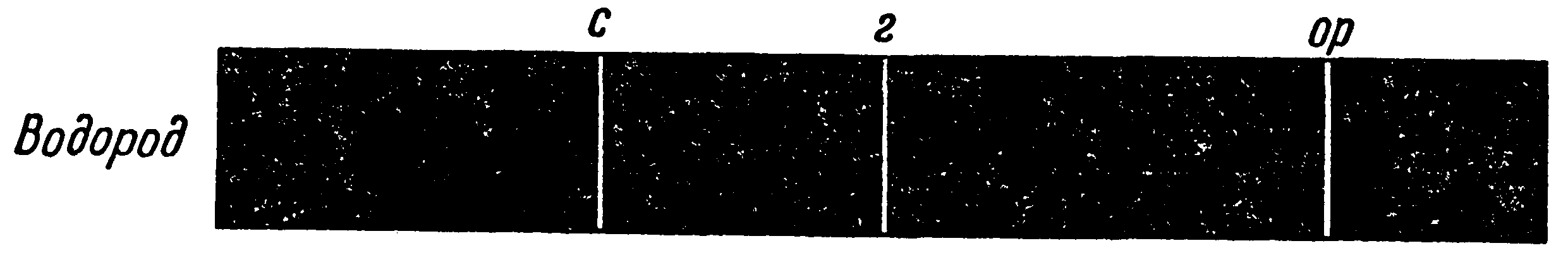 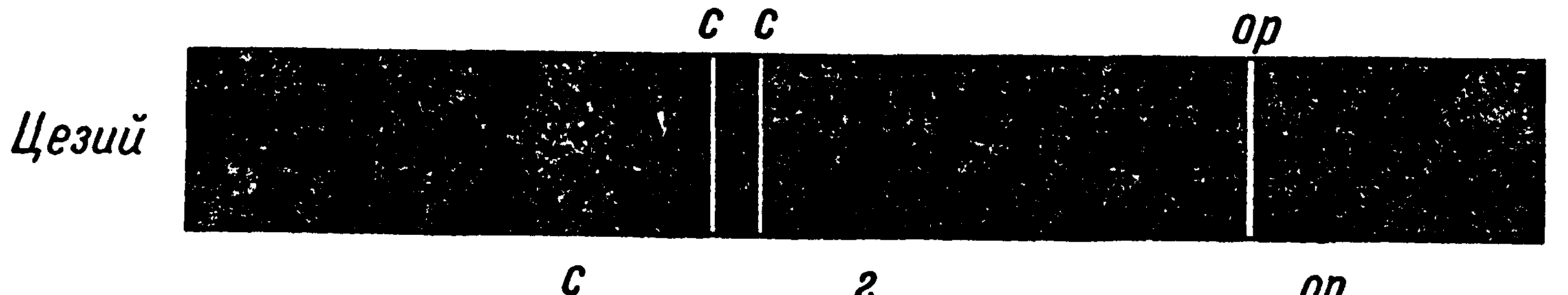 ➨ испускается раскаленными газами, имеющими атомарную структуру и находящимися под сравнительно небольшим давлением. Атомы разных элементов испускают различные частоты. Это используется для спектрального анализа. ➨ испускается раскаленными газами, имеющими атомарную структуру и находящимися под сравнительно небольшим давлением. Атомы разных элементов испускают различные частоты. Это используется для спектрального анализа. | |
| полосатый спектр | ➨ дают различные молекулярные соединения. Полосы образуются вследствие взаимодействия молекул вещества. | |
| · спектры поглощения | ➨ получаются при пропускании лучей сплошного спектра (от раскаленного источника) через менее нагретый газ. Тогда на фоне сплошного спектра наблюдаются узкие темные линии поглощения. | |
| · закон Кирхгофа для спектров поглощения | ➨ линии поглощения соответствуют линиям испускания, т.е. атомы менее нагретого элемента поглощают из сплошного спектра как раз те частоты, которые они в других условиях испускают. Следовательно, по спектру поглощения тоже можно судить о химическом составе поглощающего соединения. | |
| Спектральный анализ | ➨ метод определения качественного и количественного сос-тава вещества по его спектру. Имеет существенные преимущества перед химическим анализом, т.к. быстр, надежен, чувствителен (несколько десят-ков атомов в соединении уже дают характерные линии), точен. Спектральный анализ позволяет определить химический состав, температуру и скорость движения небесных тел, удаленных от Земли на расстояния в миллиарды световых лет. | |
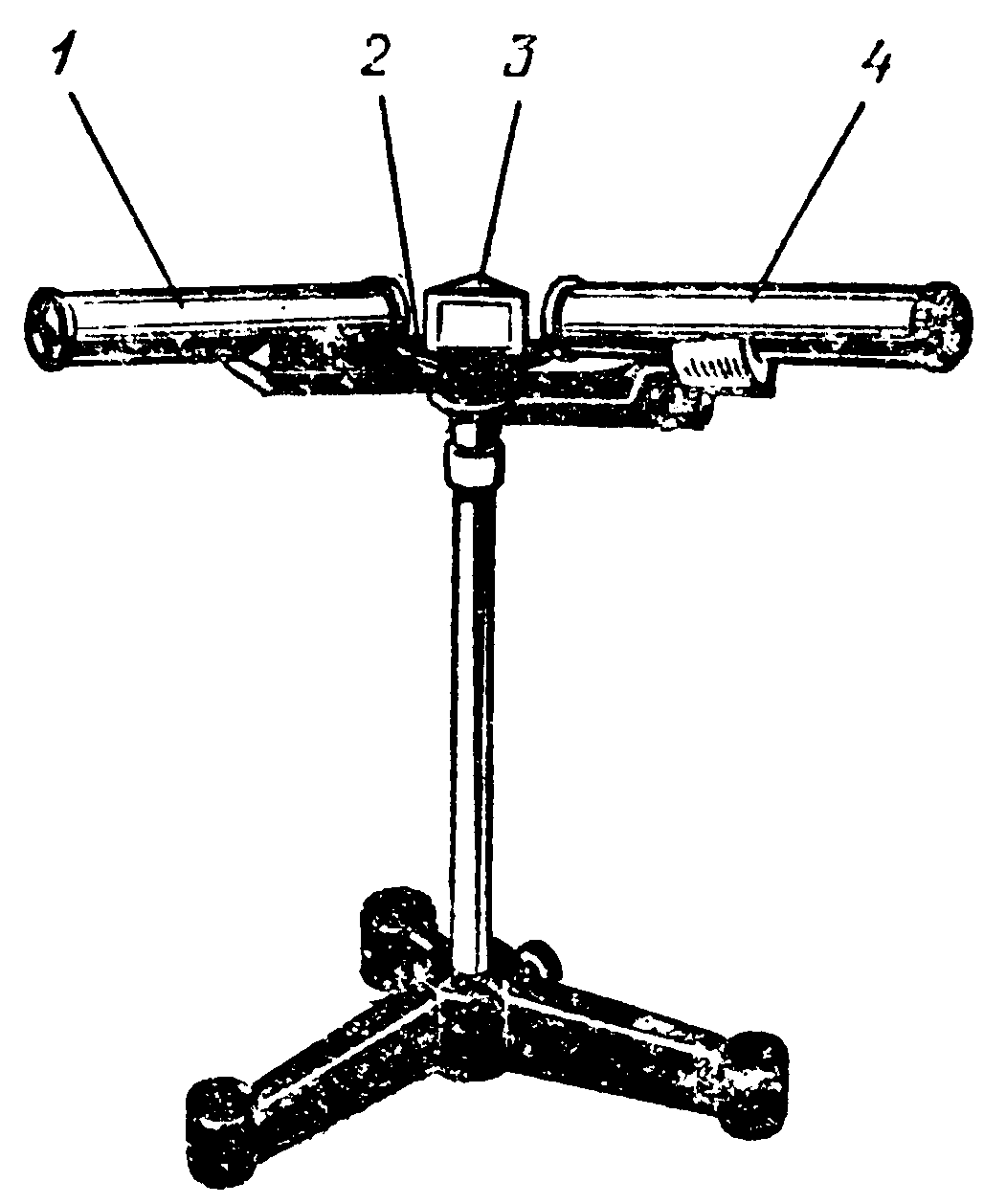 · спектроскоп · спектроскоп | ➨ прибор для разложения сложного света и наблюдения спектров. Состоит из двух труб – коллиматорной 1 и зрительной 4, укрепленных на подставке 2 и стеклянной призмы 3под крышкой. Параллельный пучок света, выходящий из коллиматора, попадает на грань стеклянной призмы. Показатель преломления света зависит от его длины волны, поэтому пучок света, состоящий из волн с разной длиной волны, разлагается на параллельные пучки света разного цвета. Линза зрительной трубы фиксирует каждый пучок и дает разноцветные изображения щели, образуя разноцветную полоску – спектр. | |
| Люминесценция | ➨ свечение веществ, не вызываемое нагреванием тела. | |
| · условия возникновения люминесценции | ➨ возникает при переходе электрона в атоме с более уда-ленной орбиты на более близкую к ядру орбиту. Спектр люминесценции содержит линии с определенной длиной волны и зависит от структуры данного атома. Атом ис-пускает излучение в том случае, если он находится в воз-бужденном состоянии, т.е. если электроны предваритель-но переведены на более высокие орбиты. | |
| · виды люминесценции: | ➨ различаются по способу ее возбуждения. | |
| - электролюминесценция | ➨ возникает при электрическом возбуждении; | |
| - хемолюминесценция | ➨ сопровождает процессы гниения; | |
| - флуорисценция | ➨возбуждается коротковолновым электромагнитным излуче-нием или потоком частиц (электронов, протонов, 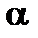 -частиц). -частиц). | |
| - фосфоресценция | ➨флуорисценция в виде зависящего от температуры после-свечения, возникающего после прекращения облучения. | |
| Лазер (оптический квантовый генератор) | ➨ устройство, генерирующее монохроматические когерентные электромагнитные волны за счет вынужденного излучения активной среды (вещества). Первый квантовый генератор был создан в 1954 г. русскими физиками Прохоровым и Басовым и независимо от них американским физиком Таунсом. Первый лазер был создан в 1960 г. американским ученым Мейманом. | |
| | |
| · монохроматическое излучение | ➨ электромагнитные колебания одной частоты. | |
| · когерентное излучение | ➨ электромагнитные колебания, происходящие в одной фазе или если разность фаз колебаний остается постоянной во времени. | |
| · спонтанное (самопроизвольное) излучение | ➨ испускание атомом кванта  электромагнитного излучения (фотона) в результате самопроизвольного (спонтанного) перехода электрона электромагнитного излучения (фотона) в результате самопроизвольного (спонтанного) перехода электрона 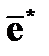 из возбужденного состояния в основное из возбужденного состояния в основное 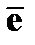 (невозбужденное). (невозбужденное). | |
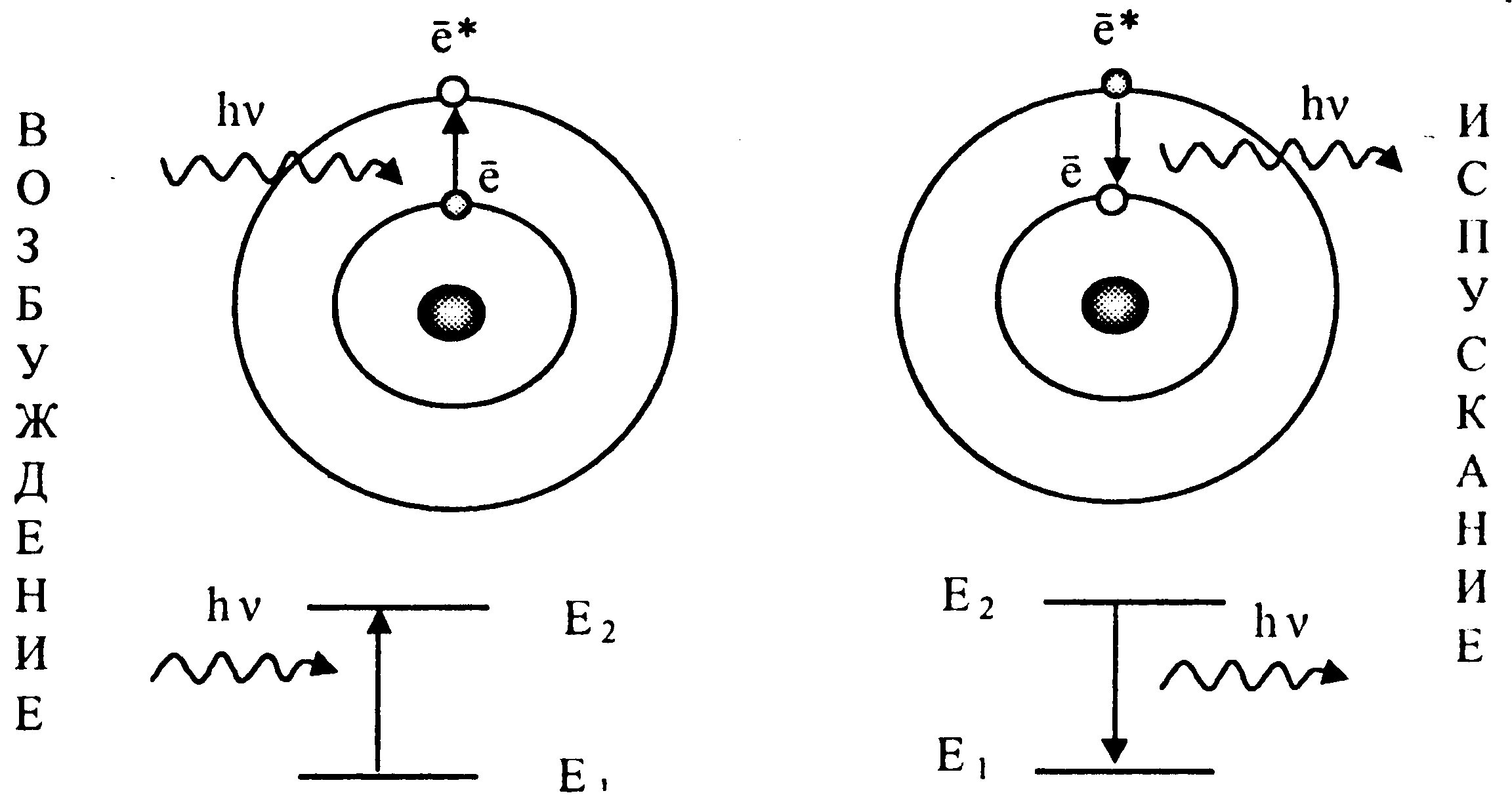 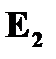 - энергия электрона в возбужденном состоянии; - энергия электрона в возбужденном состоянии; 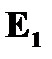 -энергия электрона в основном (невозбужденном) состоянии -энергия электрона в основном (невозбужденном) состоянии | |
| · индуцированное (вынужденное) излучение | ➨ переход электрона 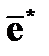 из возбужденного состояния в основное из возбужденного состояния в основное 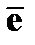 под воздействием электромагнитного излучения ( в результате стимуляции фотоном с энергией под воздействием электромагнитного излучения ( в результате стимуляции фотоном с энергией  ). ). | |
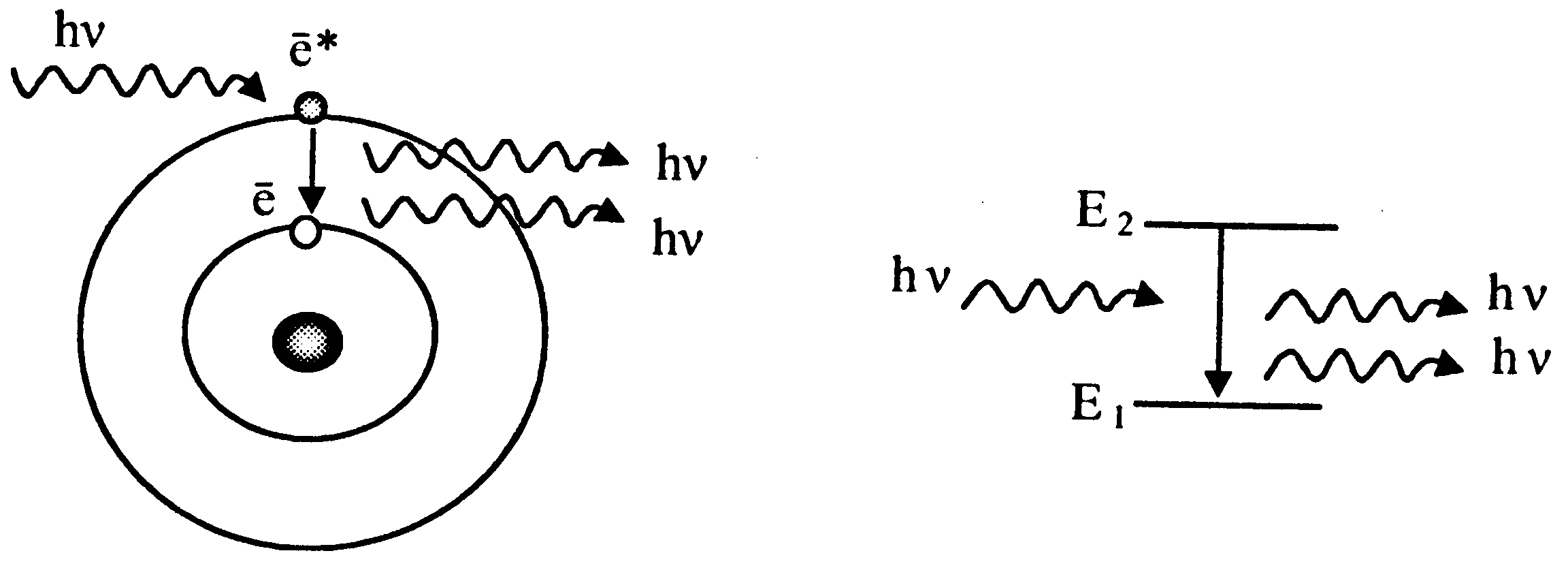 Фотон-«катализатор» попадает в возбужденный электрон и, стимулируя его переход в основное состояние, не теряет сво-ей энергии. Из атома испускаются два фотона с энергией Фотон-«катализатор» попадает в возбужденный электрон и, стимулируя его переход в основное состояние, не теряет сво-ей энергии. Из атома испускаются два фотона с энергией  . . | |
| · метастабильный энергетический уровень | ➨ энергетический уровень, на котором среднее время жизни возбужденного электрона 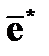 много больше времени жизни этого электрона на других энергетических уровнях. много больше времени жизни этого электрона на других энергетических уровнях. | |
| · среднее время жизни электрона | ➨ среднее время пре-бывания электрона на данном энергетичес-ком уровне. | 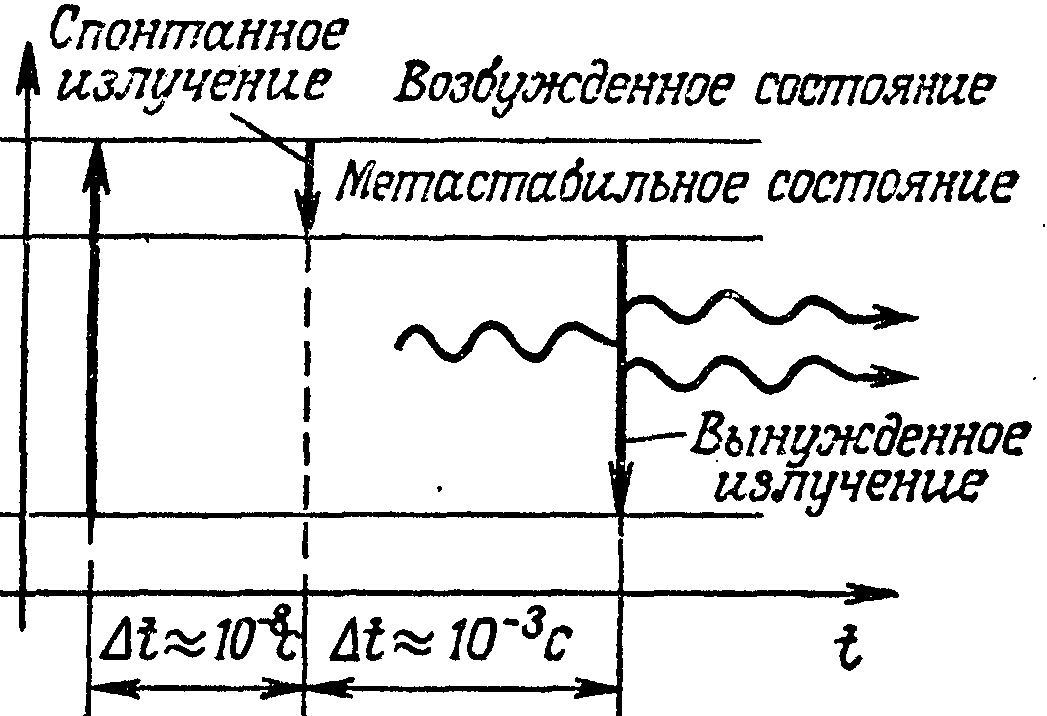 Е Е | |
| · нормальная заселенность | ➨ состояние системы, при котором число атомов в основном состоянии 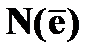 больше, чем их число в возбужденных состояниях больше, чем их число в возбужденных состояниях 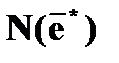 : : 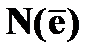  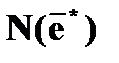 | |
| · инверсная заселенность | ➨ состояние системы, при котором число атомов в возбужденных состояниях 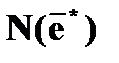 больше, чем их число в основном состоянии больше, чем их число в основном состоянии 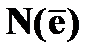 : : 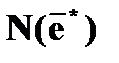  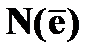 | |
| Основные компоненты лазера | ➨ 1) активная среда (в ней создаются состояния с инверсной заселенностью); 2) система накачки(устройство для создания инверсии в активной среде); 3) оптический резонатор(устройство, выделяющее в пространство избирательное направление пучка фотонов и формирующее выходящий световой пучок). | |
| | |
| · активная среда | ➨ среда, при прохождении которой падающий пучок света усиливается. Если в среде создается состояние с инверсной заселеннос-тью, то вынужденное излучение может превосходить погло-щение света атомами и падающий пучок при прохождении через вещество будет усиливаться. Интенсивность электро-магнитной волны, проходящей через активную среду, увели-чивается за счет актов вынужденного излучения. Активная среда лазера может быть твердая (рубин), жидкая (органические красители) и газообразная (гелий+неон). | |
| · накачка | ➨ процесс создания неравновесного состояния вещества, т.е. перевод системы в состояние с инверсной заселенностью. | |
| Классификация лазеров | ➨ лазеры делятся: 1) по типу активной среды (твердотельные, газовые полупроводниковые, жидкостные); 2) по методам накачки (оптические, тепловые, хими-ческие, электроионизационные и др.); 3) по режиму генерации (непрерывного или импуль-сного действия). | |
| | |
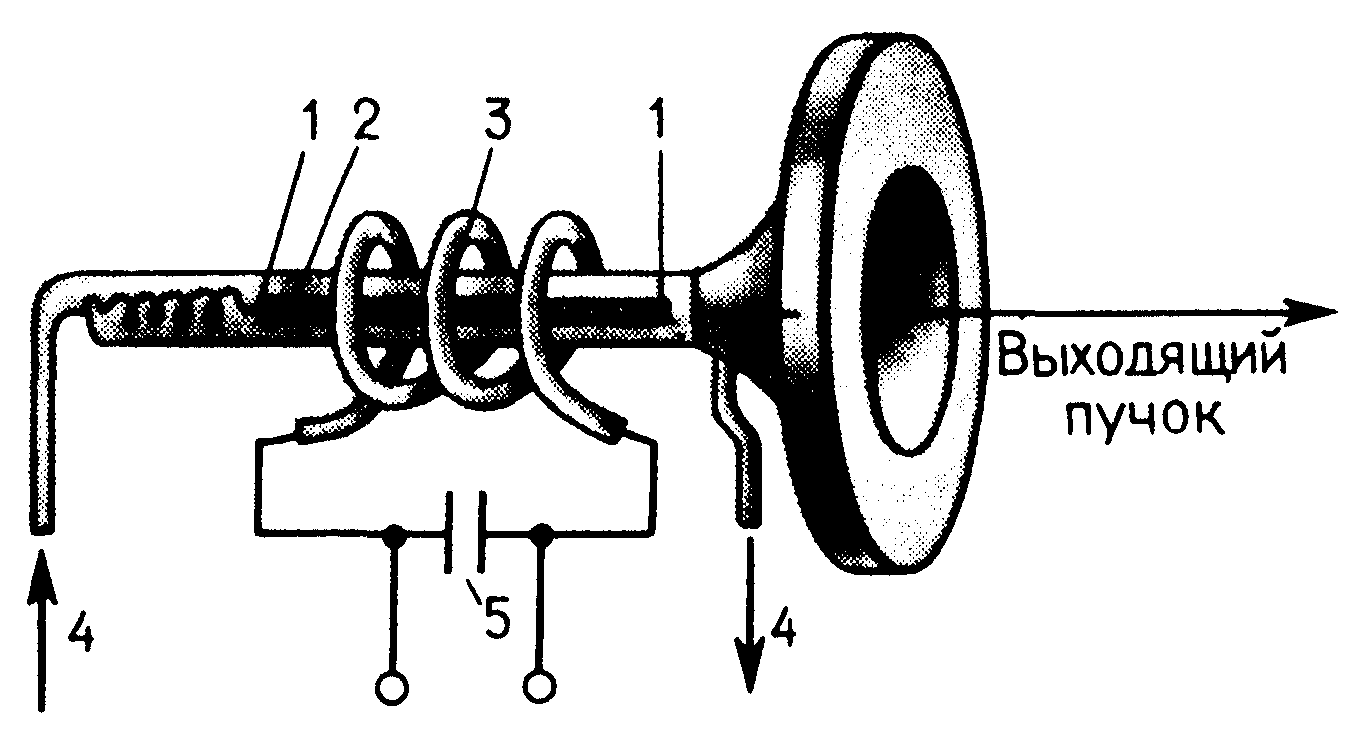
| Устройство рубинового лазера | ➨ рубиновый стержень 2 представляет собой цилиндр, длина которого в 8-10 раз превышает его диаметр. Система зеркал 1 состоит из двух строго параллель-ных друг другу плоских зеркал, расположенных возле торцов рубинового стержня. Она нужна для того, чтобы заставить световой пучок многократно проходить через рубиновый стержень. Одно из зеркал полностью отражает свет, а другое полупрозрачно, т.е. частично отражает, а частично пропускает свет. Газоразрядная лампа 3 имеет вид спирали и охваты-вает рубиновый стержень. При ее зажигании от разряда батареи конденсаторов 5 лампа дает яркую вспышку. Ее используют для возбуждения ионов хрома в рубине (лампа накачки). Система охлаждения 4 нужна для охлаждения рубинового стержня, нагревающегося при работе лазера. | |
 | |
| Принцип работы рубинового лазера | ➨ рассмотрим принцип действия первого твердотельного лазера (Мейман,1960 г.). В качестве активной среды исполь-зуется кристалл рубина (оксид алюминия 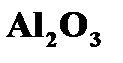 ), инверсная заселенность осуществляется по трехуровневой схеме (Басов, Прохоров, 1955 г.). В кристаллической решетке оксида алю-миния часть атомов ), инверсная заселенность осуществляется по трехуровневой схеме (Басов, Прохоров, 1955 г.). В кристаллической решетке оксида алю-миния часть атомов  заменена ионами заменена ионами 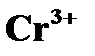 , которые участвуют в генерации лазерного излучения. , которые участвуют в генерации лазерного излучения. | |
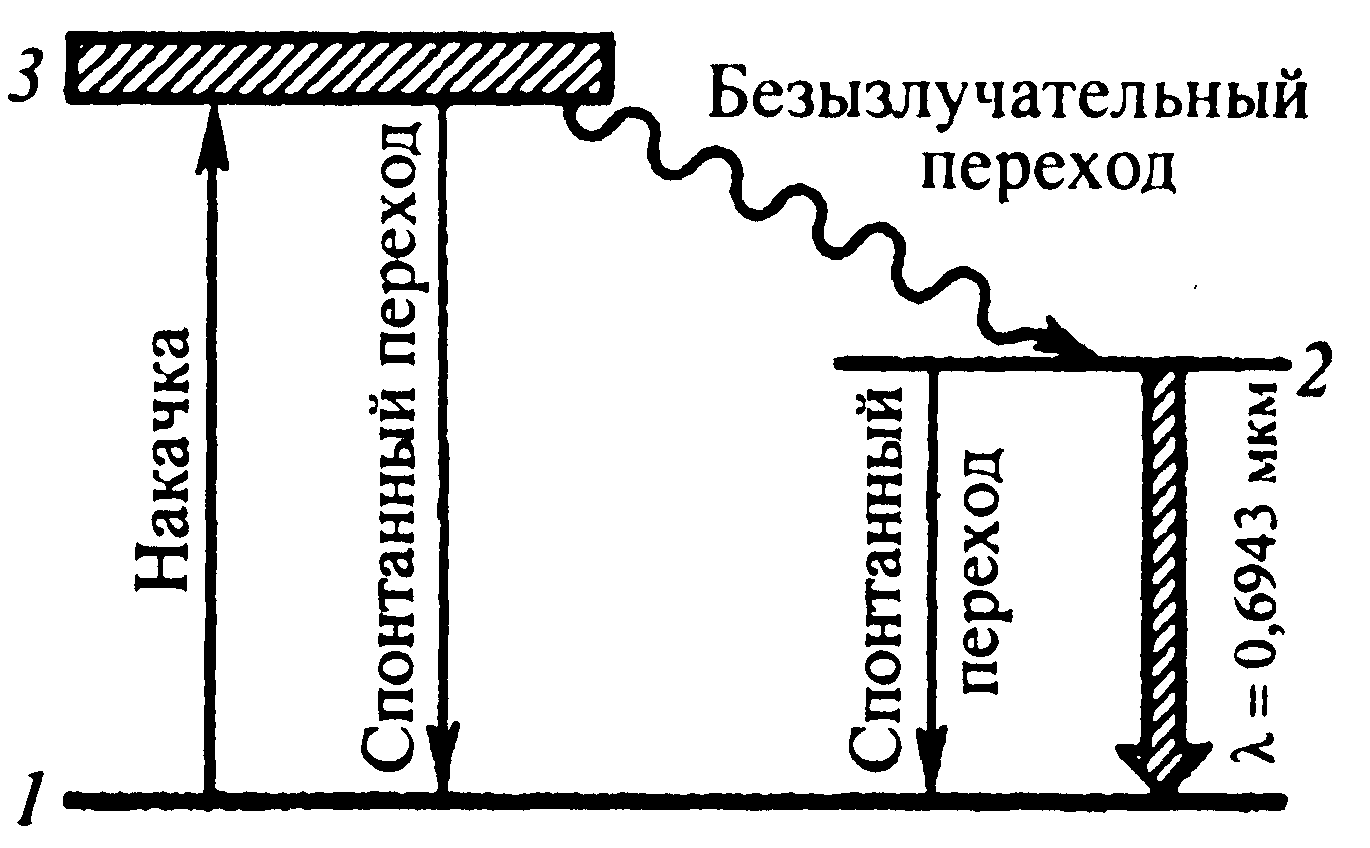 | |
| ➨ при облучении рубина сине-зеленым светом (с помо-щью лампы-вспышки) ионы хрома возбуждаются и из ос-новного стационарного состояния (энергетический уро-вень 1) переходят в возбужденное состояние (уровень 3). Через короткий промежуток времени ~10-8 с большинство ионов хрома самопроизвольно (спонтанно) переходят с энергетического уровня 3 на метастабильный энергети-ческий уровень 2, в котором они могут находиться около 10-3с (т.е. в 100 тыс. раз дольше, чем на обычном возбуж-денном уровне). Таким образом создается «перенаселен-ность» метастабильного уровня 2 (т.е. число возбуж-денных атомов больше числа невозбужденных). Важно то, что переход ионов с энергетического уровня 3 на метастабильный уровень 2 происходит без излучения света (высвобождающаяся при таком переходе энергия передается кристаллической решетке рубина). Под действием электромагнитных вол, облучающих рабочее вещество (рубин), или же под действием фотонов, появляющихся в самом веществе при спонтанных переходах атомов на уровень 2, происходит переход ионов хрома с метастабильного уровня 2 на уровень 1 и возникает вынужденное излучение света. | |
| Свойства лазерного излучения | ➨ 1) временная и пространственная когерентность; 2) строгая монохроматичность ( 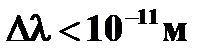 ); 3) большая плотность потока энергии; 4) очень малое угловое расхождение в пучке. ); 3) большая плотность потока энергии; 4) очень малое угловое расхождение в пучке. | |
| Применение лазеров | ➨ ·лазерные излучения используют для передачи информа-ции; для связи, особенно в космосе; для точного определе-ния расстояний; ·лазеры используют для трассировки туннелей, для геоде-дезических измерений, для определения курса и скорости кораблей, самолетов, ракет; ·лазеры используют в голографии для получения объемных изображений предметов; ·с помощью лазеров производят точечную сварку, изго-тавливают микросхемы; ·в медицине главной областью применения лазеров явля-ется хирургия, лазерные пучки используют для разрезания, сшивания и стерилизации живых тканей, для приваривания отслоившейся сетчатки глаза; ·с помощью лазерного излучения можно вызывать химии-ческие реакции, которые не происходят в обычных условиях; ·мощные лазерные пучки используются для осуществления управляемых термоядерных реакций. | |
| | | | | | | | |

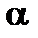 -частиц
-частиц 
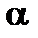 -частиц, пришел к выводу о несостоятельности мо-дели атома Томсона. Для изучения строения атома Резерфорд предложил зон-дирование атома с помощью
-частиц, пришел к выводу о несостоятельности мо-дели атома Томсона. Для изучения строения атома Резерфорд предложил зон-дирование атома с помощью 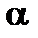 -частиц, которые испускались источником 1, помещенным внутри свинцовой полости, поглощающей все
-частиц, которые испускались источником 1, помещенным внутри свинцовой полости, поглощающей все 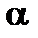 -частицы, кроме проходящих через ка-нал 2. Узкий пучок
-частицы, кроме проходящих через ка-нал 2. Узкий пучок 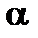 -частиц попадал на фольгу из золота 3. Рассеянные после взаимодействия с атомами золота
-частиц попадал на фольгу из золота 3. Рассеянные после взаимодействия с атомами золота 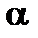 -час-тицы регистрировались под разными углами
-час-тицы регистрировались под разными углами  визуально с помощью светочувствительного экрана и микроскопа 4. Угол отклонения некоторых частиц
визуально с помощью светочувствительного экрана и микроскопа 4. Угол отклонения некоторых частиц  =1800 мог быть то-лько при лобовом столкновении положительно заряженной
=1800 мог быть то-лько при лобовом столкновении положительно заряженной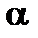 -частицы с положительно заряженным уплотнением в атоме. Резерфорд назвал его «ядро атома» и предложил в 1911 г. планетарную модель строения атома.
-частицы с положительно заряженным уплотнением в атоме. Резерфорд назвал его «ядро атома» и предложил в 1911 г. планетарную модель строения атома. 
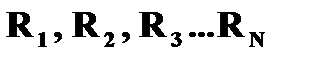 . Находясь на стаци-онарной орбите, электрон не излучает энергии.
. Находясь на стаци-онарной орбите, электрон не излучает энергии. 
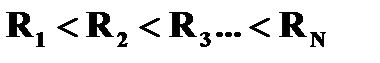 соответ-ствует строго определенная энергия
соответ-ствует строго определенная энергия 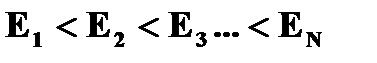 . Двигаясь по круговым орбитам электроны обладают квантованными значениями момента импульса:
. Двигаясь по круговым орбитам электроны обладают квантованными значениями момента импульса: 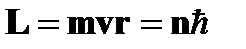 (
(  =1,2,3…) Квантованные значения – определенные дискретные значения, целые кратные постоянной Планка -
=1,2,3…) Квантованные значения – определенные дискретные значения, целые кратные постоянной Планка - 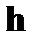 =6,63×10-34 Дж×с или
=6,63×10-34 Дж×с или 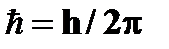 = 1,054×10-34 Дж×с.
= 1,054×10-34 Дж×с. 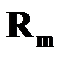 на другую
на другую 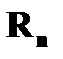 ; при этом излучается или поглощается квант световой энергии (фотон). Энергия фотона равна разности энергий электрона
; при этом излучается или поглощается квант световой энергии (фотон). Энергия фотона равна разности энергий электрона 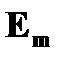 и
и 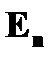 на соответствующих стационарных орбитах
на соответствующих стационарных орбитах 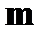 и
и  :
: 
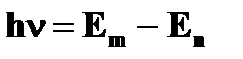 , где
, где  - частота фотона.
- частота фотона. 
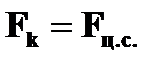
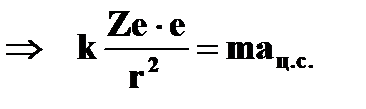
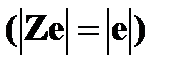
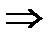
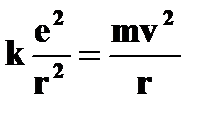
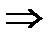
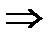
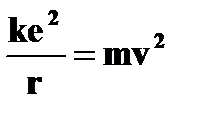 (или
(или 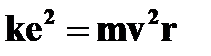 , или
, или 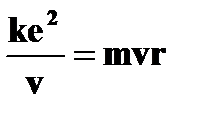 , но
, но 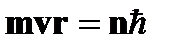 )
) 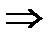
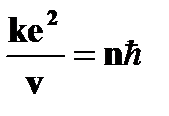
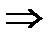
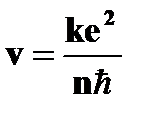 , где
, где 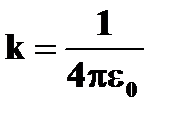 . Так как
. Так как  =1,2,3…, то можно вычислить радиусы первой, второй и всех последующих стационарных круговых орбит электронов в атоме.
=1,2,3…, то можно вычислить радиусы первой, второй и всех последующих стационарных круговых орбит электронов в атоме. 
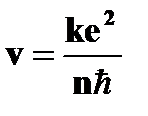
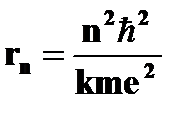
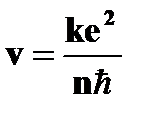
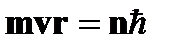
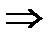
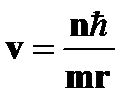 ,
, 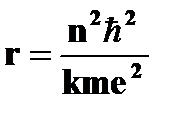 ,где
,где  =1,2,3…;
=1,2,3…; 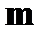 - масса электрона.
- масса электрона. 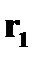 = 0,528×10-10м
= 0,528×10-10м  =1. Первый боровский радиус служит единицей длины в атомной физике.
=1. Первый боровский радиус служит единицей длины в атомной физике. 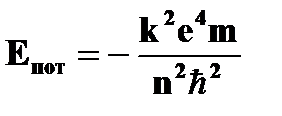 =
= 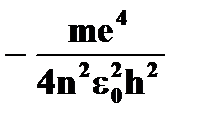
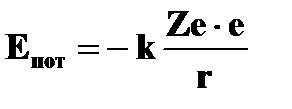 -потенциальная энергия системы двух зарядов (ядра и электрона);
-потенциальная энергия системы двух зарядов (ядра и электрона); 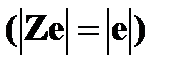
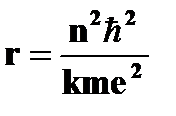 ;
; 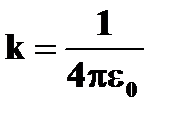 ;
; 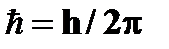 ; (
; (  =1,2,3…).
=1,2,3…). 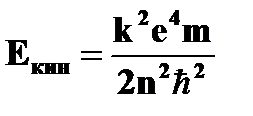 =
= 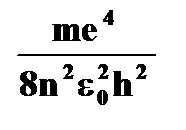
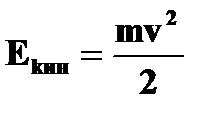 ,
, 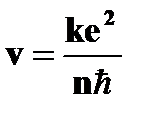 ,
, 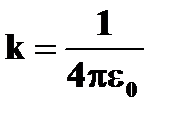 ,
, 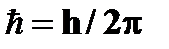 ; (
; (  =1,2,3…). ➨ кинетическая энергия электрона на любой орбите составляет половину его потенциальной энергии:
=1,2,3…). ➨ кинетическая энергия электрона на любой орбите составляет половину его потенциальной энергии: 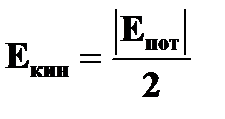
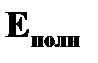 =
= 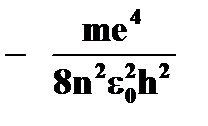
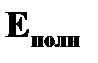 ~
~ 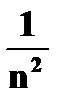
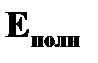 =
= 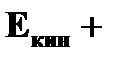
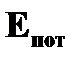 =
= 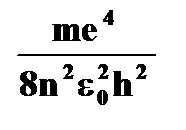
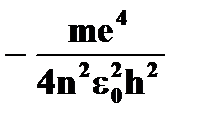
 (приводим к общему знаменателю)
(приводим к общему знаменателю) 
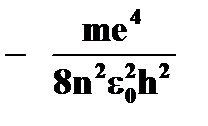 . После подстановки численных данных постоянных получаем:
. После подстановки численных данных постоянных получаем: 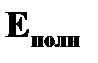 =
= 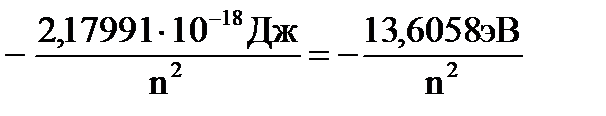 , т.е. полная энергия электрона на орбите обратно пропорциональна квадрату порядкового номера орбиты.
, т.е. полная энергия электрона на орбите обратно пропорциональна квадрату порядкового номера орбиты. 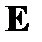 [Дж], [эВ]
[Дж], [эВ]  диаграммы
диаграммы 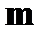 на стационарную орбиту под номером
на стационарную орбиту под номером  соответствует переход атома из состояния с энергией
соответствует переход атома из состояния с энергией 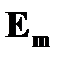 в состояние с энергией
в состояние с энергией 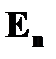 . На диаграмме этот переход обозначается вертикальной стрелкой от уровня
. На диаграмме этот переход обозначается вертикальной стрелкой от уровня 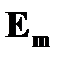 к уровню
к уровню 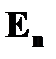 .
. 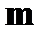 на более близкую к ядру орбиту
на более близкую к ядру орбиту  в соответствии с третьим постулатом Бора испускается энергия:
в соответствии с третьим постулатом Бора испускается энергия: 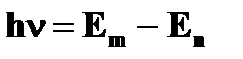 =
= 
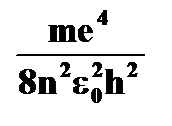 -
- 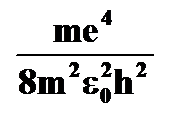 =
= 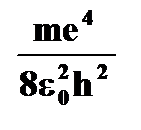
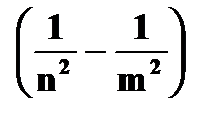
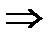
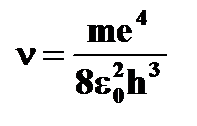
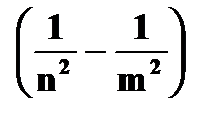
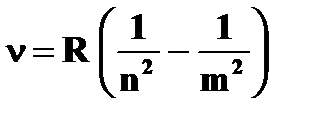
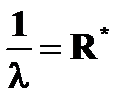
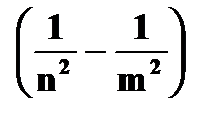
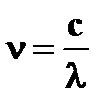 , то
, то 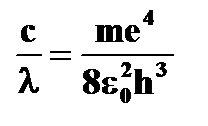
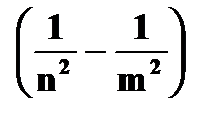 или
или 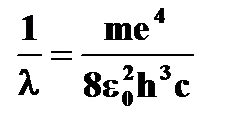
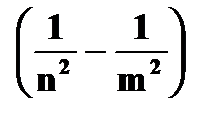
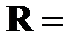
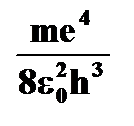 = 3,29×1015 с-1
= 3,29×1015 с-1 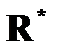 =
=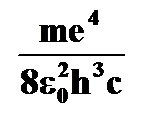 = 1,097×107 м-1 или
= 1,097×107 м-1 или 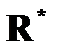 =
= 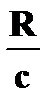
 При равных температурах газа в трубках 1 и 6положения тем-ных линий в спектре испускания атома водорода совпадают с положениями светлых линий в спектре поглощения атома.
При равных температурах газа в трубках 1 и 6положения тем-ных линий в спектре испускания атома водорода совпадают с положениями светлых линий в спектре поглощения атома. 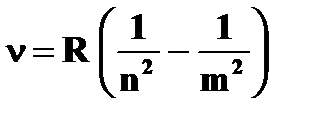
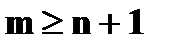
 - номер энергетического уровня, на который перешел электрон;
- номер энергетического уровня, на который перешел электрон; 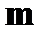 - номер энергетического уровня, с которого пришел электрон;
- номер энергетического уровня, с которого пришел электрон; 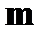 и
и  значения 1,2,3… можно получить все частоты (длины) волн спектра водорода.
значения 1,2,3… можно получить все частоты (длины) волн спектра водорода. 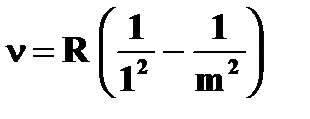 ,
, 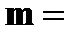 2,3,4,…
2,3,4,… 
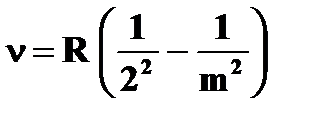 ,
, 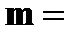 3,4,5,…
3,4,5,… 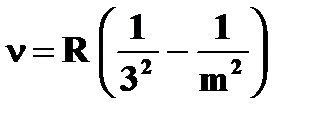 ,
, 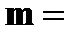 4,5,6,…
4,5,6,… 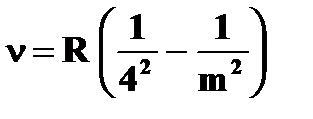 ,
, 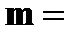 5,6,7,…
5,6,7,… 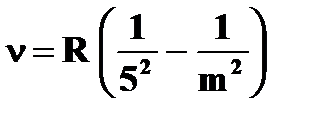 ,
, 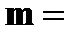 6,7,8,…
6,7,8,… 

 ➨ испускается раскаленными газами, имеющими атомарную структуру и находящимися под сравнительно небольшим давлением. Атомы разных элементов испускают различные частоты. Это используется для спектрального анализа.
➨ испускается раскаленными газами, имеющими атомарную структуру и находящимися под сравнительно небольшим давлением. Атомы разных элементов испускают различные частоты. Это используется для спектрального анализа.  · спектроскоп
· спектроскоп 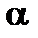 -частиц).
-частиц).  электромагнитного излучения (фотона) в результате самопроизвольного (спонтанного) перехода электрона
электромагнитного излучения (фотона) в результате самопроизвольного (спонтанного) перехода электрона 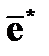 из возбужденного состояния в основное
из возбужденного состояния в основное 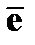 (невозбужденное).
(невозбужденное). 
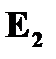 - энергия электрона в возбужденном состоянии;
- энергия электрона в возбужденном состоянии; 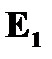 -энергия электрона в основном (невозбужденном) состоянии
-энергия электрона в основном (невозбужденном) состоянии 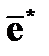 из возбужденного состояния в основное
из возбужденного состояния в основное 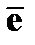 под воздействием электромагнитного излучения ( в результате стимуляции фотоном с энергией
под воздействием электромагнитного излучения ( в результате стимуляции фотоном с энергией  ).
). 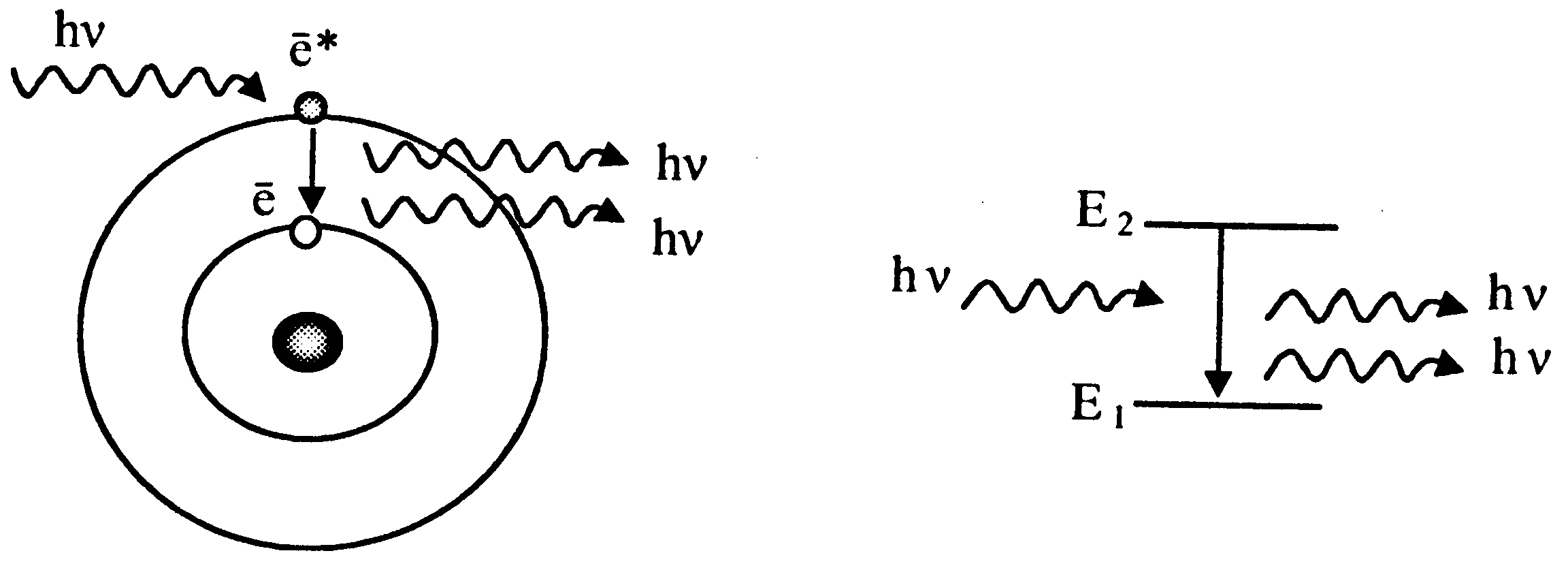 Фотон-«катализатор» попадает в возбужденный электрон и, стимулируя его переход в основное состояние, не теряет сво-ей энергии. Из атома испускаются два фотона с энергией
Фотон-«катализатор» попадает в возбужденный электрон и, стимулируя его переход в основное состояние, не теряет сво-ей энергии. Из атома испускаются два фотона с энергией  .
. 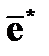 много больше времени жизни этого электрона на других энергетических уровнях.
много больше времени жизни этого электрона на других энергетических уровнях.  Е
Е 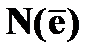 больше, чем их число в возбужденных состояниях
больше, чем их число в возбужденных состояниях 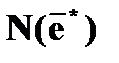 :
: 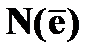

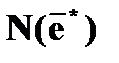
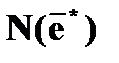 больше, чем их число в основном состоянии
больше, чем их число в основном состоянии 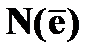 :
: 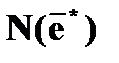

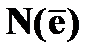

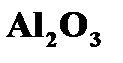 ), инверсная заселенность осуществляется по трехуровневой схеме (Басов, Прохоров, 1955 г.). В кристаллической решетке оксида алю-миния часть атомов
), инверсная заселенность осуществляется по трехуровневой схеме (Басов, Прохоров, 1955 г.). В кристаллической решетке оксида алю-миния часть атомов  заменена ионами
заменена ионами 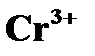 , которые участвуют в генерации лазерного излучения.
, которые участвуют в генерации лазерного излучения. 
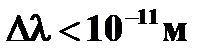 ); 3) большая плотность потока энергии; 4) очень малое угловое расхождение в пучке.
); 3) большая плотность потока энергии; 4) очень малое угловое расхождение в пучке. 