Задачи и упражнения для самостоятельного решения. 30.1. Сколько кубических метров СО2 (условия нормальные) можно получить из 1 т известняка, содержащего 95 % СаСО3?
30.1. Сколько кубических метров СО2 (условия нормальные) можно получить из 1 т известняка, содержащего 95 % СаСО3? (Ответ: 212,8 м3).
30.2. Вычислить объем одного моля эквивалентов СО2 в реакции С + О2 = СО2 при нормальных условиях. (Ответ: 5,6 л).
30.3. Составить уравнения реакций взаимодействия: а) NaHCO3 и HCl;
б) NaHCO3 и NaOH; в) Ca(HCO3)2 и NaOH; г) Ca(HCO3)2 и Ca(OH)2.
30.4. Какие типы гибридизации АО характерны для углерода? Описать с позиций метода ВС строение молекул СН4, С2Н4, С2Н2.
30.5. Карбид кальция получают по схеме: СаО + 3С → СаС2 + СО. Вычислить массу СаО, необходимую для получения 6,4 т СаС2. Какой объем СО (условия нормальные) при этом образуется? (Ответ: 5,6 т; 2240 м3).
30.6. Вычислить энтальпию образования оксида магния, исходя из уравнения реакции CO2 + 2Mg = 2MgO + C, ΔH° = –828,1 кДж. Энтальпия образования СО2 равна –393,5 кДж/моль. (Ответ: −601,8 кДж/моль).
30.7. Закончить уравнения реакций: а) SiO2 + KOH = …;
б) SiO2 + HF = …; в) Si + NaOH + H2O = …; г) SiO2 + Mg 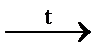 ….
….
30.8. Реакция протекает по уравнению Si + 2NaOH + H2O = Na2SiO3 + H2. Какая масса кремния и воды потребуется для получения водорода, необходимого для наполнения воздушного шара емкостью 200 м3 (условия нормальные)?
(Ответ: Si – 125 кг; Н2О – 80,3 кг).
30.9. Вычислить молярную массу эквивалентов карбоната натрия при взаимодействии с кислотой, если образуется: а) гидрокарбонат; б) угольная кислота. (Ответ: 106 г/моль; 53 г/моль).
30.10. Определить массу 40 %-го раствора фтороводородной кислоты, необходимую для растворения 6 г оксида кремния (IV). (Ответ: 15 г).
30.11. Какие из перечисленных газов при пропускании их через раствор щелочи вступают с ней в реакцию: а) СО; б) СО2; в) HCN; г) CF4?
Составить соответствующие уравнения реакций.
30.12. Вычислить энтальпию образования SiC, исходя из уравнения реакии
SiO2 + 3C = SiC + 2CO, ΔH°х.р. = 510,9 кДж.
Энтальпии образования SiO2 и CO соответственно равны –910,9 и ‑110,5 кДж/моль. (Ответ: –179 кДж/моль).
30.13. Закончить уравнения реакций:
а) CO + KMnO4 + H2SO4 = …; б) CO + K2Cr2O7 + H2SO4 = ….
30.14. Через раствор, содержащий 112 г гидроксида калия, пропустили диоксид углерода (условия нормальные), полученный при действии избытка HCl на 300 г карбоната кальция. Какая соль при этом образовалась и какова ее масса?
(Ответ: КНСО3; 200 г).
30.15. Какой объем СО2 (условия нормальные) может дать огнетушитель, содержащий 20 л8 %-го раствора NaHCO3 (плотность раствора 1,058 г/мл)? (Ответ: 448 л).
30.16. Состав минерала асбеста может быть выражен формулой CaО∙3MgО∙4SiO2. Вычислить процентное содержание SiO2 в асбесте.
(Ответ: 57,7 %).
30.17. Какой объем СО2 (условия нормальные) можно получить из 210 г
NaHCO3: а) прокаливанием; б) действием кислоты? (Ответ: 28 л; 56 л).
30.18. Закончить уравнения реакций:
а) SiO2 + Na2CO3  ….
….
б) CaC2 + H2O = …; в) Mg2Si + HCl = …; г) CO + Fe2O3 = …;
30.19. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
CaCO3 → CO2 → NaHCO3 → Na2CO3 → CO2.
30.20. Закончить уравнения реакций: а) Si + HNO3 + HF = …;
б) Al + C 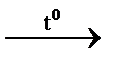 …; в) Na2SiO3 + HCl (конц.) = …; г) H2SiO3 + KOH = ….
…; в) Na2SiO3 + HCl (конц.) = …; г) H2SiO3 + KOH = ….
Углеводороды
Теоретическое введение
Углеводороды являются простейшими по составу органическими соединениями, так как состоят только из углерода и водорода. При замещении в молекулах углеводородов атомов водорода на атомы или группы атомов (радикалы) других элементов получаются другие классы органических соединений (производные углеводородов).
По характеру связи между углеродными атомами различают углеводороды с простыми связями, в которых все атомы углерода связаны одной ковалентной связью, и углеводороды с кратными (двойными или тройными) связями. В углеводородах с двойными связями два углеродных атома связаны между собой двумя ковалентными связями. Простейшим из этих углеводородов является этилен СН2=СН2.
Углеводороды с тройной связью содержат атомы углерода, связанные между собой тремя ковалентными связями, например ацетилен Н−С≡С−Н.
Углеводороды с простой связью характеризуются малой химической активностью. Они не вступают в реакции присоединения и, вследствие этого, получили название предельных (насыщенных) углеводородов. Однако при определенных условиях они способны к реакциям замещения. Углеводороды с кратными связями способны за счет разрыва второй и третьей связи присоединять водород, галогены и т. д. Например:
CН2=CН2 + Br2 → CН2Br−CН2Br.
этилен дибромэтан
Поэтому они названы непредельными (ненасыщенными) углеводородами.
Кратные связи могут содержаться и в молекулах циклических углеводородов. В тех случаях, когда цикл состоит из шести углеродных атомов, связанных между собой чередующимися простыми и двойными связями, углеводороды называются ароматическими. Простейшим из них является бензол С6Н6:
Несмотря на то, что в молекулах ароматических углеводородов имеются три двойные связи, они по своим химическим свойствам ближе к предельным углеводородам, т.е. способны, главным образом, к реакциям замещения.
Примеры решения задач
Пример 31.1. Написать уравнения реакций, при помощи которых из метана и неорганических реагентов можно получить бутан.
Решение. Бромированием метана можно получить бромметан:
CH4 + Br2 → CH3Br + HBr.
При нагревании бромметана с натрием образуется этан:
2CH3Br + 2Na → C2H6 + 2NaBr.
При взаимодействии этана с бромом образуется бромэтан:
C2H6 + Br2 → C2H5Br + HBr.
Бутан получается из бромэтана по реакции Вюрца:
2C2H5Br + 2Na → C4H10 + 2NaBr.
Пример 31.2. При сжигании газообразного углеводорода объемом 2,24 л было получено оксида углерода (IV) массой 13,2 г и воды массой 7,2 г. Плотность газа по воздуху составляет 1,52 (условия нормальные). Определить молекулярную формулу газа.
Решение. Молярная масса газа равна:
М (возд.) = 29 г/моль; Dвозд.(газа) = 1,52;
М (газа) = 29 г/моль ∙ 1,52 = 44 г/моль.
Масса углерода и водорода в 2,24 л углеводорода составляет:
12 г углерода образует 44 г СО2
х г углерода образует 13,2 г СО2 х = 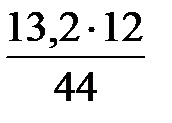 = 3,6 г С;
= 3,6 г С;
2 г водорода образует 18 г Н2О
y г водорода образует 7,2 г Н2О у = 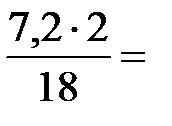 0,8 г Н.
0,8 г Н.
Масса углерода и водорода в сожженном газе составляет
3,6 + 0,8 = 4,4 г.
Рассчитаем массу 2,24 л углеводорода:
44 г углеводорода занимает объем 22,4 л
х г углеводорода занимает объем 2,24 л х = 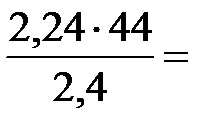 4,4 г.
4,4 г.
Итак, газ состоит только из углерода и водорода. Следовательно,
С:Н = 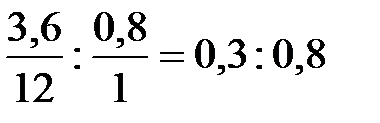 = 1:2,66,
= 1:2,66,
откуда простейшая формула СН2,66 (М = 14,66). Отношение истинного соединения к массе простейшего соединения составляет 
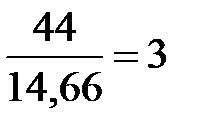 . Значит, простейшую формулу надо увеличить в 3 раза, откуда истинная формула газа С3Н8.
. Значит, простейшую формулу надо увеличить в 3 раза, откуда истинная формула газа С3Н8.
Пример 31.3. Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
этиловый спирт → Х → Y → Z → бутен-1
Указать условия протекания реакций.
Решение. При нагревании этилового спирта до 180–200 °С с концентрированной серной кислотой должен образоваться продукт, реагирующий с бромоводородом. Это этилен (вещество Х). Уравнение реакции
С2Н5ОН 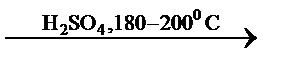 С2Н4 + Н2О.
С2Н4 + Н2О.
В результате присоединения бромоводорода к этилену образуется бромэтан (вещество Y):
С2Н4 + НBr → C2H5Br.
При нагревании бромэтана в присутствии натрия образуется бутан (Z)
C2H5Br + 2Na → C4H10 + 2NaBr.
Дегидрирование бутана в присутствии катализатора, например никеля – один из способов получения алкенов, в частности бутена-1.
CH3−CH2−CH2−CH3 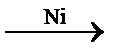 CH2=CH−CH2−CH3 + Н2
CH2=CH−CH2−CH3 + Н2
Пример 31.4. Написать уравнения реакций, которые надо провести для осуществления следующих превращений:
циклогексан → бензол → толуол → бензойная кислота.
Указать условия протекания реакций.
Решение. Циклогексан превращается в бензол при пропускании его паров над нагретым платиновым катализатором:
С6Н12 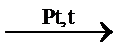 С6Н6 + 3Н2.
С6Н6 + 3Н2.
Ввести алкильную группу в бензольное кольцо можно действием галогеналкила в присутствии хлорида алюминия:
C6H6 + CH3Cl 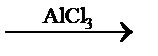 C6H5−CH3 + HCl.
C6H5−CH3 + HCl.
При действии раствора перманганата калия на толуол образуется бензойная кислота:
C6H5−CH3 + 3[O] 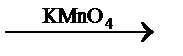 C6H5−COOH + H2O.
C6H5−COOH + H2O.
