Пример 1. Железная пластинка, погруженная в раствор серной кислоты, медленно разрушается, выделяя водород
Железная пластинка, погруженная в раствор серной кислоты, медленно разрушается, выделяя водород. Если к железной пластинке в растворе серной кислоты прикоснуться платиновой проволокой, то водород начинает выделяться на платине, а железо – разрушаться интенсивнее. Дайте объяснение этому явлению.
Решение.
Процесс самопроизвольного разрушения металла, вызываемый химическим или электрохимическим взаимодействием его с окружающей средой, называется коррозией.
При погружении железной пластинки в раствор серной кислоты протекает окислительно-восстановительная реакция:
Fe + H2SO4 = FeSO4 + H2,
Fe0 – 2 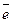 = Fe2+ – окисление,
= Fe2+ – окисление,
2H+ + 2 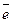 = H2 – восстановление.
= H2 – восстановление.
Если к железной пластинке прикоснуться платиновой проволокой, то в среде электролита возникает в месте контакта металлов гальванический элемент, появляется электродвижущая сила и окислительно-восстановительная реакция ускоряется. Железо в этом элементе – анод, оно окисляется и разрушается; платина – катод, на ней протекает восстановление ионов водорода. Такой вид электрохимической коррозии называется микрогальванической коррозией. Схема коррозии железа в контакте с платиной в среде серной кислоты имеет вид:
Fe ê H2SO4 ê Pt ,
анод (Fe) - Fe0 – 2 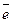 = Fe2+ – окисление,
= Fe2+ – окисление,
катод (Pt) - 2H+ + 2 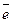 = H2 – восстановление,
= H2 – восстановление,
Fe2+ + SO  = FeSO4.
= FeSO4.
