Распределение молекул по скоростям. (Распределение Максвелла)
(Распределение Максвелла)
Молекулы газа движутся с самыми различными скоростями, причем, и величина, и направление скорости каждой отдельной молекулы непрерывно меняются из-за соударений. Каждая молекула при н.у. испытывает за секунду порядка 109 столкновений. Хаотичность движения предполагает равновероятность направлений движения, т.е. равномерное распределение молекул по направлениям. Иначе дело обстоит с численными значениями скорости. Возможные значения u, которые, согласно М-К.Т, лежат в интервале от нуля до бесконечности, отнюдь не равновероятны. Задача состоит в том, чтобы установить, какая часть из общего числа молекул движется с той или иной скоростью, т.е. найти закон распределения молекул по скоростям. При выводе этого закона Максвелл предполагал, что газ состоит из очень большого числа одинаковых молекул - N, находящихся в состоянии беспорядочного теплового движения при постоянной температуре Т, причем, никакие внешние силы на газ не действуют. Если разбить всю числовую ось скоростей молекул на малые интервалы dυ, то на каждый из них
 |
придется некоторое свое число молекул dN(υ):
Число dN(υ), очевидно, будет пропорционально общему числу молекул N и ширине интервала dυ. Чтобы записать равенство, необходимо ввести коэффициент пропорциональности, значение которого будет разным для разных интервалов, т.е. этот множитель представляет собой некую функцию f(υ). Теперь dN(υ) = f(υ)N∙dυ (21). Множитель f(υ) характеризует распределение молекул по скоростям и называется функцией распределения. Смысл этой функции в том, что она определяет, какая часть молекул имеет скорости, лежащие в интервале от υ до υ + dυ при Т = const, т.е. вероятность того, что молекула в данном газе имеет значение скорости из интервала dυ
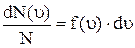 или
или 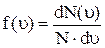 (22).
(22).
Применяя методы теории вероятности, Максвелл нашел
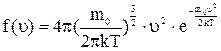 (23).
(23).
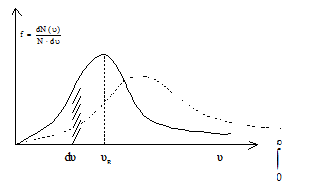 |
Относительное число молекул, скорости которых лежат в интервале от υ до υ + dυ, как это видно из рисунка, находятся, как площадь заштрихованной полоски: dN/N = f(υ)∙dυ. Очевидно, что площадь под кривой равна единице, т.е. 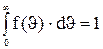
Значение скорости, на которую приходится максимум функции распределения, называется наиболее вероятной скоростью. Ее можно найти, исследовав функцию f(υ) на экстремум:
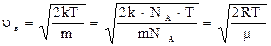 (24).
(24).
Из формулы (24) следует, что при повышении температуры максимум функции f(υ) сместится вправо, но площадь под кривой всегда равна единице. Это означает, что при повышении температуры кривая распределения будет растягиваться и понижаться (см. пунктирную линию).
Из закона распределения скоростей можно получить выражение для средней арифметической скорости молекул:
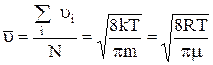 (25).
(25).
Из формулы (24) следует, что при повышении температуры максимум функции f(υ) сместится вправо, но площадь под кривой всегда равна единице. Это означает, что при повышении температуры кривая распределения будет растягиваться и понижаться (см. пунктирную линию).
Опыт Штерна (1920 г.)
Для экспериментальной проверки закона Максвелла немецкий физик Штерн поставил опыт:
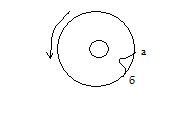 два коаксиальных жестко скрепленных друг с другом цилиндра вращались с постоянной угловой скоростью ω вокруг общей оси, вдоль которой была натянута платиновая нить, покрытая серебром. При пропускании тока по ней, нить нагревалась, и серебро испарялось. Атомы серебра могли вылетать из внутреннего
два коаксиальных жестко скрепленных друг с другом цилиндра вращались с постоянной угловой скоростью ω вокруг общей оси, вдоль которой была натянута платиновая нить, покрытая серебром. При пропускании тока по ней, нить нагревалась, и серебро испарялось. Атомы серебра могли вылетать из внутреннего
цилиндра через узкую щель и осаждались на внутренней стенке второго цилиндра. При этом в зависимости от скорости атомов υ их отклонение от точки а, лежащей на прямой нить - щель, будет разным. Чем меньше скорость, тем больше отклонение - зона аб. Если исследовать профиль следа аб, то можно судить о распределении атомов серебра по скоростям. Была установлена справедливость закона Максвелла.
