Получение кислотных оксидов и их взаимодействие с водой
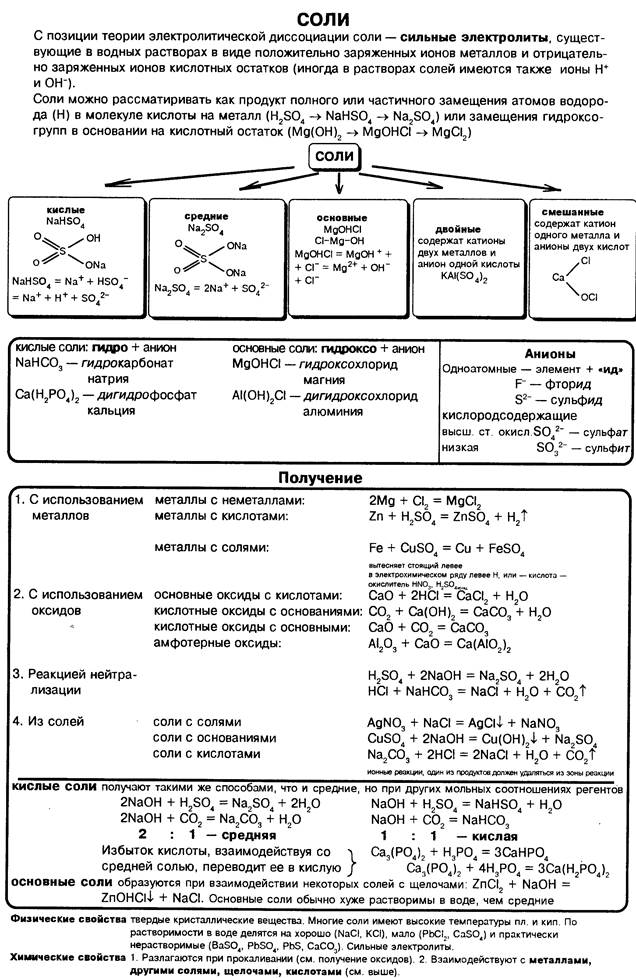
Задание 2.4.
Небольшое количество оксида фосфора с помощью стеклянной палочки поместить в пробирку. Прибавить воды. Внести 2-3 капли метилоранжа. Записать наблюдения и уравнение реакции. К полученному раствору прибавить гидроксид натрия до изменения цвета индикатора. Записать наблюдения и уравнение реакции.
Наблюдения:
________________
Уравнения реакций:
________________________________
Получение средних, кислых и основных солей и их взаимодействие с кислотами щелочами и другими солями.
Задание 2.5.
В химический стакан или пробирку внести 5 мл гидроксида калия и прибавить 1-2 капли фенолфталеина. Отметить наблюдения. Небольшими порциями, по 1-2 капли, вносить раствор соляной кислоты до полного ищезновения цвета индикатора. Записать наблюдения и уравнение реакции.
Наблюдения:
________________
Уравнение реакции:
________________
Задание 2.6.
Внести в пробирку 3-4 мл раствора хлорида кобальта и 1 мл гидроксида натрия. Записать наблюдения. Полученный раствор разделить на 2 пробирки. К первой прибавить соляной кислоты до изменения цвета раствора. Во вторую пробирку продолжить прибавлять гидроксид натрия тоже до изменения цвета раствора. Записать наблюдения и уравнения реакций.
Наблюдения:
________________
Уравнения реакций:
________________
Задание 2.7.
Внести в три пробирки по 2-3 мл растворов сульфата меди, сульфата никеля и хлорида железа. Прибавить к каждой из пробирок гидроксид калия по 1 мл
Записать наблюдения и уравнение реакций.
Наблюдения:
________________________________
Уравнения реакций:
________________________________
Выводи к лабораторной работе:
________________________________
Дата защиты лабораторной работы _________
Оценка лабораторной работы ______________ Подпись преподавателя_________________
Домашнее задание № 2
Основные классы неорганических соединений и типы химических реакций.
1. Напишите уравнения возможных реакций:
Na2O + H2O =
CaO + HCl =
NiO + H2O =
CaO + CO2=
2. Какие оксиды принадлежат к кислотным? Закончите уравнения реакций:
SO3 + CaO =
CO2 + Ca(OH)2 =
SO3 + NaOH =
P2O5 + Na2O =
________________________________
3. Какие оксиды принадлежат к амфотерным? Закончите уравнениия реакций:
ZnO + HCl =
ZnO + KOH =
________________________________
4. Как осуществить такие превращения:
CaO ® Ca(OH)2
________________
NiO ® Ni(OH)2
________________
5. Напишите уравнения реакций:
H2SO4 + NaOH =
H2SO4 + 2NaOH =
В каком случае образуется средняя соль, а в каком − кислая соль и почему?
________________________________
6. Закончите уравнения реакций:
BaSO4 + H2SO4 =
NaHCO3 + NaOH =
CaCO3 + H2O + CO2 =
7. Закончите уравнение реакций:
MgCl2 + NaOH =
Mg(OH)Cl + HCl =
MgCl2 + 2KOH =
Mg(OH)Cl + NaOH =
Какие соли называются основными?
________________________________
Оценка домашней работы ______________ Подпись преподавателя_________________




Словарь
| Закон постоянства состава |
| Закон Авогадро |
| I cледствие с закона Авогадро |
| II cледствие с закона Авогадро |
| Нормальные условия |
| Эквивалент |
| Эквивалентная масса |
| Молярная масса эквивалента вещества |
| Закон эквивалентов |
Лабораторная работа №3.
Определение молярной массы эквивалента металла методом вытеснения
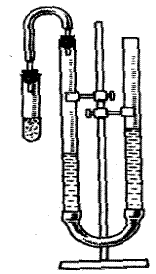 Соберите прибор для определения массы эквивалента металла методом вытеснения, схема которого представлена на рисунке. Проверьте герметичность прибора. Для этого хорошо закрепите пробки в пробирке и бюретке и переместите присоединенную бюретку вниз так, чтобы уровень воды в ней был ниже уровня воды во второй бюретке. Если прибор герметичен, то сначала уровень воды в бюретке немного снизится, а затем будет оставаться постоянным. Если уровень воды продолжает снижаться, значит, что прибор не герметичен и его нужно загерметизировать. Снимите пробирку и установите уровень воды в бюретке на отметке “0” или немного ниже. Влейте в пробирку 5 мл разведенной соляной кислоты. Взвесьте приблизительно 0,030 г алюминия на технических весах с точностью ±0,01г. Поместите алюминий на сухую стенку пробирки так, чтобы он не касался кислоты. Плотно закройте пробирку, следя за тем, чтобы металл не попал в кислоту. Убедитесь в том, что прибор закрыт герметически. После этого, перемещая присоединенную первую бюретку снизу верх, установите уровень воды в бюретке и воронке на одинаковой отметке возле “0”, для того, чтобы давление в середине прибора равнялось атмосферному давлению. Запишите в лабораторную тетрадь начальный уровень воды в бюретке (а1). Значение уровня воды нужно считывать за нижней линией мениска. Опустите металл в соляную кислоту. Наблюдайте выделение водорода и снижение уровня воды в бюретке. По окончании опыта дайте пробирке охладиться до комнатной температуры и установить опять уровень воды в бюретке и воронке на той же отметке. Запишите уровень воды в бюретке после опыта (а2). Результаты опыта запишите в таблицу 3.1.
Соберите прибор для определения массы эквивалента металла методом вытеснения, схема которого представлена на рисунке. Проверьте герметичность прибора. Для этого хорошо закрепите пробки в пробирке и бюретке и переместите присоединенную бюретку вниз так, чтобы уровень воды в ней был ниже уровня воды во второй бюретке. Если прибор герметичен, то сначала уровень воды в бюретке немного снизится, а затем будет оставаться постоянным. Если уровень воды продолжает снижаться, значит, что прибор не герметичен и его нужно загерметизировать. Снимите пробирку и установите уровень воды в бюретке на отметке “0” или немного ниже. Влейте в пробирку 5 мл разведенной соляной кислоты. Взвесьте приблизительно 0,030 г алюминия на технических весах с точностью ±0,01г. Поместите алюминий на сухую стенку пробирки так, чтобы он не касался кислоты. Плотно закройте пробирку, следя за тем, чтобы металл не попал в кислоту. Убедитесь в том, что прибор закрыт герметически. После этого, перемещая присоединенную первую бюретку снизу верх, установите уровень воды в бюретке и воронке на одинаковой отметке возле “0”, для того, чтобы давление в середине прибора равнялось атмосферному давлению. Запишите в лабораторную тетрадь начальный уровень воды в бюретке (а1). Значение уровня воды нужно считывать за нижней линией мениска. Опустите металл в соляную кислоту. Наблюдайте выделение водорода и снижение уровня воды в бюретке. По окончании опыта дайте пробирке охладиться до комнатной температуры и установить опять уровень воды в бюретке и воронке на той же отметке. Запишите уровень воды в бюретке после опыта (а2). Результаты опыта запишите в таблицу 3.1.
Таблица 3.1.
| Масса АI m, г | Уровень воды в бюретке | Температура опита Т, К | Атмосферное давление, ратм., кПа | Давление насыщенного водяного пара, р Н2 О, кПа | |
| Начальный а1, мл | После опыта а2, мл | ||||
Проведите вычисление:
1. Используя данные таблицы 3.2. рассчитайте парциальное давление водорода р H2 по формуле:
РН2 = Ратм – Р Н2 О; РН2=_________________________
Результаты запишите в табл. 3.3.
Таблица 3.2.
