Экспериментальная часть. Опыт 1. Влияние концентраций реагирующих веществ на скорость химической реакции в
Опыт 1. Влияние концентраций реагирующих веществ на скорость химической реакции в гомогенной системе.
Реакция взаимодействия тиосульфата натрия Na2S2O3 с серной кислотой H2SO4 протекает по уравнению:
Na2S2O3 + H2SO4 = Na2SO4+ S¯ +SO2 + H2O.
Проделать качественный опыт, для этого внести в пробирку 3-5 капель 1н раствора тиосульфата натрия Na2S2O3 и 2-3 капли 2н раствора серной кислоты H2SO4. Отметить появления опалесценции (слабого свечения) и дальнейшее помутнение раствора от выпадающей в осадок свободной серы.
После данного и последующего опыта следует немедленно мыть пробирки!
Приготовить три раствора тиосульфата натрия различной концентрации. Для этого в три сухие конические пробирки внести:
в первую: 4 капли раствора тиосульфата натрия и 8 капель воды;
во вторую: 8 капель раствора тиосульфата натрия и 4 капель воды;
в третью: 12 капель раствора тиосульфата натрия.
Содержимое пробирок перемешать стеклянными палочками.
Таким образом, в одинаковых объемах полученных растворов будет содержаться различное число молей тиосульфата натрия:
1С моль - количество молей тиосульфата натрия Na2S2O3 в пробирке №1,
2С моль-количество молей тиосульфата натрия Na2S2O3 в пробирке №2,
3С моль- количество молей тиосульфата натрия Na2S2O3 в пробирке №3
В пробирку №1 добавить одну каплю раствора серной кислоты, раствор перемешать стеклянной палочкой, чтобы реакция шла по всему объему раствора. По секундомеру или секундной стрелке наручных часов измерить время от момента добавления кислоты до появления в растворе первоначального помутнения. Аналогичный опыт проделать в пробирке №2, затем в пробирке №3.
Данные опытов занести в таблицу 5.1:
Таблица 5.1
Результаты опыта №1
| Пробирки | Число капель 1н р-ра Na2S2O3 | Число капель воды | Число капель серной кислоты | Условн. коцентр Na2S2O3 в молях | Время течения реакции t, сек | Скорость реакции 1/t в усл. ед.(tc) |
| C | ||||||
| 2C | ||||||
| 3C |
На миллиметровой бумаге начертить график зависимости скорости (V) реакции от концентрации реагирующих веществ (C): на оси абсцисс в произвольном масштабе отложить значения условных концентрации тиосульфата натрия, на оси ординат - значения скорости реакции в условных единицах.
Сделать вывод о влиянии концентрации реагирующих веществ на скорость химической реакции в гомогенной системе.
Опыт 2. Влияние температуры
На скорость химической реакции
Взять 2 пробирки. В одну из них поместить 5 капель тиосульфата натрия Na2S2O3, а в другую - 5 капель серной кислоты H2SO4. Обе пробирки поместить в стакан с водой при комнатной температуре.
Спустя 5 минут раствор серной кислоты прилить к раствору тиосульфата натрия. Определить время до начала помутнения.
Повторить опыт, но пробирки выдержать 5 минут в стакане с горячей водой (45-50°C), предварительно измерив ее температуру. Определить время до начала помутнения.
Понизив температуру горячей воды (25-30°C), проделать аналогичные действия с растворами в третьей паре пробирок.
Результаты наблюдений занести в таблицу 5.2.
Таблица 5.2
Результаты опыта №2
| № опы-та | Число капель Na2S2O3 | Число капель H2SO4 | Темпера-тура реак-ции, оС | Время до появления мути, t,сек | Скорость реакции в усл. ед.V=1/t |
По результатам опыта начертить график зависимости скорости реакции (V) от температуры. По оси абсцисс отложить температуру в оС, а по оси ординат - соответствующие им скорости (в усл.ед.)
Сформулировать зависимость скорости реакции от температуры.
Опыт 3. Влияние величины поверхности раздела реагирующих веществ на скорость реакции в гетерогенной системе
Взять 2 небольших и по возможности одинаковых кусочка мела CaCO3. Один из них положить на фильтровальную бумагу и стеклянной палочкой измельчить его в порошок. Полученный порошок поместить в пробирку. Второй кусочек мела целиком опустить в другую пробирку. В обе пробирки одновременно добавить 15 капель хлорводородной кислоты HCl. Отметить время полного растворения мела в каждом случае.
Написать уравнение соответствующей реакции.
Почему скорость растворения мела в этих случаях различна?
Вопросы для самоконтроля
1. От чего зависит скорость химической реакции в гомогенных и гетерогенных реакциях?
2. Как зависит скорость гомогенных реакции от концентрации реагирующих веществ и температуры?
3. Как объяснить механизм действия катализатора при гомогенном и гетерогенном катализе?
4. Написать выражения скорости для следующих реакций:
а) 2А(газ) + В(газ) = А2В(газ) , б) N2 (газ) + O2 (газ) = 2NO (газ),
в) FeO(тв) + H2 (газ) = Fe(тв) + H2O(ж)
Как изменится скорость реакции а) и б) при увеличении концентрации исходных веществ в два раза?
5. Константа скорости реакции
А + 2В = АВ2 равна 2´10-3л/мольoС.
а) Какова скорость указанной реакции в начальный момент, если концентрации веществ А равна концентрации веществ В и составляет 0,4 моль/л?
б) Какова будет скорость 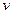 2 этой реакции через некоторое время, если к этому моменту образуется 0,1 моль/л вещества АВ2?
2 этой реакции через некоторое время, если к этому моменту образуется 0,1 моль/л вещества АВ2?
6. Температурный коэффициент скорости некоторой реакции равен 1,5. Во сколько раз увеличится скорость данной реакции при повышении температуры на 300С?
