Групповой реагент, общие и фармакопейные реакции анионов I аналитической группы
Групповой реагент – раствор BaCl2
Реакции сульфат-иона SO42-
Хлорид бария BaCl2 осаждает из разбавленных растворов сульфатов белый осадок сульфата бария:
BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl
Ba2+ + SO42- = BaSO4↓
Сульфат бария нерастворим в кислотах. Этим он отличается от других бариевых солей анионов первой группы. Реакция является фармакопейной.
Реакция фосфат-иона РО43-
1. Хлорид бария BaCl2 выделяет из нейтральных растворов белый аморфный осадок гидрофосфата бария:
Na2HPO4 + BaCl2 = BaHPO4↓ + 2NaCl
HPO42- + Ba2+ = BaHPO4↓
Осадок растворим в минеральных кислотах (кроме серной) и в уксусной кислоте.
Если проводить реакцию в слабощелочной среде или с раствором соли Na3PO4, выделяется осадок Ba3(PO4)2↓
3Ba2+ + 2PO43- = Ba3(PO4)2↓
2. Нитрат серебра AgNO3дает с фосфатом-ионом желтый осадок фосфата серебра, легко растворимый в азотной кислоте и в растворе аммиака. Полное осаждение возможно только в нейтральной или щелочной среде:
Na3PO4 + 3AgNO3 = AgPO4↓ + 3NaNO3
PO43- + 3Ag+ = AgPO4↓
Реакция является фармакопейной.
Реакции карбонат-иона СО22-
1. Хлорид бария BaCl2 из растворов карбонатов осаждает на холоде белый осадок карбоната бария:
BaCl2 + Na2CO3 = BaCO3↓ + 2NaCl
Ba2+ + CO32- = BaCO3↓
Осадок легко растворим в разбавленных хлороводородной, азотной и в уксусной кислотах. При кипячении кристаллизуется и становится более плотным.
2. Кислоты разлагают все карбонаты с бурым выделением оксида углерода (IV):
Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O
CO32- + 2H+ = H2O + CO2↑
Реакция является фармакопейной.
Образуйте данные комплексные частицы в соединения и укажите внутреннюю и внешнюю координационные сферы.
[Be(NH3)4], где Be+2; [Co(NH3)2 (NO2)4], где Co+3;
- К[Co(NH3)2 (NO2)4]
Внешняя координационная сфера К+
Внутренняя координационная сфера [Co(NH3)2 (NO2)4]
-[Be(NH3)4]SO4
Внешняя координационная сфера SO42-
Внутренняя координационная сфера [Be(NH3)4]2+
5.Составьте уравнения гидролиза солей:
NaNO3, Ca(CN)2, MgS, СH3COONa, СH3COONH4, Cu(NO3)2,
Укажите рН раствора.
NaNO3 + HOH= гидролиз не идет
Ca(CN)2+ HOH= HCN+ CaOHCN
CN-+ HOH= HCN+ OH-
CaOHCN+ HOH= Ca(OH)2+ HCN
CN-+ HOH= HCN+ OH-
Среда щелочная, фиолетовый лакмус станет синим.
Al2(SO4)3+ 2HOH= 2AlOHSO4+ H2SO4
Al3+HOH= AlOH2++ H+
2AlOHSO4+ 2HOH=(Al(OH)2)2SO4+ H2SO4
AlOH2++HOH= Al(OH)2++ H+
(Al(OH)2)2SO4+2HOH= 2Al(OH)3+ H2SO4
Al(OH)2++HOH= Al(OH)3+ H+
Среда кислая, фиолетовый лакмус станет красным.
CH3COONH4+ HOH= CH3COOH+ NH4OH
CH3COO-+ NH4++HOH= CH3COOH+ NH4OH
Среда нейтральная.
CH3COONa+ HOH= CH3COOH+ NaOH
CH3COO-+HOH= CH3COOH+ OH-
Среда щелочная, фиолетовый лакмус станет синим.
Сu(NO3)2+ HOH= CuOHNO3+ HNO3
Cu2++ HOH= CuOH++ H+
CuOHNO3+ HOH= Cu(OH)2+ HNO3
CuOH++HOH= Cu(OH)2+ H+
Среда кислая, фиолетовый лакмус станет красным.
| департамент здравоохранения Брянской области Государственное автономное образовательное учреждение среднего профессионального образования «Брянский базовый медицинский колледж» | 060301 «Фармация» (код и наименование специальности) базовый (профиль подготовки) «Фармация» (наименование ВМК) |
Учебная дисциплинаАналитическая химия
Коды проверяемых компетенций:
ОК: 2, 3
ПК: 1.1; 1.6; 2.1; 2.2; 2.3
БИЛЕТ №26
1.Определите среднюю скорость реакции: А+Б => C , концентрация вещества (А) в начальный момент была равна 1,5моль/литр, а через 30минут стала равной 0,5 моль/литр. Vср= 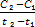 Vср =
Vср = 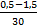 =
= 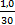 = 0,033
= 0,033
Ответ: 0,033 моль/л*мин
2.Напишите характерные реакции на ион NH4+.
Гидроксиды щелочных металлов NaOH и KOH при добавлении к водному раствору соли аммония выделяют аммиак:
NH4Cl + NaOH = NaCl + NH3↑ + H2O
При нагревании раствора аммиак улетучивается.
Реактив Несслера (смесь K2[HgJ4] с КОН) дает с солями аммония красно-бурый осадок:
2K2[HgJ4] + 4KOH + Na4Cl →[Hg2ONH2] J ↓ + 7KJ + KCL + 3H2O
