Дать определение молярной и нормальной концентрациям
Молярная концентрация — количество растворённого вещества (число молей) в единице объёма раствора. Молярная концентрация в системе СИ измеряется в моль/м³, однако на практике её гораздо чаще выражают в моль/л или ммоль/л. Также распространено выражение в «молярности». Возможно другое обозначение молярной концентрации 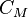 , которое принято обозначать М. Так, раствор с концентрацией 0,5 моль/л называют 0,5-молярным.
, которое принято обозначать М. Так, раствор с концентрацией 0,5 моль/л называют 0,5-молярным.
Примечание: После числа пишут «моль», подобно тому, как после числа пишут «см», «кг» и т. п., не склоняя по падежам.
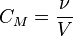 ,
,
где:
· ν — количество растворённого вещества, моль;
· V — общий объём раствора, л.
Нормальная концентрация — количество эквивалентов данного вещества в 1 литре раствора. Нормальную концентрацию выражают в моль-экв/л или г-экв/л (имеется в виду моль эквивалентов). Для записи концентрации таких растворов используют сокращения «н» или «N». Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.
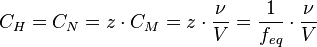 ,
,
где:
· ν — количество растворённого вещества, моль;
· V — общий объём раствора, литров;
· z — число эквивалентности (фактор эквивалентности 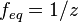 ).
).
·
Гальванический элемент. Устройство гальванического элемента. Катод, анод. Процессы, протекающие на катоде и аноде.
Гальвани́ческий элеме́нт — химический источник электрического тока, основанный на взаимодействии двух металлов и/или их оксидов в электролите, приводящем к возникновению в замкнутой цепи электрического тока.
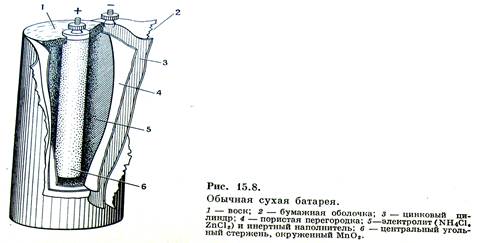
Состав гальванического элемента
: восстановителями (анодами) в портативных гальванических элементах, как правило, служат цинк Zn, литий Li, магний Mg; окислителями (катодами) – оксиды марганца MnO2, меди CuO, серебра Ag2O, серы SO2, а также соли CuCl2, PbCl2, FeS и кислород О2.
Токообразующими реакциями в этом элементе являются
:
- на аноде
(–): Zn – 2ē → Zn2+ (на практике происходит постепенное растворение цинковой оболочки корпуса элемента);
- на катоде
(+): 2MnO2 + 2NH4+ + 2ē → Mn2O3 + 2NH3 + H2O.
В электролитическом пространстве также идут процессы:
- у анода
Zn2+ + 2NH3 →[Zn(NH3)2]2+;
- у катода
Mn2O3 + H2O → [Mn2O2(OH)2] или 2[MnOOH].
10. Донорно-акцепторный механизм образования ковалентной связи. Рассмотреть на примере образования иона NH4+.
Донорно-акцепторный механизм образования ковалентной связи - это способ образования ковалентной связи между двумя атомами или группой атомов, осуществляемый за счет неподеленной пары электронов атома-донора и свободной орбитали атома-акцептора.
Донор - элемент, имеющий свободную пару электронов. Акцептор имеет пустую орбиталь.
По этому принципу образован NH4 (аммоний)
Правило Ле-Шателье.
Принцип Ле Шателье — Брауна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
Химическое равновесие смещается в ту или иную сторону при изменении любого из следующих параметров:
1) температуры системы, т.е. при её нагревании или охлаждении
2)давления в системе, т.е. при её сжатии или расширении
3) концентрации одного из участников обратимой реакции
