ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ. 202. Исходя из степени окисления хлора в соединениях НСl
(№ 202−220)
202. Исходя из степени окисления хлора в соединениях НСl, НСlO3, НСlO4, определите, какое из них является только окислителем, только – восстановителем. Укажите, какое из приведенных веществ может проявлять как окислительные, так и восстановительные свойства. На основании электронных уравнений расставьте коэффициенты в уравнении реакции, протекающей по схеме:
Р + НClO3 + Н2 O  Н3РO4 + НCl.
Н3РO4 + НCl.
203. Составьте электронные уравнения и укажите, какой процесс – окисление или восстановление происходит при следующих превращениях: Аs+3 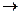 As+5; N+3
As+5; N+3 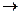 N−3; S−2
N−3; S−2 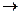 S0.
S0.
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, протекающей по схеме:
Н3АsО3 + КМnO4 + Н2SO4  Н3АsO4 + МnSO4 + K2SO4 + H2О.
Н3АsO4 + МnSO4 + K2SO4 + H2О.
204. Исходя из степени окисления фосфора в соединениях РН3, Н3РO4, Н3РО3, определите, какое из них является только окислителем, только – восстановителем. Укажите, какое из данных веществ может проявлять как окислительные, так и восстановительные свойства. На основании электронных уравнений расставьте коэффициенты в уравнении реакции, протекающей по схеме:
Р + НNO3 + Н2О  Н3РO4 + NO.
Н3РO4 + NO.
205. Составьте электронные уравнения и укажите, какой процесс – окисление или восстановление − происходит при следующих превращениях:
Мn+6 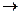 Мn+2; Cl+5
Мn+2; Cl+5 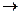 Сl−;N−3
Сl−;N−3 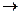 N+5.
N+5.
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, протекающей по схеме:
Cu2O + HNO3  Cu(NO3)2 + NO + H2O.
Cu(NO3)2 + NO + H2O.
206. Исходя из степени окисления хрома, йода и серы в соединениях К2СrO4, КJ и Н2SO3, определите, какое из веществ является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительныe свойства? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, протекающей по схеме:
NаСrO2 + РbО2 + NаО  Nа2СrO4 + Nа2РbO2 + Н2О.
Nа2СrO4 + Nа2РbO2 + Н2О.
207. Объясните, могут ли происходить окислительно-восстановительные реакции между веществами: а) NН3 и КМnO4; б) НNO2 и НJ; в) НСl и Н2Sе? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, протекающей по схеме:
КМnO4 + КNO + Н2SO4  МnSO4 + КNО3 + К2SO4 + Н2O.
МnSO4 + КNО3 + К2SO4 + Н2O.
208. Укажите, могут ли происходить окислительно-восстановительные процессы между веществами: а) РН3 и НВr; б) K2Сr2O7 и Н3РО3; в) НNО3 и Н2S? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, протекающей по схеме:
K2Сr2O7 + Н2S + H2SO4  Сr2(SO4)3 + S + K2SO4 + Н2O.
Сr2(SO4)3 + S + K2SO4 + Н2O.
209−220. Составьте электронные уравнения. Расставьтe коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, а какое – восстановителем.
| № задачи | Уравнения реакций |
КВr + КВrO3 + Н2SO4  Вr2 + К2SO4+ Н2О, Cu2O + HNO3 Вr2 + К2SO4+ Н2О, Cu2O + HNO3  Cu(NO3)2 + NO + Н2О Cu(NO3)2 + NO + Н2О | |
НСl + СrO3  Сl2 + СrСl3 + Н2O, Сd + КМnO4 + Н2SO4 Сl2 + СrСl3 + Н2O, Сd + КМnO4 + Н2SO4  CdSO4 + MnSO4 + K2SO4+ Н2O CdSO4 + MnSO4 + K2SO4+ Н2O | |
СrO3 + КClO + КОН  К2СrO4+ КСl + Н2O, MnSO4 + РbO2 +НNО3 К2СrO4+ КСl + Н2O, MnSO4 + РbO2 +НNО3  НМnO4+ Рb(NО3)2 + PbSO4+Н2O НМnO4+ Рb(NО3)2 + PbSO4+Н2O | |
Н2S + Cl2 + Н2О  Н2SO4 + НСl, К2Сr2O7 + Н2S + Н2SO4 Н2SO4 + НСl, К2Сr2O7 + Н2S + Н2SO4  S+ Сr2(SO4)3 + K2SO4 + Н2О S+ Сr2(SO4)3 + K2SO4 + Н2О | |
J2 + Сl2 + Н2O  НJO3 + НСl, АsН3 + НNО3 НJO3 + НСl, АsН3 + НNО3  Н3АsO4 + NO2 + Н2O Н3АsO4 + NO2 + Н2O | |
К2Сr2O7 + НСl  Сl2 + СrСl3 + КСl + H2О, Аu + НNО3 + НСl Сl2 + СrСl3 + КСl + H2О, Аu + НNО3 + НСl  АuСl3 + NO + Н2O АuСl3 + NO + Н2O | |
НNO3 + Zn  N2O + Zn(NO3)2 + H2О, FeSO4 + КClO3 + Н2SO4 N2O + Zn(NO3)2 + H2О, FeSO4 + КClO3 + Н2SO4  Fe2(SO4)3 + КСl + H2О Fe2(SO4)3 + КСl + H2О | |
NаСrO2 + Вr2 + NаОН  Nа2СrO4 + NаВr + H2О, FeS + НNО3 Nа2СrO4 + NаВr + H2О, FeS + НNО3  Fe(NО3)2 +S + NO + H2О Fe(NО3)2 +S + NO + H2О | |
Na2SO3 + KМnO4 + H2O  Na2SO4 + MnO2 + KOH, Р + НClO3 + Н2О Na2SO4 + MnO2 + KOH, Р + НClO3 + Н2О  Н3РO4 + НСl Н3РO4 + НСl | |
КClO3 + Nа2SO3  КСl + Nа2SO4, КМnO4 + НВr КСl + Nа2SO4, КМnO4 + НВr  Вr2 + КВr + МnВr2 + Н2О Вr2 + КВr + МnВr2 + Н2О | |
РbS + НNO3  S+ Рb(NO3)2 + NO + Н2О, КМnO4 + Nа2SO3 + КОН S+ Рb(NO3)2 + NO + Н2О, КМnO4 + Nа2SO3 + КОН  К2МnО4 + Nа2SO4 + Н2О К2МnО4 + Nа2SO4 + Н2О | |
HNO3 + Са  NН4NО3 + Са(NO3)2 + H2O, К2S + КМnO4 + Н2SO4 NН4NО3 + Са(NO3)2 + H2O, К2S + КМnO4 + Н2SO4  S + К2SO4 + МnSO4 + Н2О. S + К2SO4 + МnSO4 + Н2О. |
