Подбор коэффициентов методом электронно-ионного баланса
(метод полуреакций)
При подборе коэффициентов методом ЭМБ отпадает необходимость нахождения степеней окисления элементов, легко определяются стехиометрические коэффициенты в молекулярном уравнении.
Правила оформления уравнений ОВР, протекающих в кислотной среде.
- Записать схему реакции. Определить молекулы или ионы, которые участвуют в процессе окисления и восстановления.
- Записать в ионном виде полуреакции окисления и восстановления. Слабые электролиты, твердые и газообразные вещества записываются в молекулярном виде.
- На основании закона сохранения массы и энергии при составлении уравнений полуреакций следует соблюдать баланс веществ и баланс зарядов.
Для уравнивания числа атомов кислорода в ту часть полуреакции, где он в избытке, добавляют столько катионов водорода Н+, чтобы, связавшись с атомами кислорода, образовались молекулы Н2О. В противоположную часть добавляют молекулы Н2О.
Уравнять кислород, затем водород, затем уравнивают электроны.
- Балансируют (уравнивают) число отданных и принятых ē в полуреакциях.
- Суммируют сначала левые, а затем правые части полуреакций, не забывая предварительно умножить множитель на коэффициент, если он стоит перед формулой. Результат – суммарное ионное уравнение.
- Подчеркивают и сокращают одинаковые ионы и молекулы.
- Добавляют недостающие катионы или анионы. Количество добавляемых ионов в левую и правую части ионного уравнения должно быть одинаковым. Результат – молекулярное уравнение.
Например:
| Схема уравнения |  S0+HNO3- H2SO42- + NO0 S0+HNO3- H2SO42- + NO0 | |
| 1-я полуреакция |   1 S0 + 4H2O0 -6ē SO42- + 8H+ 1 S0 + 4H2O0 -6ē SO42- + 8H+  2 NO3- + 4H+ + 3ē NO0 + 2H2O0 2 NO3- + 4H+ + 3ē NO0 + 2H2O0 | |
| 2-я полуреакция | ||
| Суммарное ионное уравнение |  S + 4H2O + 2NO3- + 8H+ SO42- + 8H+ + 2NO + 4H2O S + 4H2O + 2NO3- + 8H+ SO42- + 8H+ + 2NO + 4H2O  S + 2NO3- SO42- + 2NO S + 2NO3- SO42- + 2NO | |
| Добавляемые ионы | 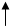 2H+ = 2H+ 2H+ = 2H+ | |
| Итоговое молекулярное уравнение | S +2HNO3 = H2SO4 + 2NO |
1.
 KNO2- + HClO3- KNO3- + HCl-
KNO2- + HClO3- KNO3- + HCl-

 3 NO2- + H2O0 - 2ē NO3- + 2H+
3 NO2- + H2O0 - 2ē NO3- + 2H+
 1 ClO3- + 6H+ + 6ē Cl- + 3H2O0
1 ClO3- + 6H+ + 6ē Cl- + 3H2O0

 3NO2- + 3H2O + ClO3- + 6H+ 3NO3- + 6H+ + Cl- + 3H2O
3NO2- + 3H2O + ClO3- + 6H+ 3NO3- + 6H+ + Cl- + 3H2O
 3NO2- + ClO3- 3NO3- + Cl-
3NO2- + ClO3- 3NO3- + Cl-
3K+ + H+ = 3K+ + H+
3KNO2 + HClO3 = 3KNO3 + HCl
2.
 KI- + KNO2- + H2SO4 I20 + NO0 + K2SO4 + H2O
KI- + KNO2- + H2SO4 I20 + NO0 + K2SO4 + H2O

 1 2I- - 2ē I20
1 2I- - 2ē I20
 2 NO2- + 2H+ + 1ē NO0 + H2O
2 NO2- + 2H+ + 1ē NO0 + H2O

 2I- + 2NO2- + 4H+ I2 + 2NO + 2H2O
2I- + 2NO2- + 4H+ I2 + 2NO + 2H2O
2K+ + 2K+ + 2SO42- = 4K+ + 2SO42-
2KI + 2KNO2 + 2H2SO4 = I2 + 2NO + 2K2SO4 + 2H2O
 3.
3.
 HCl- + HClO3- Cl20 + H2O
HCl- + HClO3- Cl20 + H2O

 5 Cl- - 1ē Cl0
5 Cl- - 1ē Cl0
 1 ClO3- + 6H+ + 5ē Cl0 + 3H2O
1 ClO3- + 6H+ + 5ē Cl0 + 3H2O

2Cl- + ClO 3-+ 6H+ 5Cl0 +Cl0 + 3H2O
 5HCl + HClO3 = 3Cl2 + 3H2O
5HCl + HClO3 = 3Cl2 + 3H2O
4.
 KMnO4- + Fe2+SO4 + H2SO4 Mn2+SO4 + Fe23+(SO4)3 + K2SO4 + H2O
KMnO4- + Fe2+SO4 + H2SO4 Mn2+SO4 + Fe23+(SO4)3 + K2SO4 + H2O
 2 MnO4- + 8H+ +5ē Mn2+ +4H2O0
2 MnO4- + 8H+ +5ē Mn2+ +4H2O0
 5 2Fe2+ - 2ē 2Fe3+
5 2Fe2+ - 2ē 2Fe3+

 2MnO4- +16H+ + 10Fe2+ 2Mn2+ +8H2O + 10Fe3+
2MnO4- +16H+ + 10Fe2+ 2Mn2+ +8H2O + 10Fe3+
2K+ + 8SO42- +10SO42- = 2SO42- +2K+ + SO42- + 15SO42-
2KMnO4 + 8H2SO4 +10FeSO4 = 2MnSO4 + K2SO4 + 5Fe2(SO4)3 + 8H2O
5.
 K2Cr2O72- + H2S2- + H2SO4 S0 + Cr23+(SO4)3 + K2SO4 + H2O
K2Cr2O72- + H2S2- + H2SO4 S0 + Cr23+(SO4)3 + K2SO4 + H2O
 |
 1 Cr2O72- + 14H+ + 6ē 2Cr3+ + 7H2O
1 Cr2O72- + 14H+ + 6ē 2Cr3+ + 7H2O
 3 S2- -2ē S0
3 S2- -2ē S0



 Cr2O72- + 14H+ + 3S2- 2Cr3+ + 7H2O +3S
Cr2O72- + 14H+ + 3S2- 2Cr3+ + 7H2O +3S
8H+ +16H+
2K+ + 4SO42- = 3SO42- + 2K+ + SO42-
K2Cr2O7 + 4H2SO4 + 3H2S = Cr2(SO4)3 +K2SO4 + 3S +7H2O
6.
 KI- + H2SO42- I20 + H2S2- + K2SO4 + H2O
KI- + H2SO42- I20 + H2S2- + K2SO4 + H2O
 |
 4 2I- -2ē I20
4 2I- -2ē I20
 1 SO42- + 8H+ +8ē S2- +4H2O
1 SO42- + 8H+ +8ē S2- +4H2O

 8I- + SO42- + 8H+ 4I2 + S2- +4H2O
8I- + SO42- + 8H+ 4I2 + S2- +4H2O
8K+ + 2H+ + 4SO42- = 2H+ +8K+ + 4SO42-
 |
8KI + 5H2SO4 = 4I2 + H2S + 4K2SO4 +4H2O
7.
 Сa0 + HNO3- Ca2+(NO3)2 + N2O0 +H2O
Сa0 + HNO3- Ca2+(NO3)2 + N2O0 +H2O

 4 Сa0 - 2 ē Ca2+
4 Сa0 - 2 ē Ca2+
 1 2NO3- +10H+ + 8 ē N2O0 +5H2O
1 2NO3- +10H+ + 8 ē N2O0 +5H2O

 4Сa + 2NO3- +10H+ 4Ca2+ + N2O +5H2O
4Сa + 2NO3- +10H+ 4Ca2+ + N2O +5H2O
8NO3- = 8NO3-
4Сa + 10HNO3 = 4Ca(NO3)2 + N2O +5H2O
8.
 K2Cr2O72- + KNO2- + H2SO4 Cr23+(SO4)3 +KNO3- + K2SO4 +H2O
K2Cr2O72- + KNO2- + H2SO4 Cr23+(SO4)3 +KNO3- + K2SO4 +H2O
 |
 1 Cr2O72- + 14H+ +6 ē 2Cr3++7H2O
1 Cr2O72- + 14H+ +6 ē 2Cr3++7H2O
 3 NO2- + H2O -2 ē NO3- + 2H+
3 NO2- + H2O -2 ē NO3- + 2H+

 Cr2O72- +14H+ + 3NO2- + 3H2O 2Cr23+ + 7H2O +3NO3- + 6H+
Cr2O72- +14H+ + 3NO2- + 3H2O 2Cr23+ + 7H2O +3NO3- + 6H+
 Cr2O72- + 8H+ + 3NO2- 2Cr23+ +4H2O +3NO3-
Cr2O72- + 8H+ + 3NO2- 2Cr23+ +4H2O +3NO3-
2K+ + 4SO42-+3K+ = 3SO42- +3K+ + 2K + +SO42-
K2Cr2O7 + 4H2SO4+ 3KNO2 = Cr2(SO4)3 +3KNO3 + K2SO4 +4H2O
9.
 Pb0 + HNO3- Pb2+(NO3)2 + NO20 +H2O
Pb0 + HNO3- Pb2+(NO3)2 + NO20 +H2O
 |
 1 Pb0 -2 ē Pb2+
1 Pb0 -2 ē Pb2+
 2 NO3- + 2H+ +1 ē NO20 +H2O
2 NO3- + 2H+ +1 ē NO20 +H2O

 Pb + 2NO3- + 4H+ Pb2++ 2NO2 +2H2O
Pb + 2NO3- + 4H+ Pb2++ 2NO2 +2H2O
2NO3- = 2NO3-
Pb + 4HNO3 = Pb(NO3)2 + 2NO2 + 2H2O
10.
 NaBr - + NaBrO3- +H2SO4 Br20 + Na2SO4 +H2O
NaBr - + NaBrO3- +H2SO4 Br20 + Na2SO4 +H2O
 |
 5 Br - -1 ē Br0
5 Br - -1 ē Br0
 1 BrO3- +6H+ +5 ē Br0 + 3H2O
1 BrO3- +6H+ +5 ē Br0 + 3H2O

 5Br - +BrO3- +6H+ 5Br0 + Br0 +3H2O
5Br - +BrO3- +6H+ 5Br0 + Br0 +3H2O
5Na+ + Na+ +3SO42- = 6Na+ + SO42-
5NaBr + NaBrO3- + 3H2SO4 = 3Br20 + 3Na2SO4 +3H2O
