Методические рекомендации. Изучение этой темы целесообразно разбить на три части
Изучение этой темы целесообразно разбить на три части. Сначала изучить материал по учебнику: образование растворов, физическая и химическая теория растворов, разбавленные растворы неэлектролитов, растворы электролитов и попробуйте ответить на контрольные вопросы. Затем следует выполнить задачи и упражнения на нахождение концентраций растворов.
В химических расчетах используется в основном три способа выражения концентрации: массовая доля показывает, сколько граммов растворенного вещества находится в 100 г раствора
ω= 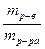 (2)
(2)
где, ω - массовая доля,
m р-в - масса растворенного вещества
m р-ра - масса раствора
Молярная концентрация - показывает, сколько молей растворенного вещества находится в 1 л. (1000 мл.) раствора
CM = 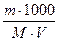 ; (3)
; (3)
где, m - масса растворенного вещества
М- молярная масса растворенного вещества
V - объем раствора
См молярная концентрация
Молярная концентрация эквивалента (нормальная концентрация) показывает, сколько молей эквивалента растворенного вещества, находится в одном литре (1000 мл.) раствора.
СН = 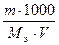 (4)
(4)
где, Сн – моль – экв./л
Мэ - молярная масса эквивалента
V -объем раствора
Количество молей v = 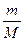
Количество моль-эквивалента vэкв= 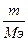 ; (5)
; (5)
Плотность раствора ρ= 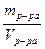 (6)
(6)
Титр-это количество граммов растворенного вещества, содержащего в 1 мл раствора.
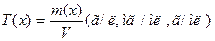
Задачи на пересчет из одной концентрации в другую являются составным этапом большинства задач, включающих свойства растворов.
Пример1 Найдите молярную концентрацию 10% раствора сахарозы С12Н22О11. Плотность раствора равна 1,08 г/мл.
Дано: Решение:
Wc 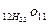
 = 10%
= 10%  нам дано 10% С12 Н 22О11 , это значит в 100 г р-ра
нам дано 10% С12 Н 22О11 , это значит в 100 г р-ра
ρ = 1.08 г/мл содержится 10г С12Н22О11
См - ?
Находим объем раствора V= 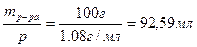
Находим число молей в 10г. С12Н22О11. v= 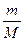 ;
;
М (С12Н22О11) =12+12+22+1 + 11∙16=342 г/моль v = 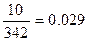 моль
моль
92,59 мл - 0,029 моль
1000мл - х моль
См = 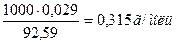
в 1 литре содержится 0,315 моль С12Н22О11
Ответ: См =0,315 моль
Пример 2 Найдите массовую долю 0,25 н раствора НNO3 , если плотность раствора равна 1,03г/мл.
Дано: Решение:
Сн = 0,25н 0,25 н означает, что в 1000мл содержится 0,25 моль-экв
ρ =1,03 г/мл HNO3
ω HNO3 -? Находим эквивалентную массу
М( HNO3) =1+ 14+16-3-63 г/моль
Мэ = 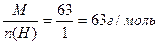
Находим массу 0,25 моль-экв. HNO3 m = 0,25*63=15.75 г Находим массу 1000мл. раствора.
mр.ра= V∙ ρ =1000мл ∙ 1,03 г/моль=1030 г
1030 г р-ра содержится 15,75 г HNO3
100 г р-ра содержится х г HNO3
ω = 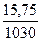 ∙100 = 1.53г или 1,53%
∙100 = 1.53г или 1,53%
Ответ: W =1,53%
Контрольные вопросы
1 Какие растворы называются истинными?
2 Какие физические и химические силы участвуют в образовании растворов?
3 Какие способы выражения концентрации растворов вам известны?
4 Чем отличается молярная концентрация от молярной концентрации эквивалента?
5 Сформулируйте законы Рауля
6 Что такое осмос и Осмотическое давление? Закон Вант-Гоффа.
7 В чем заключается влияние природы растворенного вещества и его концентрации на понижение температуры замерзания раствора?
8 Объясните причину понижения температуры при смешивании льда с солью.
Рекомендуемая литература
Основная
1 Хомченко Г.П., Цитович И.К Неорганическая химия.- М.: Высшая школа, 1987
2 Князев Д.А. Смарыгин С.Н Неорганическая химия.- М.: Высшая школа, 1990
Дополнительная
3 Ахметов Н.С. Неорганическая химия М., Высшая школа 1990
4 Платонов Ф.П., Дейкова З.Е Практикум по неорганической химии., М., Высшая школа, 1985. Стр.69-85.
Лабораторная работа
