Комплексонометрическое титрование
Комплексоны – это специальные органические комплексообразующие реагенты класса аминополикарбоновых кислот, которые являются полидентатными лигандами, связывающие ионы металлов по типу внутрикомплексных солей и широко применяемые в качестве титрантов при количественном определении металлов. Впервые использовать комплексоны в аналитической химии предложил в 1949 г. швейцарский ученый Г.Шварценбах.
Наиболее распространенными комплексонами являются слабая четырехосновная этилендиаминтетрауксусная кислота и дигидрат её динатриевой соли (комплексон ЭДТА, Na2H2Y·2H2O, торговое название «Трилон Б»):
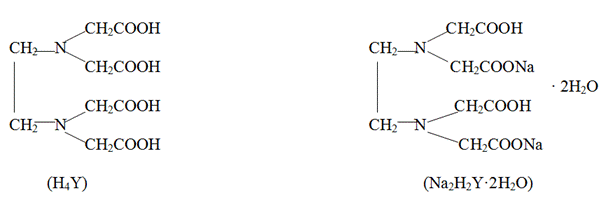
Именно Трилон Б используется в реакции комплексонометрического титования меди. При этом - комплексонаты практически всех металлов бесцветны и хорошо растворимы в воде.
Как говорилось выше, в методе комплексонометрического титрования основным рабочим раствором является раствор дигидрата динатриевой соли этилендиаминтетрауксусной кислоты, которая выпускается промышленностью под торговым названием «трилон Б» со степенью очистки «ХЧ» (химически чистый) или «ЧДА» (чистый для анализа). Трилон Б хорошо растворим в воде и его растворы устойчивы при хранении. Рабочий раствор трилона Б можно готовить по точной навеске (с учетом влажности образца), однако обычно его точную концентрацию определяют по стандартному раствору сульфата).
Исходя из всего выше сказанного, реакция между ионом меди и трилоном Б может быть коротко записана в следующем виде:
Cu2+ + H2Y2- « CuY2- + 2H+
Комплексон III, как и другие комплексоны, образует растворимые внутрикомплексные соли со многими металлами. При этом металл замещает атомы водорода карбоксильных групп –COOH, а так же связывается координационной связью с атомами азота:
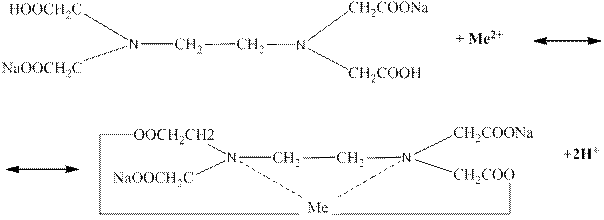
При этом следует отметить ряд особенностей протекания реакции, благодаря которым комплексонометрия получила широкое применение в химическом анализе:
1. в результате реакции образуются комплексы только одного состава с соотношением металл:лиганд равным 1:1 (комплексонаты); при этом комплексонаты бесцветны, хорошо растворимы в воде и обладают высокой устойчивостью, так как центральный атом металла прочно связан полидентатным хелатным лигандом;
2. реакция является обратимым процессом и может быть сдвинута как в сторону образования, так и в сторону разрушения комплексоната, что легко достигается с помощью варьирования величины рН раствора – подкисление приводит к смещению равновесия влево к исходным реагентам, а подщелачивание способствует образованию комплексоната;
3. в результате реакции выделяются ионы водорода, поэтому её следует проводить в буферной среде, поддерживая оптимальное значение рН, определяемое константой устойчивости комплексоната.
Внутренний электролиз
Метод внутреннего электролиза, как и обычная электрогравиметрия, основан на пропускании тока через раствор пробы, выделении определяемого металла в свободном состоянии и определении массы металла. Однако в качестве источника тока здесь используется не электролизер, а создаваемый в ходе анализа внутренний гальванический элемент, включающий в себя платиновый катод, на котором выделяется определяемый металл, и анод, изготовленный из какого-либо материала, окислительно-восстановительный потенциал которого меньше потенциала определяемого элемента.
Рассмотрим непосредственно определение меди. Если в раствор CuSO4 поместить замкнутые накоротко платиновую сетку и цинковый стержень, то образуется гальванический элемент, в котором более активный металл отдает электроны и переходит в раствор:
Zn – 2e = Zn2+ .
Электроны переходят на платину и с нее передаются ионам меди, восстанавливая их:
Cu2+ + 2e = Cu .
В результате на платиновом катоде оседает металлическая медь, которую можно количественно определить по привесу электрода.
К недостаткам метода следует отнести возможность восстановления анализируемого элемента непосредственно материалом анода, в нашем примере:
Zn + Cu2+ = Zn2+ + Cu,
что приводит к образованию слоя меди, пассивирующего анод, и к потерям меди на анодную реакцию.
Этот процесс называется цементацией анода. Поскольку при цементации на катоде выделяется не вся медь, количественный анализ по привесу катода становится невозможным. Существуют различные методы борьбы с цементацией. Это, в частности, отделение раствора у катода (католита) от анолита с помощью полупроницаемых мембран, использование отдельных сосудов для катода и анода (соединенных солевым мостиком) и т.п. Необходимо также тщательно следить за надежностью электрических контактов, т.к. разрыв цепи немедленно влечет за собой выделение меди на цинковом электроде. По этой же причине, начав процесс, нельзя вынимать электроды из раствора.
