Расчет относительной молекулярной массы
Мr(К3РО4) = 3 · Ar(К) + 1 · Аr(Р) + 4 · Аr(О) = 3 · 39 + 1 ·31 + 4 · 16 = 212
Значения Аr для каждого химического элемента указаны в периодической системе химических элементов Д.И. Менделеева
Определение молярной массы вещества
Молярная масса вещества численно равна относительной молекулярной массе, но имеет иной физический смысл и единицы измерения.
М (К3РО4) = 212 г/моль
Формулы для расчета количества вещества
ν = 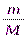 ν =
ν = 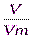 ν =
ν = 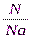
Основные законы химии
1. Периодический закон химических элементов Д.И. Менделеева (1869г.)
“Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от заряда ядра атома”.
2. Закон А. Авогадро (1811 г.)
“В равных объемах различных газов при одинаковых внешних условиях содержится одинаковое число молекул”.
3. Закон постоянства состава (Ж. Пруст, 1808 г.)
“Каждое чистое вещество имеет постоянный качественный и количественный состав, который не зависит от способа и места получения”. Закон справедлив для веществ молекулярного строения.
4. Закон сохранения массы веществ (М.В. Ломоносов, 1748 г.)
“Масса веществ, вступивших в реакцию, равна массе продуктов реакции”.
В современной формулировке точнее говорить о сохранении массы и энергии веществ.
Умение решать расчетные задачи свидетельствует о высоком уровне усвоения дисциплины. Ниже по тексту и в конце пособия приведены основные типы расчетных задач, методы их решения и оформления
Расчет массовой доли химического элемента
Задача 1. Рассчитайте массовую долю атомов водорода в молекуле аммиака.
Дано: NH3
Найти: ω(Н) = ?
Решение.
Массовая доля рассчитывается как массы части к массе всего целого.
Примем за часть – массу атомов водорода, их в составе молекулы аммиака 3 штуки.
За целое примем массу всей молекулы аммиака.
ω(Н) = 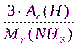 =
= 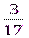 =
= 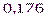
ω(Н) = 17,6%
Ответ: ω(Н) = 17,6%
Вывод химической формулы соединения по известным массовым долям химических элементов
Задача 2. Определите формулу медного колчедана, если в его составе содержится 34,8% меди, 30,4% железа и 34,8 % серы.
Дано: ω(Cu)=34,8% ω(Fe)=30.4% ω(S)=34,8%
Найти: Формулу CuxFeySz
Решение.
Так как состав вещества не зависит от массы или объема взятого образца, пусть взято 100 г исследуемого вещества, тогда
m(Cu) = 100 г · ω(Cu) : 100% = 34,8 г
m(Fe) = 30,4 г
m(S) = 34,8 г
Индексы x, у, z обозначают в искомой формуле число атомов каждого химического элемента или количество вещества атомов названных элементов.
x = ν(Cu) = 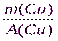 =
= 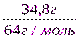 =
= 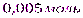
y = ν(Fe) = 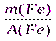 =
= 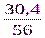 =
= 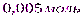
z = ν(S) = 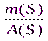 =
= 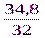 =
= 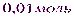
Находим соотношение числа атомов меди,
железа и серы:
x:y:z = 0,005 : 0,005 : 0,01 = 1 : 1 : 2
(Целые числа получили при делении каждого значения на меньшее из них).
Следовательно, состав формулы медного колчедана CuFeS2
Ответ: CuFeS2
