Методика работы на фотоэлектроколориметре
ПРИНЦИП МЕТОДА
Фотометрические методы анализа основаны на зависимости между интенсивностью окраски раствора и концентрацией вещества. Зависимость величины аналитического сигнала от концентрации выражается уравнением основного закона светопоглощения (закон Бугера-Ламберта-Бера):
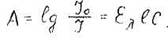
где А - оптическая плотность раствора;
I0 - интенсивность падающего потока;
I - интенсивность прошедшего потока света через поглощающий раствор;
l - толщина поглощающего слоя, см;
С - концентрация поглощающего вещества, моль/л;
ελ - молярный коэффициент поглощения.
Сульфосалициловая кислота образует с ионами Fe3+ окрашенные комплексные соединения разного состава и цвета в зависимости от рН раствора.
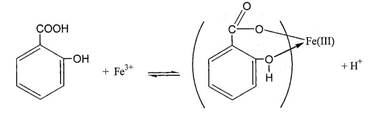
В кислой среде при рН I,8-2,5 образуется моносульфосалицилат железа красно-фиолетового цвета, при рН 4,0-8,0 - дисульфосалицилат железа(III) красно-бурого цвета и в интервале рН 8,0-11,5 - трисульфосалицилат железа желтого цвета. При рН > 13 комплекс разрушается с образованием основных солей и гидроксида железа (III).
Железо (III) определяют в кислой среде в виде моносульфосалицилатного комплекса, а в щелочной среде в виде трисульфосалицилата определяют суммарное содержание железа (III) и железа (II), так как ион Fe2+ окисляется кислородом воздуха. Трисульфосалицилатный комплекс железа (III) достаточно устойчив и позволяет проводить определение железа в присутствии ацетат-, борат-, фосфат- и фторид-ионов. Ионы Al (III), Sn (II) и некоторые другие образуют бесцветные комплексы, не мешающие определению железа (III). В этом случае прибавляют избыток реактива. Медь (II) образует менее устойчивый сульфосалицилатный комплекс и обнаружению железа (III) в кислой среде не мешает.
Обнаружение Fе3+ в виде сульфосалицилатного комплекса
Выполнение реакции. К 3-5 каплям анализируемого раствора прибавляют 3-5 капель раствора сульфосалициловой кислоты; Появление буро-филетовой окраски (если рН=2) указывает на присутствие Fe3+ в растворе. Если окраски нет, то наличие Fe3+ в растворе не исключено, так как рН раствора может быть меньше 1 (что не фиксируется универсальным индикатором), в растворе могут быть бесцветные комплексы железа(III). К раствору прибавляют по каплям раствор концентрированного NH4OH до рН = 10. Появление желтой окраски указывает на присутствие железа (III). Параллельно ставят контрольный опыт.
Определение железа (III) фотоколориметрическим методом
Построение градуировочного графика
В мерные колбы вместимостью 50 мл помещают 0,5; 1; 1,5; 2,0; 2,5; 3,0 мл стандартного рабочего раствора, содержащего 0,1 мг/мл железа (III), 1 мл 1 М раствора серной кислоты, 5 мл раствора сульфосалициловой кислоты, разбавляют водой до метки и перемешивают.
Раствором сравнения служит раствор не содержащий железо. Оптическую плотность растворов измеряют на фотоэлектроколориметре в кювете с толщиной поглощающего слоя 5 см относительно раствора сравнения при λ = 510 нм. По найденным значениям оптических плотностей строят градуировочный график. Параметры градуировочного графика выражают по методу наименьших квадратов для зависимости: у = а + b·х с применением программируемого микрокалькулятора.
Проведение анализа
Анализируемый раствор, содержащий железо, помещают в мерную колбу вместимостью 50 мл, прибавляют 1мл 1 М раствора серной кислоты, 5 мл раствора сульфосалициловой кислоты, доводят до метки дистиллированной водой; и перемешивают. Далее измерение оптической плотности раствора проводят, как указано при построении градуировочного графика. Содержание железа (III) в мг находят по градуировочному графику.
Методика работы на фотоэлектроколориметре
Колориметр фотоэлектрический концентрационный КФК-2
Однолучевой фотоколориметр предназначен для измерения пропускания Т, оптической плотности А и концентрации окрашенных растворов, рассеивающих взвесей, эмульсий и коллоидных растворов в области 315 - 980 нм. Пределы измерения пропускания 100 - 5 % (А= 0 ÷ 1,3). Основная абсолютная погрешность измерения пропускания 1%. Среднее квадратическое отклонение определения пропускания по результатам 10 измерений не превышает Sr = 0,3 % (О,003).
Блок-схема прибора:
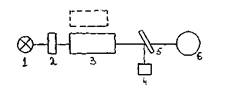
1 - источник света;
2 - светофильтр;
3 - кювета с исследуемым раствором или раствором сравнения;
4 - фотодиод (при измерениях в области 590-980);
5 - пластина, которая делит световой поток на 2 потока;
6 - фотоэлемент (при измерениях в области спектра 315-540нм).
Порядок измерений на фотоэлектроколориметре КФК-2
1. С помощью шнура и выключателя 2 «сеть» включают прибор (см. рис. 1) в сеть за 15 мин до начала измерений и прогревают при открытой крышке кюветного отделения. Если необходимо, корректируют установку стрелки микроамперметра на нуль по шкале коэффициентов пропускания (верхняя шкала) с помощью потенциометра «нуль», выведенного под шлиц (на рисунке не указано).
2. С помощью ручки 3 вводят необходимый светофильтр.
3. Устанавливают минимальную чувствительность прибора. Для этого ручку 5 ставят в положение «1» и ручки 6 - в крайнее левое положение. При этом положения «1», «2», «3» ручки 5, отмеченные на лицевой панели черным цветом, должны использоваться при работе со светофильтрами в области 315-540 нм, а положения «1», «2», «3», отмеченные красным цветом, - при работе со светофильтрами в области 590-980 нм.
4. В кюветное отделение помещают кюветы с исследуемым раствором и с раствором сравнения. Кювету с раствором сравнения устанавливают в дальнее положение кюветодержателя. Кювету с анализируемым раствором устанавливают в ближнее положение. Крышку кюветного отделения закрывают.
| Рисунок 1 Внешний вид колориметра КФК-2: 1 – шкала регистрирующего прибора; 2 – кнопка включения прибора в сеть; 3 – ручка переключения светофильтров; 4 – ручка перемещения кювет; 5 – ручка включения фото-приемников; 6 – ручки установки 100%-го свето-пропускания; 7 – крышка кюветного отделения. | 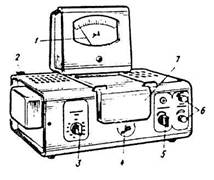 |
5. Ручкой 4 в световой поток вводят кювету с раствором сравнения и ручками 6 и 5 устанавливают отсчет «100» по верхней шкале микроамперметра.
6. Поворотом ручки 4 заменяют кювету с раствором сравнения кюветой с исследуемым раствором и снимают отсчет по шкале коэффициентов светопропускания (верхняя шкала) или в единицах оптической плотности (нижняя шкала).
ЛИТЕРАТУРА
1. Практическое руководство по физико-химическим методам анализа / Под ред. И.П. Алимарина, В.М. Иванова. - М.: Изд-во Моск. ун-та, 1981. -С. 58.
2. Методические указания к выполнению лабораторных работ по аналитической химии /Сост.: И.А. Шевчук, Т.Н. Симонова, Л.Я. Енальева, А.С. Алемасова, Т.С. Чагир-Галкина. - Донецк: ДонГУ, 1988. - С. 16-24.
3. Физико-химические методы анализа. Практическое руководство /Под ред. В.Б. Алесковского. -Л.: Химия, Ленингр. отд-ние, 1988. -С. 176-220.
