Опыт 2. Приготовление раствора заданной концентрации и проверка ее титрованием
Пример. Приготовить 100 мл 0,5 Н раствора NaOH из кристаллического NaOH.
1. Определить количество NaOH (m), необходимое для приготовления заданного раствора:
1000 мл – 20 г (0,5 Н) МNaOH = 40
100 мл – m m = 2 г.
2. Взвесить 2 г NaOH, перенести в стакан и добавить примерно 60 мл воды. Стеклянной палочкой тщательно перемешать раствор до полного растворения щёлочи. Раствор перелить в мерную колбу на 100 мл. Стакан сполоснуть небольшим количеством воды (~ 15 мл) и прилить её в ту же колбу с помощью воронки. Объём раствора в цилиндре довести до 100 мл (до метки) и тщательно перемешать.
3. Из мерной колбы отобрать пипеткой 10 мл приготовленного раствора и перенести его в коническую плоскодонную колбу для титрования. В колбу добавить 2…3 капли индикатора (метилоранж) и титровать раствором соляной кислоты до перехода желтого окрашивания раствора в розовый. Титрование повторить три раза, каждый раз точно определяя объем израсходованной кислоты (V1,V2,V3). Затем рассчитать средний объём
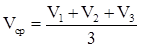 .
.
4. Число грамм-эквивалентов щёлочи в объёме пипетки (10 мл) равно чис-лу грамм-эквивалентов кислоты в объёме Vс.р.. По формуле Vm . Nm = Vk . Nk определить нормальную концентрацию приготовленного раствора щелочи. Сравнить полученные результаты с заданием.
Контрольные вопросы и упражнения
1. Что такое растворы?
2. Что такое компонент раствора? Из каких компонентов состоят растворы? В каких агрегатных состояниях могут находиться компоненты раствора?
3. Дайте определение процессов гидратации и сольватации при растворении.
4. Охарактеризуйте следующие свойства растворов: давление пара над раствором, температуры кипения и замерзания.
5. Какой раствор называется: разбавленным, концентрированным, насыщенным, ненасыщенным, пересыщенным?
6. Что показывает коэффициент растворимости?
7. Назовите условие выпадения из растворов осадков малорастворимых электролитов.
8. Что выражает величина, называемая концентрацией раствора?
9. Дайте определение молярности, моляльности, нормальности, титра, мольной доли и процентной концентрации.
10. Сколько нужно взять гидроксида калия, чтобы приготовить 500 г 8 %-го водного раствора?
11. Сколько граммов соды Na2CO3 нужно, чтобы приготовить 2 л 0,2 М раствора?
12. В 200 г воды растворили 6,37 г хлорида магния. Определите моляльную концентрацию раствора.
13. В 200 мл воды растворили 20 г нитрата калия. Определить массовую долю (%) KNO3 .
14. Какую массу (г) 15 % раствора хлорида кальция можно приготовить, имея 170 мл воды?
15. В 175 мл воды растворили 25 г CuSO4 . 5H2O. Какая массовая доля (%) CuSO4 в полученном растворе?
16. Какой объем (мл) 94 % раствора серной кислоты (пл.1,837 г/мл) требуется для приготовления 1 л 20 % раствора (пл.1,143 г/мл)?
17. Какую массу (г) сульфата натрия надо добавить к 300 г 10 % раствора, чтобы получить 20 % раствор ?
18. В 200 мл воды растворили 5,6 л хлороводорода (н.у.). Определить массовую долю (%) хлороводорода в полученном растворе.
19. Какая масса (г) нитрата калия содержится в 2 л 0,1 М раствора нитрата калия?
20. Определить молярную концентрацию раствора, содержащего 14 г гидроксида калия в 500 мл раствора.
21. Какой объём (мл) 0,2 М раствора гидроксида калия требуется, чтобы осадить в виде Fe(OH)3 всё железо, содержащееся в 29 мл 1,4 М раствора хлорида железа (III) ?
22. Теплота растворения безводного сульфата натрия равна –80,3 кДж/моль, а теплота растворения кристаллогидрата сульфата натрия Na2SO4.10Н2О равна –78,7 кДж/моль. Вычислить теплоту гидратации Na2SO4.
23. Определить теплоту гидратации безводного сульфата цинка, если известно, что теплота его растворения 77,11 кДж, а теплота растворения ZnSO4.7H2O равна –17,67 кДж.
24. К 0,05 л раствора сульфида стронция с молярной концентрацией 0,002 моль/л прилит равный объём раствора сульфата магния с концентрацией 0,004 моль/л. Выпадет ли осадок сульфата стронция ?
Ионообменные реакции
Реакции в растворах электролитов, при которых не изменяется заряд ионов, входящих в соединения, называются ионообменными. Например, взаимодействие электролитов в состоянии равновесия
К1А1 + К2А2 D К1А2 + К2А1.
Константа равновесия
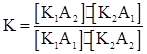 (4)
(4)
Чтобы узнать, в какую сторону смещено данное равновесие, рассмотрим диссоциацию каждого из 4-х электролитов:
К1А1⇆К1⁺ + А 1 - 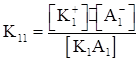 ;
;
К2А2⇆К2⁺ + А2⁻ 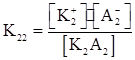 ;
;
К1А2⇆К1⁺+А2⁻ 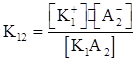 ;
;
К₂А₁⇆К₂⁺+А₁⁻ 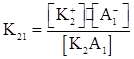 .
.
Подставляя в уравнение (4) вместо концентраций значения К, получим
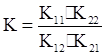 .
.
Если К>1, т.е. К₁₁· К₂₂>К₁₂·К₂₁, то равновесие смещено вправо (легче идёт прямая реакция).
Если К<1,т.е. К₁₁·К₂₂<К₁₂·К₂₁, то равновесие смещено влево (в сторону обратной реакции).
При К→ ∞ реакция будет необратимой.
Равновесие в ионообменных реакциях смещается в сторону образования наименее диссоциированных соединений.
Ионообменные реакции протекают в растворах электролитов в следующих случаях:
1) если образуется осадок трудно растворимого вещества;
2) если образуется газ (легколетучее вещество);
3) если образуется слабый электролит (плохо диссоциирующее соединение);
4) если образуется комплексный ион.
В уравнениях ионных реакции формулы сильных электролитов записывают в диссоциированном виде, слабых – в недиссоциированном.
Примеры:
1.Образование осадков:
AgNO3 + NaCl = AgCl↓ + NaNO3;
Ag+ + NO₃¯ + Na+ + CI¯ = AgCl + Na+ + NO₃¯;
Ag+ + Cl¯ = AgCl.
2. Образование газов:
Na₂S + H₂SO₄ = Na2SO4 + H2S↑;
2 Na+ + S²¯+2 H+ + SO₄²¯ = H2S↑ + 2 Na+ + SO₄²¯ ;
2 H+ + S²¯= H₂S↑.
3. Образование слабых электролитов. Чаще всего это – образование воды,
слабого основания или слабой кислоты:
а) образование воды:
NaOH + HCl = H₂O + NaCl ;
Na+ + OH⁻ + H+ + Cl⁻ = H₂O + Na+ + Cl⁻ ;
H+ + OH⁻ = H₂O;
б) образование слабого основания:
NH₄Cl + KOH = NH₄OH + KCl;
NH₄+ + Cl⁻ + K+ + OH⁻= NH₄OH + K++ Cl⁻;
NH₄+ + OH⁻ = NH₄ОН;
в) образование слабой кислоты:
2 CH₃COONa + H₂SO₄ = 2 CH₃COOH + Na₂SO₄;
2 CH₃COO⁻ + 2 Na+ + 2 H+ + SO₄²⁻ = 2 CH₃COOH + 2 Na+ + SO₄²⁻;
CH₃COO⁻ + H+ = CH₃COOH.
4. Образование комплексного иона (например, катиона)
CuSO₄ ∙ 4 H₂O + 4 NH₃ = [Cu(NH₃)₄]SO₄ + 4 H₂O;
[Cu(H₂O)₄]²+ + SO₄²⁻ + 4 NH₃ = [Cu(NH₃)₄]²+ + SO₄²⁻ + 4 H₂O.
Лабораторная работа
Ионообменные реакции
Цель работы
Получение сильных малорастворимых и слабых электролитов.
Оборудование и реактивы
Пробирки. Кусочек мела. Хлорид аммония (крист.). Рзбавленные растворы: хлорида бария, сульфата натрия, нитрата свинца, хлорида калия, йодида калия, соли железа (II), соли меди (II), сульфида аммония, ацетата натрия, дихромата калия, хлорида магния, аммиака, соляной и серной кислот.
