Нитрование концентрированной азотной кислотой
Метод нитрования концентрированной азотной кислотой используется значительно реже, чем нитрование нитрующей смесью.
Достоинство метода— не надо регенерировать серную кислоту.
Недостатками методаявляются: низкая концентрация нитроний-катиона; быстро теряется реакционная способность при разбавлении водой, выделяющейся в процессе нитрования; сильное окислительное действие азотной кислоты, которая более сильно по сравнению с нитрующей смесью реагирует с черными металлами; расход азотной кислоты обычно в 1,5 раза выше теоретического.
Однако, учитывая относительно невысокую цену на азотную кислоту, высокую стоимость и малый тоннаж многих лекарственных веществ, этот метод нитрования часто используют в химфармпредприятиях, на которых экономически невыгодно организовывать регенерацию отработанной серной кислоты
Метод применяют, как правило, для нитрования активированных аренов, либо для О-нитрования. Этим методом нитруют п-цимол, тетралин, ксилол. Первичные ароматические амины нитруют после защиты аминогруппы. Фенилуксусная и коричная кислоты нитруются, главным образом, в п-положение.
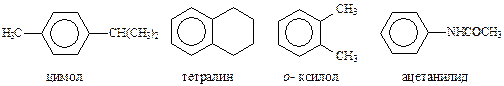
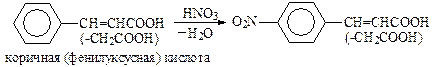
· В синтезе левомицетина концентрированную азотную кислоту используют при получении «нитроэфира» (С- и О-нитрование при 3 °С, «прямой слив»):
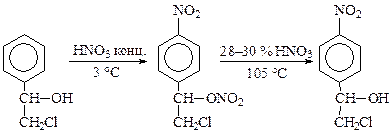
По другой методике получение нитроэфира ведут методом «обратного слива» в избытке азотной кислоты при температуре 8—12 °С. Дальнейшее повышение температуры нитромассы недопустимо, так как она может разлагаться со взрывом.
· При получении нитросорбида используют 98 %-ную азотную кислоту:
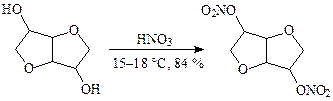
Устранение недостатков методасвязано, прежде всего, с уменьшением окислительных свойств кислоты и увеличением концентрации электрофильных частиц. Поэтому, чем выше концентрация азотной кислоты и ниже температура нитрования аренов, тем реакция идет быстрее и меньше сопровождается окислением. Кроме этого используют:
1. Кислоты Льюиса в качестве катализаторов для увеличения концентрации электрофильных частиц.
2. Нитрование азотной кислотой в среде инертного органического растворителя, чтопозволяет:
· уменьшить окислительное действие азотной кислоты, подбирая растворитель таким образом, чтобы в нем растворялись исходные вещества, и не растворялся продукт реакции;
· регулировать концентрацию нитроний-катиона, а, следовательно, и скорость реакции полярностью и количеством растворителя (чем более полярный растворитель, тем быстрее идет реакция);
· катализировать процесс добавлением небольших количеств сильных кислот. Например, добавка 0,001 моль/л H2SO4 увеличивает скорость нитрования бензола в нитрометане в 2 раза, а 0,01 — в 30 раз.
Необходимо при этом учитывать, что многие растворители, явно нереагирующие с азотной кислотой, образуют с ней комплексные соединения.
3. Нитрование концентрированной азотной кислотой с азеотропной отгонкой воды из реакционной массы идет при температуре кипения азеотропной смеси и постоянной концентрации электрофила. Нитрование проводится минимально необходимым количеством азотной кислоты.
