Аминокислоты, пептиды и белки
Аминокислоты – бесцветные кристаллические вещества, плавящиеся при температурах 200 – 320°С, часто с разложением. Они растворимы в воде, большинство нерастворимо в органических растворителях.
a-Аминокислоты являются соединениями, из которых строятся молекулы белков. Белки играют роль опорных структур в живых организмах, транспортируют жиры в кровеносной системе, являются гормонами, ферментами, переносчиками кислорода из легких в ткани и др. Природные a-аминокислоты, входящие в состав белков, их названия и сокращенные обозначения приведены ниже. В общем виде их можно отобразить следующей формулой:
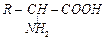 .
.
В зависимости от характера радикала R их можно разделить на 8 основных групп.
1. Моноаминокарбоновые кислоты R
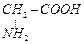 | глицин | glu | H - |
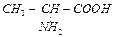 | аланин | ala | CH3 - |
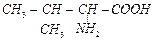 | валин | val | 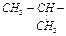 |
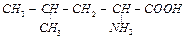 | лейцин | leu | 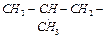 |
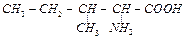 | изолейцин | ile | 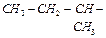 |
3. Моноаминодикарбоновые кислоты
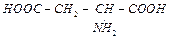 | аспаргиновая кислота | asp | НООС– СН2– | ||||
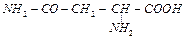 | аспаргин | asn | 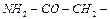 | ||||
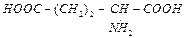 | глутаминовая кислота | glt | 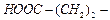 | ||||
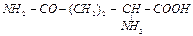 | глутамин | gln | 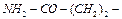 | ||||
3. Диаминокарбоновые кислоты
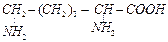 | лизин | lys | 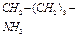 | ||
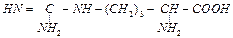 | аргинин | arg | 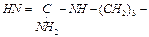 | ||
4. Оксиаминокислоты
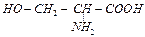 | серин | ser | 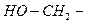 |
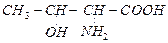 | треонин | thr | 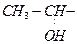 |
5. Меркаптоаминокислоты
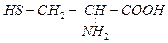 | цистеин | cys | 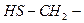 |
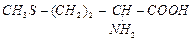 | метионин | met | 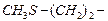 |
6. Ариламинокислоты
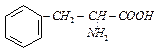 | фенилаланин | phe | 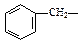 | |
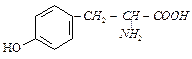 | тирозин | tyr | 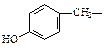 | |
7. Гетероалкиламинокислоты
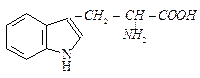 | триптофан | try | 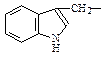 |
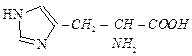 | гистидин | his | 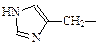 |
8. Гетероциклическая кислота
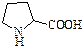 | пролин | pro |
Химические свойства
Аминокислоты – амфотерные соединения, сочетающие свойства слабых органических кислот и слабых оснований:
H2N–CH2–COOH + NaOH ® H2N–CH2–COONa + H2O
H2N–CH2–COOH + HCl ® Cl–H3N+–CH2–COOH
Растворы аминокислот имеют нейтральную реакцию: при растворении в воде аминогруппа реагирует с карбоксильной группой той же молекулы с образованием биполярного иона – внутренней соли: H2N–CH2–COOH  H3N+–CH2–COO–.
H3N+–CH2–COO–.
Поведение аминокислот при нагревании сходно с таковым для оксикислот: a-аминокислоты
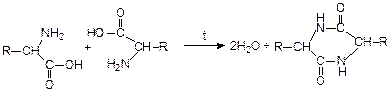
b-аминокислоты
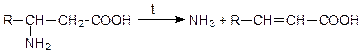
остальные аминокислоты
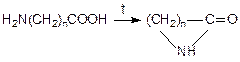
Белки – это полимеры аминокислот, полученные в результате конденсации.
Продукт конденсации двух аминокислот – дипептид:
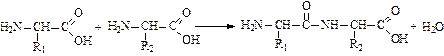
Группа атомов 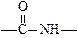 называется пептидной (или амидной), а связь между ними – пептидной связью.
называется пептидной (или амидной), а связь между ними – пептидной связью.
Дипептид может дальше реагировать с аминокислотами, образуя длинные полипептидные цепочки, содержащие более 40 остатков аминокислот, – белки. Их также называют полипептидами, потому что в молекулах многократно повторяется пептидная группа. Молярные массы белков лежат в пределах от 10000 до нескольких миллионов. В состав природных белков входят 20 a-аминокислот. Часть из них может быть синтезирована организмом (заменимые аминокислоты), другая поступает в организм только с пищей (незаменимые аминокислоты).
Порядок соединения аминокислот в молекулах белков называется первичной структурой белка. За счет внутримолекулярных водородных связей молекулы белков сворачиваются в спираль, образуя вторичную структуру белка. Спирали в свою очередь образуют вторичную спираль (третичная структура белка). Спирали могут объединяться попарно за счет межмолекулярных водородных связей, образуя четвертичную структуру.
В зависимости от формы макромолекул различают глобулярные (шаровидные) и фибриллярные (нитевидные) белки.
Под действием высоких температур, сильных кислот и щелочей, солей токсичных металлов, радиации четвертичная, третичная и вторичная структуры белков частично или полностью разрушаются, идет процесс денатурации белков.
При изменении кислотности среды (добавлении разбавленных растворов кислот или щелочей, не вызывающих денатурации) происходит их взаимодействие с концевыми амино- и карбоксильной группами. В более жестких условиях кислоты и щелочи вызывают гидролиз пептидов и белков (расщепление на исходные аминокислоты, которые реагируют с избытком кислоты или щелочи с образованием солей).
