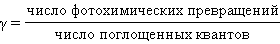Фотохимические реакции. Основные законы фотохимии. Кинетика фотохимических реакций
Реакции, протекающие под воздействием светового излучения, называются фотохимическими.
Основной закон фотохимии – закон квантовой эквивалентности А. Эйнштейн
(каждый поглощенный квант света hν вызывает изменение одной молекулы)
Важнейшим параметром фотохимической реакции служит квантовый выход γ:
|
В зависимости от типа фотохимической реакции квантовый выход может меняться в широких пределах. Это связано с возможностью потери поглощенной энергии до фотопревращения. Если время существования фотовозбужденной молекулы и скорость фотодиссоциации совпадают, то γ ~ 1. При γ >> 1 фотореакция идет по цепному механизму.
Типы фотохимических реакций:
1. Фотодиссоциация (фотолиз) приводит к разложению исходного вещества, поглотившего световую энергию. Примерами реакции фоторазложения служат такие: разложение галогенидов серебра (основа серебряной фотографии), фотолиз паров ацетона CH3CO CH3 → CO + другие продукты.
2. Фотосинтез приводит к образованию более сложных соединений. Примерами реакций фотосинтеза служат:
· фотосинтез озона в верхних слоях атмосферы, создающий защитный озоновый слой:
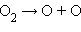 | фотодиссоциация |
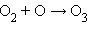 | фотосинтез |
- фотосинтез органических соединений из углекислого газа, воды, минеральных веществ зелеными растениями. В частности, синтез глюкозы может быть описан уравнением:
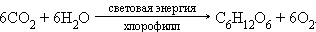 |
Фотохромизм– явление обратимого изменения пространственного или электронного строения молекул под действием света, сопровождающееся изменением окраски вещества. На основе фотохромных материалов изготовляются линзы с переменным светопропусканием, оконные стекла, фотохромные системы на основе некоторых органических и координационных соединений.
Кинетика фотохимических реакций описывается обычными дифференциальными уравнениями, выражающими закон действующих масс. Единственное отличие от обычных реакций с термическим возбуждением состоит в том, что скорость фотохимических процессов не зависит от концентрации исходного вещества, а в соответствии с законом фотохимической эквивалентности определяется только интенсивностью поглощенного света.
Механизм и кинетика гомогенно-каталитических реакций. Кислотно-основной катализ.
При гомогенном катализе катализатор и реагенты находятся в одной фазе. Гомогенный катализ можно подразделить на кислотно-основный, окислительно-восстановительный, координационный и ферментативный.