Обмен белков и нуклеиновых кислот
Теоретические вопросы, которые необходимо знать для изучения данной темы.
Понятие об аминокислотах. Классификация аминокислот. Строение протеиногенных аминокислот. Физические и химические свойства аминокислот. Амфотерные свойства аминокислот. Образование пептидов. Понятие о белках, их распространение в природе. Функции белков в организме животных. Строение белков. Элементарный состав. Уровни структурной организации белковой молекулы. Первичная, вторичная и третичная структуры. Олигомерные белки и четвертичная структура. Типы связей в молекулах белков (пептидная, водородная, дисульфидная, ионная, водородная) и их роль в формировании структуры белка. Физико-химические свойства белка (молекулярная масса, растворимость, заряд белковой молекулы, онкотическое давление, амфотерные и буферные свойства). Классификация белков. Характеристика отдельных групп простых белков (альбуминов, глобулинов, протаминов, гистонов, проламинов, глютелинов, склеропротеинов). Характеристика отдельных групп сложных белков белков (хромопротеинов, фосфопротеинов, гликопротеинов, липопротеинов, нуклеопротеинов).Понятие о нуклеиновых кислотах, их классификация и биологическая роль. Состав, строение и биологическая роль ДНК. Пуриновые и пиримидиновые азотистые основания ДНК. Дезоксирибонуклеозиды. Дезоксирибонуклеотиды и порядок их соединения в молекуле ДНК. Первичная структура ДНК. Вторичная структура ДНК. Правила Чаргаффа. Третичная структура ДНК. Состав, строение и биологическая роль РНК. Пуриновые и пиримидиновые азотистые основания РНК. Рибонуклеозиды. Рибонуклеотиды и порядок их соединения в молекуле ДНК. Первичная структура РНК. Вторичная и третичная структура РНК. Виды РНК и их биологическая роль. Переваривание белков в организме животных. Ферменты, участвующие в расщеплении белков в желудочно-кишечном тракте. Особенности переваривания белков у жвачных животных. Биохимические процессы, протекающие в толстом отделе кишечника. Пути использования аминокислот в организме животных. Понятие о гликогенных и кетогенных аминокислотах. Трансаминирование и его биологическая роль. Окислительное дезаминирование аминокислот и его биологическая роль. Декарбоксилирование аминокислот. Роль биогенных аминов для организма животных. Токсичность аммиака и пути его нейтрализации (образование аммонийных солей, амидирование аспарагиновой и глутаминовой кислот, синтез мочевины). Обмен сложных белков. Распад хромопротеинов в организме животных. Желчные пигменты. Катаболизм нуклеопротеинов. Конечные продукты распада пуриновых (АМФ, ГМФ) и пиримидиновых (ЦМФ, УМФ) рибонуклеотидов. Биосинтез белка. Компоненты белоксинтезирующей системы. Краткая характеристика основных стадий синтеза белка (инициации, элонгации, терминации).
Диссоциация аминокислот
О
// нейтральная среда
Н3С¾СН¾С биполярный ион
½ \
NH3+ О-
½НОН
О ОН- О Н+ О
// // //
Н3С¾СН¾С ¾¾ Н3С¾СН¾С ¾¾® Н3С¾СН¾С
½ \ ½ \ ½ \
NH2 О- NH2 ОН NH3+ ОН
анион аминокислоты катион аминокислоты
(в щелочной среде) (в кислой среде)
Аминокислоты обладают амфотерными свойствами поскольку могут проявлять как кислотные так и основные свойства. Кислотные свойства проявляются по карбоксильной группе а основные – по аминогруппе. В нейтральной среде аминокислоты диссоциируют по обеим функциональным группам: по карбоксильной с образованием карбоксил-аниона а по аминогруппе – с образованием замещенного аммонийного катиона. В процессе диссоциации моноаминокарбоновых аминокислот образуется биполярный ион.
В щелочной среде (рН>7) диссоциация по аминогруппе подавлена, при этом происходит диссоциация только карбоксильной группы с образованием отрицательно заряженного аниона. В кислой среде (рН<7) подавлена диссоциация карбоксильной группы, при этом диссоциирует аминогруппа с образованием положительно заряженного аммонийного катиона. В процессе электрофореза положительно заряженные катионы пойдут к катоду, а отрицательно заряженные анионы - к аноду. Диссоциация функциональных групп в аминокислотных остатках также будет определять заряд образующегося белка.
Образование пептидной связи
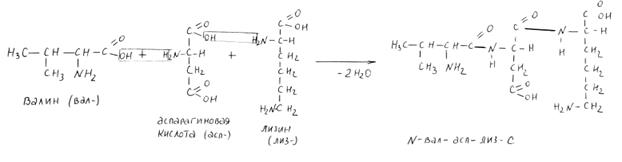
валиласпартиллизин
Пептидная связь образуется за счет атомов водорода a-аминогруппы и гидроксила карбоксильной группы при этом образуются пептиды. Название пептидов складывается из названий входящих в него аминокислот. В аминокислотах, у которых в образование пептидной связи произошло по карбоксильной группе, в названиях вместо окончания -ин появляется - ил. Название С- концевого остатка аминокислоты (свободная карбоксильная группа) не меняется.
Задания для контрольной работы:
72.Приведите классификацию аминокислот по различным признакам. Приведите по два представителя на каждую классификационную единицу.
73.Приведите примеры реакций диссоциации аминокислот в кислой, нейтральной и щелочной среде каждой классификационной группы.
74.Приведите уравнения реакций для глицина и назовите полученные продукты: а) диссоциация в нейтральной, кислой и щелочной средах; б) последовательное взаимодействие с аспарагиновой кислотой и серином.
75.Приведите уравнения реакций для α-аланина и назовите полученные продукты: а диссоциация в нейтральной, кислой и щелочной средах ; б) последовательное взаимодействие с глутаминовой кислотой и валином.
76.Приведите уравнения реакций для аспарагиновой кислоты и назовите полученные продукты: а) диссоциация в нейтральной и кислой средах; б) последовательное взаимодействие с лизином и метионином.
77.Приведите уравнения реакций для валина и назовите полученные продукты: а) диссоциация в нейтральной, кислой и щелочной средах; б) последовательное взаимодействие с аспарагиновой кислотой и фенилаланином.
78.Приведите уравнения реакций для треонина и назовите полученные продукты: а) диссоциация в нейтральной, кислой и щелочной средах; б) последовательное взаимодействие с аргинином и триптофаном.
79.Приведите уравнения реакций для гистидина и назовите полученные продукты: а) диссоциация в нейтральной, кислой и щелочной средах; б) последовательное взаимодействие с глутаматом и валином; в) декарбоксилирование. Укажите биологическую роль продукта данной реакции.
80.Приведите уравнения реакций для глутаминовой кислоты и назовите полученные продукты: а) диссоциация в нейтральной, кислой и щелочной средах; б) последовательное взаимодействие с лизином и метеонином.
81.Приведите уравнения реакций для серина и назовите полученные продукты: а) диссоциация в нейтральной, кислой и щелочной средах; б) последовательное взаимодействие с аспартатом и фенилаланином.
82.Приведите уравнения реакций для тирозина и назовите полученные продукты: а) взаимодействие с соляной кислотой; б) диссоциация в нейтральной, кислой и щелочной средах; в) последовательное взаимодействие с глутаминовой кислотой и валином.
83.Что такое белки? Перечислите основные функции, выполняемые ими в организме животных. Какие белки относят к полноценным, а какие к неполноценным? Приведите примеры полноценных и неполноценных белков.
84.Охарактеризуйте первичную, вторичную, третичную структуры белков. Почему не все белки имеют четвертичную структуру?
85.Приведите классификацию белков по различным признакам: а) по химической природе; б) по кислотно-основным свойствам. На каждую единицу классификации приведите примеры названий белков.
86.Охарактеризуйте альбумины и хромопротеины, их строение, физико-химические свойства и биологическую роль.
87.Охарактеризуйте глобулины и фосфопротеины, их строение, физико-химические свойства и биологическую роль.
88.Охарактеризуйте проламины и нуклеопротеины, их строение, физико-химические свойства и биологическую роль.
89.Охарактеризуйте глютелины и гликопротеины, их строение, физико-химические свойства и биологическую роль.
90.Охарактеризуйте гистоны и липопротеины, их строение, физико-химические свойства и биологическую роль.
91.Приведите структурную формулу пептида N-сер-глу-вал-асп –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
92.Приведите структурную формулу пептида N-вал-асн-фен-тре –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
93.Приведите структурную формулу пептида N-асп-цис-ала-тре –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
94.Приведите структурную формулу пептида N-сер-ала-вал-тир –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
95.Приведите структурную формулу пептида N-сер-лиз-цис-асп –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
96.Приведите структурную формулу пептида N-лиз-тре-вал-арг –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
97.Приведите структурную формулу пептида N-арг-глу-вал-сер –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
98.Приведите структурную формулу пептида N-глу-вал-асп -три–С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
99.Приведите структурную формулу пептида N-глу-глу-тре-асп –С. Приведите его диссоциацию в нейтральной среде. Укажите полюс электрода, к которому он будет двигаться при электрофорезе.
100.Приведите все возможные пути нейтрализации токсичности аммиака в организме сельскохозяйственных животных.
101.Приведите возможные пути превращения пировиноградной кислоты и вовлечение её в обмен липидов и углеводов.
102.Приведите структурную формулу аденозинмонофосфата (АМФ) и назовите его составные компоненты.
103.Приведите структурную формулу гуанозинмонофосфата (ГМФ) и назовите его составные компоненты.
104.Приведите структурную формулу цитидинмонофосфата (ЦМФ) и назовите его составные компоненты.
105.Приведите структурную формулу уридинмонофосфата (УМФ) и назовите его составные компоненты.
106. Приведите структурную формулу дезоксиаденозинмонофосфата (д-АМФ) и назовите его составные компоненты.
107.Приведите структурную формулу дезоксигуанозинмонофосфата (д-ГМФ) и назовите его составные компоненты.
108.Приведите структурную формулу дезоксицитидинмонофосфата (д-ЦМФ) и назовите его составные компоненты.
109.Приведите структурную формулу динуклеотида, состоящего из АМФ и ЦМФ.
110.Приведите структурную формулу динуклеотида, состоящего из ГМФ и ЦМФ.
111.Приведите структурную формулу динуклеотида, состоящего из УМФ и АМФ.
112.Приведите структурную формулу динуклеотида, состоящего из ЦМФ и ГМФ.
113.Приведите конечные продукты обмена нуклеиновых кислот в организмах сельскохозяй- ственных животных. Приведите химизм катаболизма одного из азотистых оснований нуклеиновых кислот.
114.Укажите все возможные виды РНК и охарактеризуйте их роль в организме животных.
115.Охарактеризуйте строение первичной, вторичной структур ДНК и РНК.
116.Вторичная структура ДНК. Принцип комплементарности. Правила Чаргаффа.
117.Дайте определения понятиям «ген», «транскрипция», «трансляция». Укажите биологи-
ческую роль ДНК.
118.Дайте понятие об азотистом балансе. В каких физиологических состояниях он становится отрицательным? Каково его значение в ветеринарии?
119.Приведите схему переваривания белков в желудочно-кишечном тракте животных. Укажите ферменты, участвующие в этом процессе.
120.Охарактеризуйте процессы дезаминирования аминокислот в клетке. Приведите схемы возможных путей данного процесса. В какие процессы обмена веществ могут включаться безазотистые остатки аминокислот?
121.Приведите схему трансаминирования аминокислот. Какова роль a-кетоглутарата в дан ном процессе?
122.Приведите возможные пути нейтрализации аммиака в организме животных. Укажите биологическую роль орнитинового цикла.
123.Приведите схему реакции декарбоксилирования гистидина. Укажите биологическую роль продукта реакции.
124.Приведите схемы реакций декарбоксилирования аспарагиновой и глутаминовой кислот. Укажите биологическую роль продуктов реакций.
125.Дайте понятие о глюкогенных и кетогенных аминокислотах. В каких процессах могут использоваться безазотистые остатки глюкогенных и кетогенных аминокислот? Приведите примеры представителей каждой группы и возможные пути включения их безазотистых остатков в обмен веществ.
126.Укажите возможные пути использования фенилаланина в организме животных.
127.Укажите возможные пути использования цистеина в организме животных.
128.Приведите возможные пути включения в обмен веществ аспаргиновой и глутаминовой кислот. Назовите биологическое значение продуктов реакций.
129.Приведите схему катаболизма хромопротеинов на примере гемоглобина. Каково значение глюкуроновой кислоты в данном обмене. Назовите конечные продукты обмена.
130.Приведите схему катаболизма ГМФ. Укажите конечные продукты распада.
131.Приведите схему катаболизма ТМФ. Укажите конечные продукты распада.
132.Приведите схему катаболизма УМФ. Укажите конечные продукты распада.
