Качественная реакция на хлорид-ион
1. Нитрат серебра AgN03 с ионом С1~ дает белый творожистый осадок хлорида серебра:
NaCl + AgNOs = AgCl| -f NaN03, Cr + Ag+ = AgClj.
Осадок нерастворим в азотной кислоте, но легко растворяется в аммиаке с образованием комплексного соединения:
AgCl + 2NH3 = [Ag(NH3)2]Cl.
№39 кислородные соединения хлора.
Хлор образует четыре кислородсодержащие кислоты:хлорнотистую, хлористую, хлорноватую и хлорную. Хлорноватистая кислота НСlO НСlO = HСl + O
В присутствии водоотнимающих веществ образуется оксид хлора (I): 2 НСlO = 2 Н2О + Сl2O
Хлорная, или белильная, известь СаОСl2, или СаСl(СlO), образуется при взаимодействии хлора с порошкообразным гидроксидом кальция — пушенкой: Са(ОН)2 + Сl2 = Cl-O-Ca-Cl + H2O
Хлористая кислота НСlO2 НСlO2 + 3 НС1 = Сl2 + 2 Н2О
Хлорноватая кислота НСlO3 образуется при действии на ее соли — хлораты — серной кислоты. НСlO3 + 6 НВr = НСl + 3 Вr2 + 3 Н2О
№40 Общая характеристика элементов 6А группы периодической системы Менделеева. Характеристика серы, как простого вещества.
Общая характеристика: К элементам А-группы VI группы относятся кислород, сера, селен, теллур и радиоактивный полоний. Общая электронная конфигурация внешнего валентного слоя типа ns2nр4 обусловливает, прежде всего, окислительные свойства этих элементов, при переходе от кислорода к полонию их окислительная способность резко ослабляется. Наибольшей окислительной способностью в виде простых веществ обладают кислород и сера — типичные неметаллы.
Сера: элемент третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 16. Проявляет неметаллические свойства. В водородных и кислородных соединениях находится в составе различныхионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы вводе.
химические свойства: На воздухе сера горит, образуя сернистый ангидрид — бесцветный газ с резким запахом: 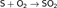
Расплав серы реагирует с хлором, при этом возможно образование двух низших хлоридов (дихлорид серы и дитиодихлорид) 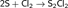
№41 Кислород: аллотропия, физические и химические своства, пременение.
Физ. Св-ва:При нормальных условиях кислород — это газ без цвета, вкуса и запаха.
Хим. Св-ва:Сильный окислитель, взаимодействует практически со всеми элементами, образуя оксиды. Степень окисления −2. Как правило, реакция окисления протекает с выделением тепла и ускоряется при повышении температуры. Пример реакций, протекающих при комнатной температуре: 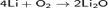
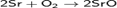
Окисляет соединения, которые содержат элементы с не максимальной степенью окисления:

Окисляет большинство органических соединений:

При определённых условиях можно провести мягкое окисление органического соединения:

Аллотропия:
№42 Сероводород: получение, свойсва, действие на организм.
бесцветный газ с запахом протухших яиц и сладковатым вкусом. Химическая формула — H2S. Плохо растворим в воде, хорошо — в этаноле. Ядовит. При больших концентрациях разъедает многие металлы. Концентрационные пределы воспламенения с воздухом составляют 4,5—45 % сероводорода.
Химические св-ва: Собственная ионизация жидкого сероводорода ничтожно мала. В воде сероводород мало растворим, водный раствор H2S является очень слабой кислотой:
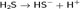 Ka = 6.9·10−7 моль/л; pKa = 6.89.
Ka = 6.9·10−7 моль/л; pKa = 6.89.
Реагирует со щелочами:
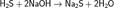 (обычная соль, при избытке NaOH)
(обычная соль, при избытке NaOH)
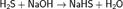 (кислая соль, при отношении 1:1)
(кислая соль, при отношении 1:1)
Сероводород — сильный восстановитель. На воздухе горит синим пламенем:
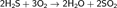
- Действие на организм: В медицине — в составе природных и искусственных сероводородных ванн, а также в составе некоторых минеральных вод.
№43 Оксид серы +4: получение, физическое и химическое свойство, применение
Получение: Промышленный способ получения — сжигание серы или обжиг сульфидов, в основном — пирита: 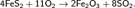
Хим. Св-во: Относится к кислотным оксидам. Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима): 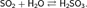
Со щелочами образует сульфиты: 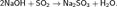
Физ. св-во: В нормальных условиях представляет собой бесцветный газ с характерным резким запахом (запах загорающейся спички). Под давлением сжижается при комнатной температуре
Применение: Большая часть оксида серы(IV) используется для производства серной кислоты. Используется также в виноделии в качестве консерванта (пищевая добавка E220). Так как этот газ убивает микроорганизмы, им окуривают овощехранилища и склады. Оксид серы(IV) используется для отбеливания соломы, шелка и шерсти, то есть материалов, которые нельзя отбеливать хлором.
№44 Оксид серы +6: получение , физическое и химическое свойство, применение.
Получение: Можно получить термическим разложением сульфатов:
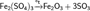
или взаимодействием SO2 с озоном:
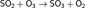
Для окисления SO2 используют также NO2:
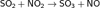
Химическое св-во: 1. Кислотно-основные: SO3 — типичный кислотный оксид, ангидрид серной кислоты. Его химическая активность достаточно велика. При взаимодействии с водой образует серную кислоту: 
Взаимодействует с основаниями: 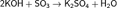
и оксидами: 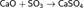
Применение: Серный ангидрид используют в основном в производстве серной кислоты.
№45 Тиосульфат натрия: получение, свойства, качественная реакция на тиосульфат-ион.
- Получение:окислением полисульфидов Na;
- кипячение избытка серы с Na2SO3:
S + Na2SO3 →(t) Na2S2O3;
- взаимодействием H2S и SO2 с NaOH (побочный продукт в производстве NaHSO3, сернистых красителей, при очистке промышленных газов от S):
4SO2 + 2H2S + 6NaOH → 3Na2S2O3 + 5H2O;
- кипячение избытка серы с гидроксидом натрия:
4S + 6NaOH → 2Na2S + Na2S2O3 + 3H2O
Химическое св-во:С сильными окислителями, например, свободным хлором, окисляется до сульфатов или серной кислоты:
Na2S2O3 + 4Cl2 + 5H2O → 2H2SO4 + 2NaCl + 6HCl. Более слабыми или медленно действующими окислителями, например, иодом, переводится в соли тетратионовой кислоты: 2Na2S2O3 + I2 → 2NaI + Na2S4O6.
Физ. св-во:Бесцветные моноклинные кристаллы.
качественная реакция на тиосульфат-ион:
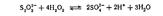
№46 Серная кислота: получение, физическое св-во, Кислотно- основные св-ва серной к-ты.
Физ. св-ва: Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с кислым «медным» вкусом
Получение:
Кислотно – основные св –ва:
№47 Окислительно-востоновительные св-ва концентрированной и разбавленной серной кислоты.
Конц:Концентрированная серная кислота очень активно взаимодействует с неметаллами. Реакцию растворения углерода в горячей концентрированной серной кислоте можно представить уравнением С + 2 Н2SO4 = СО2 + 2 SO2 + 2 Н2О
При окислении серы горячей концентрированной серной кислотой в качестве продукта окисления и продукта восстановления образуется диоксид серы: S + 2 Н2SO4 = 3 SO2 + 2 Н2О
Концентрированная серная кислота окисляет бромид — и иодид-ионы до свободных брома и иода:
2 КВг + 2 Н2SO4 = К2SО4 + SO2 + Вr2 + 2Н2О
2 КI + 2 Н2SО4 = К2SO4 + SO2 + 2 Н2О
Разб: В разбавленном водном растворе серной кислоты большинство ее молекул диссоциируют:
H2SO4 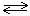 H+ + HSO4-
H+ + HSO4-
HSO4- 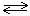 H+ + SO42-
H+ + SO42-
Образующиеся ионы Н+ выполняют функцию окислителя.
Как и соляная кислота, разбавленный раствор серной кислоты взаимодействует только с металлами активными исредней активности (расположенными в ряду активности до водорода).
Химическая реакция протекает по схеме:
Ме + H2SO4(разб.)→ соль + H2↑
Пример:
2 Al + 3 H2SO4(разб.) → Al2(SO4)3 + 3 H2↑
1│2Al0 – 6e- → 2Al3+ - окисление
3│2H+ + 2e- → H2 – восстановление
Металлы с переменной валентностью окисляются разбавленным раствором серной кислоты до низших положительных степеней окисления:
Fe0 → Fe2+
№48 соли серной кислоты, качественная реакция на сульфат-ион. Применение в медицине и народном хозяйстве.
Сульфа́ты — минералы, соли серной кислоты H2SO4. В их кристаллической структуре обособляются комплексные анионы SO42−. Наиболее характерны труднорастворимые сульфаты сильных двухвалентных оснований, особенно Ba2+, а также Sr2+ и Ca2+. Более слабые основания образуют основные соли, часто весьма неустойчивые (например сульфаты окисленного железа), более сильные основания — двойные соли и кристаллогидраты.
Кач реакция: Взаимодействие серной кислоты с хлоридом бария: H2SO4+BaCl=BaSO4(выпадает в осадок белого цвета)+2HCL Процесс взаимодействия ионов бария с сульфат-ионами приводит к образованию белого нерастворимого осадка BaSO4. Это качественная реакция на сульфат-ионы.
Применение:
Вопрос 49. Общая характеристика V А группы периодической системы Д.И Менделеева. Азот – простое вещество.
Строение внешнего электронного слоя … ns2np3

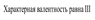





Азот, распространение в природе,
способы получения, физические и химические свойства.
Простое вещество состоит из двухатомных молекул N2, связь ковалентная неполярная, атомы связаны тройной связью
Характерные степени окисления: -3, 0, +1, +2, +3, +4, +5
Распространение в природе
Азот составляет около 4/5 атмосферного воздуха, т. е. 78,2% по объему.
Из соединений азота наибольшее значение имеет NaNO3 — чилийская селитра,
образующая большие залежи на тихоокеанском побережье Чили. В почве содержатся незначительные количества связанного азота.
Азот является составной частью белков.
Азот — четвёртый по распространённости элемент Солнечной системы (после водорода, гелия и кислорода).
Получение
1. в промышленности
Азот получают из жидкого воздуха, для этого воздух переводят в жидкое состояние и при температуре -1960С азот испаряется.
2. в лаборатории : а) разложение нитрита аммония при нагревании NH4NO2 = N2 ↑+ 2H2O
б) пропускание аммиака над оксидом меди (II) при температуре ~700°С 2NH3 + 3CuO → N2↑ + 3H2O + 3Cu
Физические свойства
При обычных условиях — газ без цвета, без запаха и вкуса, мало растворим в воде: 100 мл воды при 0°С растворяется 2,33 мл азота. В жидком состоянии (темп. кипения -195,8 °C) – бесцветная, подвижная, как вода, жидкость.
При -209,86 °C азот переходит в твердое состояние в виде снегоподобной массы или больших белоснежных кристаллов.
Химические свойства.
при обычных условиях азот реагирует только (!) с литием
6Li + N2 = 2Li3N (нитрид лития)
Азот N2 взаимодействует как окислитель:
1. с водородом N2 + 3H2 ↔ 2NH3 + Q
2. с металлами N2 + 3Ca = Са3N2
Азот N2 взаимодействует как восстановитель:
1. с кислородом (при очень высокой температуре, выше 1500°С) N2 + О2 = 2NO
(другие оксиды азота при взаимодействии с кислородом не образуются)
2. с фтором N2 +3F2 = 2NF3
Вопрос 50. Аммиак: получение, свойства, действие на организм.
Получение
1.в промышленности аммиак получают
прямым синтезом из азота и водорода
N2 + 3H2 = 2NH3
2. в лабораторных условиях аммиак получают
нагреванием солей аммония со щелочами:
(NH4)2SO4 + 2NaOH = Na2SO4 + 2NH3↑+ 2Н2О
2NH4C1 + Са(ОН)2 = СаС12 + 2NH3↑+ 2Н2О
Физические свойства
Аммиак — бесцветный газ с характерным запахом. Очень легко растворим в воде (в 1 л воды при 20°С растворяется 700 л NH3).
Водный раствор аммиака, содержащий 10 % NН3 - нашатырный спирт.
Химические свойства Кислотно-основные свойства Аммиак — слабое основание
1. взаимодействие с водой
NH3+ Н20 ↔ NH4ОН ↔ NH4+ + ОН-
2. газообразный аммиак взаимодействует с кислотами, образуя соли аммония:
NH3 + HC1 = NH4Cl
3. взаимодействие с солями некоторых металлов
с образованием комплексных соединений – аммиакатов CuSO4 + 4NH3 = [Cu(NH3)4]SO4
Химические свойства
Кислотно-основные свойства
Аммиак — слабое основание
1. взаимодействие с водой
NH3+ Н20 ↔ NH4ОН ↔ NH4+ + ОН-
2. газообразный аммиак взаимодействует с кислотами, образуя соли аммония:
NH3 + HC1 = NH4Cl
3. взаимодействие с солями некоторых металлов
с образованием комплексных соединений – аммиакатов CuSO4 + 4NH3 = [Cu(NH3)4]SO4
1. взаимодействие со щелочами
NH4C1 + NaОН = NаС1 + NH3↑ + Н2О
Качественная реакция на катион аммония NH4+,
выделяющийся аммиак определяют по запаху или по посинению лакмусовой бумажки
2. взаимодействие с солями
NH4C1 + AgNO3 = NH4NO3 + AgCl↓
Ag+ + C1- = AgCl↓
3. гидролиз NH4C1 + HOH ↔ NH4OH + H+ рН < 7, среда кислая
Действие на организм.
По физиологическому действию на организм относится к группе веществ ухудшающего действия способных вызвать токсический отек легких и поражение нервной системы.
Пары аммиака сильно раздражают слизистые оболочки глаза и органов дыхания, а также кожные покровы. Человек воспринимает, как резкий запах. Пары аммиака вызывают обильное слезотечение, боль в глазах, химический ожог роговицы, служит потерю сознания, приступы кашля, покраснение кожи.
Вопрос 51. Оксиды азота: получение, свойства.
Получение: Закись азота получают нагреванием сухого нитрата аммония. Разложение начинается при 170 градусах и сопровождается выделением тепла. Поэтому, чтобы не дать протекать ему слишком бурно, надо вовремя прекратить нагревание, т.к при температурах более 300 градусах нитрат аммония разлагается со взрывом.
NH4NO3=N2O+2H2O
В химической промышленности закись азота яв-ся побочным продуктом и для ее разрушения используют каталитические конвертеры, т.к выделение в виде товарного продукта, как правило экономически нецелесообразно.
Физические свойства.
Бесцветный газ, тяжелее воздуха ( относительная плотность 1,527) с характерным сладковатым запахом. Растворим в воде, этиловом спирте, эфире, серной кислоте. При 0 градусах и давлении 30 атомной массы, а также при комнатной температуре и давлении 40 атомн. Массы сгущается в бесцветную жидкость. Из 1 кг жидкой закиси азота образуется 500 л газа.
Химические свойства.
Относится к несолеобразующим оксидам, с водой, с растворами щелочей и кислот не взаимодействует. Не воспламеняется, но поддерживает горение. Смеси с эфиром, циклопропаном, хлорэтилом в определенных концентрациях взрывоопасны. В нормальных условиях N2O химически инертен, при нагревании проявляет свойства окислителя
N2O+H2=N2+H2O
N2O+C=N2+CO
При взаимодействии с сильными окислителями N2O может проявлять свойства восстановителя.
5N2O+8KMnO4+7H2SO4=5Mn(NO3)2+3MnSO4+4K2SO4+7H2O
При нагревании N2O разлагается
2N2O=2N2+O2
Вопрос 52. Азотная кислота: получение, кислотно-основные свойства.
Получение
1.в лаборатории действием концентрированной серной кислоты на безводные нитраты:
NaNO3 + H2SO4 = NaHSO4 + HNO3
2. в промышленности каталитическим окислением аммиака кислородом воздуха:
4NH3 + 5O2 = 4NO + 6H2O
2NO + O2 = 2NO2
4NO2 + 2Н2О + О2 = 4HNО3
Кислотно-основные свойства
1.в водных растворах полностью диссоциирует
НNO3 ↔ Н+ + NO3-
2. с оксидами металлов
MgO + 2HNO3 = Mg(NO3)2 + H2O
3. с основаниями
NaOH + HNO3 = NaNO3 + H2O
4. с солями более слабых кислот
Na2CO3 + 2HNO3 = 2NaNO3 + CO2 + H2O
Вопрос 53. Окислительно-восстановительные свойства концентрированной и разбавленной азотной кислоты.
1. с металлами
| Металлы | Основной продукт восстановления кислоты |
| Концентрированная HNO3 | |
| щелочные металлы (Na, K и др.), щелочноземельные металлы, магний, цинк и другие активные металлы | N2O или N2 |
| железо, алюминий, хром, золото, платина | не реагирует |
| Медь, серебро, свинец, висмут и другие малоактивные металлы | NO2 |
| Разбавленная HNO3 | |
| Щелочные металлы (Na, K и др.), щелочноземельные металлы, магний, цинк, железо и другие активные металлы | NH3 или NH4NO3 |
| Медь, серебро, свинец, висмут и другие малоактивные металлы | NO |
При взаимодействии азотной кислоты с металлами
водород не выделяется (!)
3Cu + 8HNO3(разб)= 3Cu(NO3)2 + 2NO +4H2O
4Ca + 10HNO3(конц) = 4Cа(NO3)2 + N2O +5H2O
Царская водка – смесь 1 часть азотной + 3 части концентрированной соляной кислоты.
Аu + HNO3 + ЗНС1 = AuCl3 + NO + 2H2O
2. с неметаллами
При нагревании с концентрированной азотной кислотой:
неметаллы окисляются до кислородных кислот,
азотная кислота восстанавливается до NO2 или NO
S + 2HNO3 = H2SO4 + 2NO
Р + 5HNO3 = Н3РО4 + 5NO2 + Н2О
Вопрос 54. Соли азотной и азотистой кислоты: свойства, применение.
