V1: Методы осадительного титрования
F1: Химические методы анализа
F2: Лебедева М.И.
V1: Методы осадительного титрования
I: {{1}}; II-1; k=A;
S: Требования, предъявляемые к реакциям в методах осадительного титрования:
-: осадок нерастворим и выпадает быстро, допустимо соосаждение;
-: осадок нерастворим и выпадает медленно, допустимо соосаждение;
-: осадок частично растворим и выпадает быстро, соосаждение недопустимо;
-: осадок нерастворим и выпадает быстро, соосаждение недопустимо.
I: {{2}}; II-1; k=A;
S: Вещество, применяемое в качестве стандартного в методе аргентометрии:
-: NaC1;
-: Nа2В4O7 • 10Н2О;
-: Н2С204 • 2Н2O;
-: АgNO3.
I: {{3}}; II-1; k=B;
S: Индикатор, используемый для установления титра раствора АgNОз методом Мора:
-: эриохромовый черный Т;
-: мурексид;
-: хромат калия
-: крахмал.
I: {{4}}; II-1; k=B;
S: Среда, необходимая для определения хлоридов методом Мора:
-: кислая или нейтральная;
-: нейтральная или слабощелочная;
-: сильнощелочная;
-: щелочная или слабокислая.
I: {{5}}; II-1; k=C;
S: Значение рСа в точке эквивалентности при титровании 0,05 М раствора СаС12 раствором Na2SO4 такой же концентрации при ПР(СаSO4)= 6 • 10–5, равно:
-: 1,80;
-: 2,11;
-: 1,05;
-: 4,22.
I: {{6}}; II-2; k=A;
S: Среда, необходимая для роданидометрического определения хлоридов и бромидов:
-: слабощелочная;
-: щелочная или нейтральная;
-: нейтральная;
-: кислая.
I: {{7}}; II-2; k=A;
S: Параметр, от которого зависит величина скачка на кривой титрования:
-: интервал перехода индикатора и исходные концентрации реагирующих веществ;
-: рН исходных растворов и ПРосадка;
-: исходные концентрации растворов и ПРосадка;
-: скорость образования осадка и полнота осаждения.
I: {{8}}; II-2; k=B;
S: Название вещества, используемого в качестве адсорбционного индикатора:
-: дифениламин;
-: эозин;
-: мурексид;
-: эриохромовый черный Т.
I: {{9}}; II-2; k=B;
S: Вещество, применяемое для установления титра раствора роданида аммония:
-: АgNО3;
-: КNO3;
-: NaС1;
-: К2СrO4.
I: {{10}}; II-2; k=C;
S: Формула для расчета [Cl–] при титровании NaС1 по методу Мора в точке эквивалентности:
-: [Cl–] = 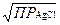 ;
;
-: [Cl–] = 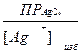 ;
;
-: [Cl–] = [Ag+];
-: [Cl–] = 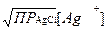 .
.
I: {{11}}; II-3; k=A;
S: Условие, позволяющее применять хромат калия в качестве индикатора при титровании хлоридов раствором нитрата серебра:
-: различие в величинах ПР(АgСl)и ПР(Аg2СгO4);
-: изменение [Cl–] в растворе;
-: изменение [H+] в растворе;
-: собственная окраска индикатора.
I: {{12}}; II-3; k=A;
S: Вещество, которое осаждается первым, если 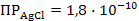 ;
;
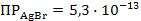 ;
; 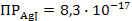 ;
; 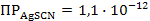 ;
;
-: хлорид серебра;
-: бромид серебра;
-: иодид серебра;
-: роданид серебра.
I: {{13}}; II-3; k=B;
S: Порядок титрования Аg+ – ионов методом Мора:
-: раствор NаС1 титруют раствором АgNО3;
-: раствор АgNОз титруют раствором NаС1;
-: раствор АgNОз может быть и титрантом, и титруемым раствором;
-: раствор К2СгO4 титруют раствором АgNОз.
I: {{14}}; II-3; k=B;
S: Индикатор, применяемый в методе Фольгарда:
-: Аg2СгO4;
-: К2СrO4;
-: FеNН4(SO4)2 • 12Н2O;
-: NH4SСN.
I: {{15}}; II-3; k=С;
S: Установить соответствие между концентрациями растворов AgNO3 при определении хлоридов:
L1: молярность (моль/ 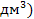 ;
;
L2: титр (г/ 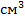 );
);
L3: нормальность (моль/ 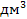 );
);
L4: титр по 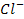 (г/
(г/ 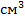 );
);
R1: 5,6 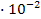 ;
;
R2: 9,5 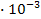 ;
;
R3: 5,6 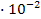 ;
;
R4: 2 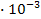 .
.
I: {{16}}; II-4; k=A;
S: Вещество, имеющее большую растворимость, если ПР(АgСl) и ПР(Аg2СгO4) равны 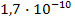 и
и 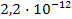 , соответственно:
, соответственно:
-: хлорид серебра;
-: обе соли нерастворимы в воде;
-: растворимость обеих солей одинакова;
-: хромат серебра.
I: {{17}}; II-4; k=A;
S: Условия, необходимые при титровании методом Фольгарда:
-: отсутствие окислителей, собственной окраски раствора и пептизирующих веществ, кислая среда;
-: присутствие окислителей и пептизирующих веществ, кислая среда;
-: собственная окраска раствора, нейтральная среда;
-: отсутствие окислителей и собственной окраски раствора, слабощелочная среда.
I: {{18}}; II-4; k=B;
S: Условия, не позволяющие применять эозин в качестве индикатора при определении хлоридов:
-: эозин адсорбируется слабее хлорид-ионов;
-: эозин адсорбируется сильнее хлорид-ионов;
-: хлорид-ионы и эозин адсорбируются одинаково;
-: хлорид-ионы не сорбируются индикатором.
I: {{19}}; II-4; k=B;
S: Стандартное вещество для установления титра АgNO3:
-: Na2С2O4;
-: NaC1;
-: Н2С2O4 • 2Н2O;
-: К2Сг2O7.
I: {{20}}; II-4; k=C;
S: Индикатор меркурометрического определения хлоридов:
-: крахмал;
-: дифенилкарбазон;
-: эозин;
-: дифениламин.
I: {{21}}; II-5; k=A;
S: Содержание серебра [% (масc.)] в анализируемом сплаве после растворения 0,30 г сплава в азотной кислоте, если на титрование полученного раствора расходуется 23,8 см3 0,1 М раствора NН4SСN, равно:
-: 63,4;
-: 39,2;
-: 60,3;
-: 85,6.
I: {{22}}; II-5; k=A;
S: Титр (г/см3) по хлориду калия 0,05605 М раствора АgNОз :
-: 0,06552;
-: 0,01638;
-: 0,00417;
-: 0,02082.
I: {{23}}; II-5; k=B;
S: Индикатор меркурометрического определения хлоридов:
-: роданид железа (III);
-: хромат калия;
-: дифенилкарбазон;
-: железоаммонийные квасцы.
I: {{24}}; II-5; k=B;
S: Заряд частиц АgС1, при титровании хлоридов раствором нитрата серебра, изменяется:
-: с положительного на отрицательный;
-: с отрицательного на положительный;
-: заряд частиц не изменяется;
-: частицы электронейтральны.
I: {{25}}; II-5; k=C;
S: Параметр, изменяющийся при увеличении рН раствора при титровании с адсорбционными индикаторами:
-: не влияет;
-: интенсивность окраски уменьшается;
-: интенсивность окраски возрастает;
-: влияние зависит от структуры индикатора.
I: {{26}}; II-6; k=A;
S: Значение рАg, если 25 см3 0,1 М раствора АgNО3 в момент, когда добавлено 24 см3 0,1 М раствора NaCl:
-: 1,05;
-: 2,69;
-: 4,20;
-: 3,60.
I: {{27}}; II-6; k=A;
S: ПР 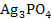 , если растворимость фосфата серебра составляет 4
, если растворимость фосфата серебра составляет 4 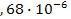 М:
М:
-: 2 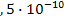 ;
;
-: 1 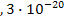 ;
;
-: 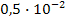 ;
;
-: 1 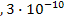 .
.
I: {{28}}; II-6; k=B;
S: Заряд частиц АgС1 при титровании раствора нитрата серебра раствором хлорида натрия изменяется:
-: с отрицательного на положительный;
-: с положительного на отрицательный;
-: частицы АgС1 электронейтральны;
-: заряд частиц не изменяется.
I: {{29}}; II-6; k=B;
S: Стандартное вещество в методе роданидометрии:
-: АgNО3;
-: КС1;
-: К2СrO4;
-: К2Сг2O7.
I: {{30}}; II-6; k=C;
S: Индикатор, для определения иодидов методом осаждения:
-: эозин;
-: хромат калия;
-: дифениламин;
-: крахмал.
I: {{31}}; II-7; k=A;
S: Индикатор, для определения хлоридов методом Фаянса:
-: эозин;
-: флуоресцеин;
-: эриохромовый черный Т;
-: дифениламин.
I: {{32}}; II-7; k=A;
S: Ионы, определяемые методом Мора:
-: Аg+, SСN–;
-: I–, SСN–;
-: Сl–, Вг –, Аg+;
-: С1–, SСN–.
I: {{33}}; II-7; k=B;
S: Условия при титровании хлоридов методом Мора:
-: рН=7; титрант – АgNO3;
-: рН=7; титрант – NH4SСN;
-: рН < 7; титрант – АgNO3;
-: рН > 7; титрант – NH4SСN
I: {{34}}; II-7; k=B;
S: Масса (г) хлорид-ионов в растворе, если на титрование 25 см3 раствора КС1 затрачивается 22 см3 раствора АgNO3 с титром 0,003588 г/см3 составляет:
-: 0,01794;
-: 0,01648;
-: 0,00725;
-: 0,03296.
I: {{35}}; II-7; k=C;
S: Требования к реакциям при осадительном титровании:
-: малое значение ПРи быстрое выпадение осадка;
-: большое значение ПРи медленное выпадение осадка;
-:быстрое выпадение осадка и наличие соосаждения;
-:наличие соосаждения и полное осаждение определяемого вещества.
I: {{36}}; II-8; k=A;
S: Стандартное вещество в методе Мора:
-: АgС1;
-: NaCl;
-: AgNO3;
-: Na2С2O4.
I: {{37}}; II-8; k=A;
S: Установите соответствие между ионом и индикатором, применяемым для его определения:
L1: иодиды;
L2: бромиды;
L3: хлориды
L4: роданиды;
R1: эозин;
R2: флуоресцеин;
R3: хромат калия;
R4: 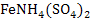 .
.
I: {{38}}; II-8; k=B;
S: Масса (г) NаС1 в 500 см3 раствора, если на титрование 25 см3 раствора NaС1 расходуется 22 см3 раствора AgNO3 с титром 0,001700 г/см3 равна:
-: 2,574;
-: 3,084;
-: 2,820;
-: 6,230.
I: {{39}}; II-8; k=B;
S: Индикатор, при определении бромидов методом Фаянса:
-: дифениламин;
-: флуоресцеин;
-: ферроин;
-: метиленовый синий.
I: {{40}}; II-8; k=C;
S: Концентрации (моль/дм3) ионов Аg+, при которых начинается осаждение АgС1 и Аg2СгO4 , если титруют 0,1 М раствор NaС1 и 0,01 М К2СгO4 раствором АgNO3 , 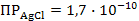 ,
, 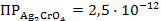 :
:
-: 10–10; 10–11;
-: 10–9; 3 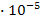 ;
;
-: 10–9; 9 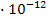 ;
;
-: 10–9; 3 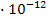
I: {{41}}; II-9; k=A;
S:рН при определении хлоридов и бромидов методомроданидометрии:
-: >>7;
-: 7;
-: < 7;
-: 1–13.
I: {{42}}; II-9; k=A;
S: Факторы, влияющие на величину скачка кривой титрования в методах осаждения:
-: полнота осаждения и рН раствора;
-: исходные концентрации растворов и ПР осадка;
-: скорость осаждения и рН титруемого раствора;
-: ПР осадка и полнота осаждения.
I: {{43}}; II-9; k=B;
S: Стандартное вещество для установления титра раствора NН4SСN:
-: Аg2СгO4;
-: АgС1;
-: АgNO3;
-: NaCl.
I: {{44}}; II-9; k=B;
S: Заряд частиц АgI при прямом титровании раствора нитрата серебра раствором КI изменяется:
-: с положительного на отрицательный;
-: с отрицательного на положительный;
-: частицы электронейтральны;
-: заряд частиц не изменяется.
I: {{45}}; II-9; k=C;
S: Масса (г) хлорид-ионов втитруемом растворе, если на титрование раствора NН4С1 затрачивается 30 см3 раствора АgNO3 с титром по хлору 0,003512 г/см3 равна:
-: 0,2108;
-: 0,0527;
-: 0,1054;
-: 0,0304.
I: {{46}}; II-10; k=A;
S: Масса (г) КС1 в 500 см3 раствора, если на титрование 25 см3 раствора КС1 расходуется 34 см3 0,0150 М раствора АgNОз равна:
-: 3,72;
-: 5,32;
-: 4,54;
-: 0,76.
I: {{47}}; II-10; k=A;
S: Навеска (г) галита, содержащего 40 % NaCl, которая необходима для приготовления 1 дм3 0,1 М раствора:
-: 14,61;
-: 15,02;
-: 13,95;
-: 10,40.
I: {{48}}; II-10; k=B;
S: Титрант и рН раствора при определении хлоридов методом Мора:
-: АgN03, рН=7;
-: NaC1, рН < 7;
-: NaCl, рН >>7;
-: АgNO3, рН > 7.
I: {{49}}; II-10; k=B;
S: Ионы, определяемые методом Мора:
-: С1–, Вг –;
-: Аg+ , С1–, Вг –, SСN–;
-: Аg+, С1–, Вг –;
-: Аg+, SCN–.
I: {{50}}; II-10; k=C;
S: Адсорбционный индикатор в методах осадительного титрования:
-: крахмал;
-: ферроин;
-: флуоресцеин;
-: хромат калия.
I: {{51}}; II-11; k=A;
S: Титрант при определении хлоридов методом Мора:
-: NaC1;
-: Нg2(NО3)2;
-: NH4SСN;
-: АgNO3.
I: {{52}}; II-11; k=A;
S: Последовательность осаждения ионов, если на раствор, содержащий 1 моль/дм3 Ва2+ –ионов и 0,01 моль/дм3 Са2+–ионов, действуют раствором оксалата аммония.
ПР(СаС2O4) = 2,3 • 10–9, ПР(ВаС2O4) = 1,1 • 10–7:
-: Ва2+, Са2+;
-: Са2+, Ва2+;
-: одновременно;
-: Са2+ с примесью Ва2+.
I: {{53}}; II-11; k=B;
S: Титр (г/см3) по хлору 0,1121 н раствора АgNO3:
-: 0,007952;
-: 0,001987;
-: 0,003975;
-: 0,002036.
I: {{54}}; II-11; k=B;
S: рС1, при титровании 0,1 М раствора NaС1 раствором АgNO3 такой же концентрации, если раствор оттитрован на 95 %:
-: 5,2;
-: 2,6;
-: 1,3;
-: 1,8.
I: {{55}}; II-11; k=C;
S: Индикатор, при меркурометрическом определении хлоридов:
-: дифениламин;
-: дифенилкарбазон;
-: эриохромовый черный Т;
-: фенолфталеин.
I: {{56}}; II-12; k=A;
S: Титр (г/см3) 0,1121 н раствора АgNОз равен:
-: 0,013279;
-: 0,019057;
-: 0,040280;
-: 0,065880.
I: {{57}}; II-12; k=A;
S: рАg, если 0,1 М раствор NaС1 оттитрован 0,1 М раствором АgNОз на 95 %:
-: 3,6;
-: 4,3;
-: 7,7;
-: 5,8.
I: {{58}}; II-12; k=B;
S: Ученый, предложивший использовать хромат калия в качестве индикатора при аргентометрическом определении хлоридов ###
+: Карл Мор;
I: {{59}}; II-12; k= B;
S: Индикаторы, в методах осадительного титрования:
-: эозин, хромат калия;
-: крахмал, метиловый красный;
-: ферроин, мурексид;
-: эриохромовый черный Т, мурексид.
I: {{60}}; II-12; k= C;
S: Заряд частиц АgС1 при титровании раствора нитрата серебра раствором хлорида натрия изменяется с:
-: с отрицательного на положительный;
-: с отрицательного на нейтральный;
-: с положительного на отрицательный;
-: с положительного на нейтральный.
I: {{61}}; II-13; k=A;
S: Действие индикатора в методе Фольгарда:
-: образование окрашенного соединения;
-: изменение концентрации индикатора;
-: диссоциация индикатора;
-: образование окрашенного комплекса.
I: {{62}}; II-13; k=A;
S: Максимальная масса навески (мг) хлорида натрия для установления титра 0,1 М раствора АgNОз при титровании из бюретки вместимостью 25 см3:
-: 137,0;
-: 146,3;
-: 68,5;
-: 34,3.
I: {{63}}; II-13; k= B;
S: Среда, для роданидометрического определения хлоридов и бромидов:
-: сильнокислая или сильнощелочная;
-: кислая;
-: слабощелочная или нейтральная;
-: сильнощелочная или нейтральная.
I: {{64}}; II-13; k= B;
S: Титрант и рН раствора при определении хлоридов методом Мора:
-: NH4SCN, рН<7;
-: АgNO3, рН=7;
-: NаС1, рН=7
-: NH4SCN, рН > 7.
I: {{65}}; II-13; k=C;
S: Ионы, определяемые методом Фольгарда:
-: Аg+, С1–, Вr –, Fе3+, MnO4
-: SСN–, С1–, Вr –, I–, Аg+;
-: С2O42–, С1–, Вr, Аg+;
-: С1–, Вr –-, I–, МnO4–.
I: {{66}}; II-14; k=A;
S: Максимальная масса навески (мг) хлорида натрия для установления титра 0,1 М раствора АgNO3 при титровании из бюретки вместимостью 5 см3 равна:
-: 29,2;
-: 14,5;
-: 43,5;
-: 28,2.
I: {{67}}; II-14; k=A;
S: Параметр, определяющий величину скачка на кривой титрования в методах осаждения:
-: ПРосадка и рН раствора;
-: К ионизации индикатора и рН раствора;
-: Кионизации индикатора и ПРосадка;
-: ПРосадка и исходные концентрации растворов.
I: {{68}}; II-14; k= B;
S: Стандартное вещество для определения титра раствора АgNO3:
-: NaCl;
-: К2Сг2O7;
-: NH4SСN;
-: К2СгO4.
I: {{69}}; II-14; k= B;
S: Изменение интенсивности окраски адсорбционного индикатора при уменьшении рН:
-: ослабление;
-: возрастание;
-: возрастание, затем ослабление;
-: изменение рН не влияет на окраску индикатора.
I: {{70}}; II-14; k=C;
S: Параметр, обусловливающий применение индикатора К2СгO4 при титровании хлоридов раствором АgNO3:
-: различие в константах ионизации АgС1 и Аg2СгO4;
-: различие в величинах ПР(АgС1)и ПР(Аg2СгO4);
-: изменение концентрации ионов водорода в растворе;
-: собственная окраска индикатора.
I: {{71}}; II-15; k=A;
S: Масса (мг) роданида калия в растворе, если на титрование раствора КSСN расходуется 26,05 см3 0,1015 н раствора АgNO3:
-: 513,0;
-: 256,5;
-: 265,5;
-: 384,0.
I: {{72}}; II-15; k=A;
S: Стандартное вещество для установления титра раствора NН4SСN:
-: Nа2С2O4;
-: АgNO3;
-: АgС1;
-: КС1.
I: {{73}}; II-15; k= B;
S: Требования к осадкам в методах осадительного титрования:
-: интенсивная окраска, большое значение ПР;
-: быстрое выпадение, отсутствие соосаждения;
-: малое значение ПР, быстрое выпадение осадка;
-: интенсивная окраска, отсутствие соосаждения.
I: {{74}}; II-15; k= B;
S: Адсорбционный индикатор:
-: эозин;
-: эриоглауцин;
-: крахмал;
-: ферроин.
I: {{75}}; II-15; k=C;
S: Условия необходимые для определения роданидов методом Фольгарда:
-: отсутствие окислителей, рН=7;
-: присутствие окислителей, рН < 7;
-: отсутствие солей ртути, присутствие окислителей;
-: присутствие окислителей, рН > 7.
I: {{76}}; II-16; k=A;
S: Вещество, на титрование которого расходуется больший объем раствора АgNO3 при условии, что титры и объемы растворов КС1 и NaCl одинаковы:
-: хлорида калия;
-: хлорида натрия;
-: различия незначительны;
-: объемы титранта одинаковы.
I: {{77}}; II-16; k=A;
S: Стандартное вещество в методе Мора:
-: NaCl;
-: АgС1;
-: ВаС12;
-: FеС13;
I: {{78}}; II-16; k= B;
S: Условия, необходимые для определения роданидов методом Фольгарда:
-: присутствие окислителей и сильнокислая среда;
-: отсутствие окислителей и солей ртути;
-: присутствие солей ртути и нейтральная среда;
-: присутствие окислителей и сильнощелочная среда.
I: {{79}}; II-16; k= B;
S: Факторы, влияющие на величину скачка кривой осадительного титрования:
-: ПРосадка и рН растворов;
-: концентрации растворов и Кионизации индикатора;
-: концентрации растворов и ПРосадка;
-: концентрации и рН растворов.
I: {{80}}; II-16; k=C;
S: Явление, наблюдаемое в растворе с увеличением рН при титровании с адсорбционными индикаторами:
-: интенсивность окраски возрастает;
-: интенсивность окраски уменьшается;
-: индикатор разрушается;
-: изменений не происходит.
I: {{81}}; II-17; k=A;
S: Содержание Cl– – ионов (мг/дм3), если на титрование 100 см3 воды израсходовано
22,0 см3 раствора АgNO3 с титром поС1– равным0,0012 г/ см3:
-: 264;
-: 300;
-: 110;
-: 290.
I: {{82}}; II-17; k=A;
S: Факторы, от которых зависит величина скачка на кривой осадительного титрования:
-: полнота осаждения и ПРосадка;
-: концентрации растворов и ПРосадка;
-: интервал перехода индикатора и ПРосадка;
-: скорость осаждения и рН растворов.
I: {{83}}; II-17; k= B;
S: Адсорбционный индикатор:
-: флуоресцеин;
-: мурексид;
-: дифениламин;
-: крахмал.
I: {{84}}; II-17; k= B;
S: Фамилия основателя метода равного помутнения ###:
+: Гей Люcсак
I: {{85}}; II-17; k=C;
S: Установите соотношения между электролитом и формулой определения его растворимости:
L1: BaSO4;
L2: HgJ2;
L3: Ca3(PO4)2;
L4: Ag2CrO4;
R1: 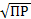 ;
;
R2: 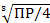 ;
;
R3: 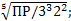
R4: 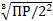 .
.
I: {{86}}; II-18; k=A;
S: Стандартное вещество в методе Фольгарда:
-: K2CrO4;
-: NaCl;
-: AgNO3;
-: Hg(NO3)2;
I: {{87}}; II-18; k=A;
S: Вещество, которое осаждается первым при титровании бромидов и иодидов раствором АgNОз; ПРAgBr = 5 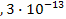 ; ПРAgJ =
; ПРAgJ = 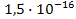 :
:
-: бромид серебра;
-: иодид серебра;
-: иодид серебра и частично хлорид серебра;
-: соли осаждаются одновременно.
I: {{88}}; II-18; k= B;
S: Требования, предъявляемые к осадкам в методах осадительного титрования:
-: наличие окраски, большое значение ПР;
-: малое значение ПР, быстрое выпадение осадка;
-: быстрое выпадение осадка, отсутствие окраски осадка;
-: большое значение ПР, быстрое выпадение осадка.
I: {{89}}; II-18; k= B;
S: Стандартное вещество для установления титра раствора Нg(NОз)2:
-: К2СrO4
-: NaС1;
-: К2Сг2O7;
-: АgNОз.
I: {{90}}; II-18; k=C;
S: Индикатор для определения хлоридов меркуриметрическим методом осаждения:
-: дифениламин;
-: дифенилкарбазон;
-: эозин;
-: муреусид.
I: {{91}}; II-19; k=A;
S: Масса (г) хлорида аммония в растворе на титрование которого расходуется 25 см3 0,05 М раствора АgNОз равен:
-: 0,134;
-: 0,099;
-: 0,067;
-: 0,033.
I: {{92}}; II-19; k=A;
S: Условия применения метода Фольгарда:
-: отсутствие окислителей и рН (1–13);
-: отсутствие собственной окраски раствораи пептизирующих веществ, кислая среда;
-: нейтральная среда и собственная окраска раствора;
-: нейтральная среда, отсутствие окислителей и присутствие пептизирующих веществ.
I: {{93}}; II-19; k= B;
S: Стандартное вещество для определения титра NН4SСN:
-: NaNОз;
-: АgС1;
-: AgNОз
-: КС1.
I: {{94}}; II-19; k= B;
S: Механизм действия индикатора метода Мора:
-: образование окрашенного комплекса;
-: диссоциация индикатора;
-: образование окрашенного осадка;
-: таутомерный переход.
I: {{95}}; II-19; k=C;
S: Индикатор, применяемый при определении бромидов роданометрическим методом:
-: Fе(SCN)з;
-: К2СrO4;
-: С6Н5–NН–С6Н5;
-: FeNH4(SO4)2.
I: {{96}}; II-20; k=A;
S: Навеска (г) карналлита, содержащего 40 % (мас.) хлорид-ионов, необходимая для определения ионов С1– (титрант – 0,1 М раствор АgNO3, объем титранта 25 см3) равна:
-: 0,34;
-: 0,35;
-: 0,11;
-: 0,22.
I: {{97}}; II-20; k=A;
S: Заряд частиц АgС1 при титровании хлоридов раствором нитрата серебра изменяется:
-: с электронейтрального на положительный;
-: с электронейтрального на отрицательный;
-: с отрицательного на положительный;
-: с положительного на отрицательный.
I: {{98}}; II-20; k=A;
S: Фактор, позволяющий использовать К2СrO4 в качестве индикатора при титровании хлоридов раствором АgNOз:
-: изменение редокс-потенциала титруемого раствора;
-: изменение концентрации ионов водорода в растворе;
-: различие в величинах ПР(AgСl) и ПР(Аg2СгO4);
-: образование неокрашенного осадка.
I: {{99}}; II-20; k=A;
S: Индикатор и титрант меркурометрического определения хлоридов:
-: Fе(SСN)3 и Нg2(NO3)2;
-: Нg2(NO3)2 и Fе(SСN)3;
-: К2СгO4 и Нg2(NO3)2;
-: Нg2(NO3)2 и К2СгO4.
I: {{100}}; II-20; k=A;
S: Адсорбционный индикатор:
-: флуоресцеин;
-: мурексид;
-: роданид железа (III);
-: хромат калия.
I: {{101}}; II-21; k=A;
S: рС1раствора при титровании 0,1 н раствора NaС1 0,1 н раствором АgNOз, когда добавлено 90 % титранта равен:
-: 3,0;
-: 1,2;
-: 2,28;
-: 1,50.
I: {{102}}; II-21; k=A;
S: Стандартное вещество в методе роданидометрии:
-: NaNO3;
-: КС1;
-: АgNO3;
-: К2СгO4.
I: {{103}}; II-21; k=A;
S: Индикаторы в методах осадительного титрования:
-: мурексид и железоаммонийные квасцы;
-: хромат калия и железоаммонийные квасцы;
-: хром темно-синий и ферроин;
-: крахмал и хромат калия.
I: {{104}}; II-21; k=A;
S: Ионы, определяемые методом Фольгарда:
-: С2O42–, С1–, Аg+;
-: SCN–, С1–, Вr –, I –, Аg+;
-: С2O42–, С1–, Вr –, I – ;
-: SCN–, С1–, Вr –, Аg+.
I: {{105}}; II-21; k=A;
S: Значение [H+] при определении хлоридов и бромидов методом роданидометрии:
-: >> 10–7;
-: 10–7;
-: < 10–7;
-: 10–1 – 10–13.
I: {{106}}; II-22; k=A;
S: Содержание (моль) бромид-ионов в титруемом растворе, на титрование которого расходуется 24 см3 раствора АgNO3 с титром по брому 0,002518 г/см3:
-: 7 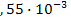 ;
;
-: 7 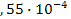 ;
;
-: 3 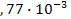 ;
;
-: 3 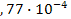 .
.
I: {{107}}; II-22; k=A;
S: Ионы, определяемые методом Мора:
-: С1–, Вr –, I–;
-: Аg+, SСN –;
-: Аg+, Сl –, Вr –;
-: Аg+, I–, Вr –.
I: {{108}}; II-22; k=A;
S: Индикатор, применяемый при меркурометрическом определении хлоридов:
-: дифенилкарбазон;
-: хромат калия;
-: дифениламин;
-: мурексид.
I: {{109}}; II-22; k=A;
S: Титрант и индикатор метода Мора:
-: АgNOз и К2СгO4;
-: К2СrO4 и АgNOз;
-: АgNО3, и NH4SCN;
-: NH4SCN и АgNO3
I: {{110}}; II-22; k=A;
S: Установить соответствие между методом определения хлоридов и применяемым индикатором
L1: метод Фаянса;
L2: метод Мора;
L3: метод Фольгарда;
L4: меркуриметрия;
L5: меркурометрия.
R1: флуоресцеин;
R2: K2CrO4;
R3: NH4Fe(SO4)2;
R4: дифенилкарбазон;
R5: Fe(SCN)3.
I: {{111}}; II-23; k=A;
S: Масса (г) хлорид-ионов в растворе, на титрование которого затрачивается 16 см3 раствора АgNО3 с титром по Cl– равным 0,001837 г/см3, равна:
-: 0,0324;
-: 0,0147;
-: 0,0588;
-: 0,0294.
I: {{112}}; II-23; k=A;
S: Индикатор, применяемый для аргентометрического определения иодидов:
-: железоаммонийные квасцы;
-: эозин;
-: хромат калия;
-: мурексид.
I: {{113}}; II-23; k=B;
S: Среда, необходимая для определения хлоридов и бромидов методом роданидометрии:
-: любая;
-: кислая;
-: щелочная;
-: нейтральная.
I: {{114}}; II-23; k=B;
S: Титр (г/см3) по NаС1 0,0560 М раствора АgNOз:
-: 0,003276;
-: 0,004028;
-: 0,006553;
-: 0,003042.
I: {{115}}; II-23; k=C;
S: Индикатор и титрант метода Фольгарда:
-: FеNН4(SO4)2 и NН4SСN;
-: Fе(SСN)3 и NaC1;
-: NaС1 и Fе(SСN)3;
-: NН4SСN и FеNН4(SO4)2.
I: {{116}}; II-24; k=A;
S: рС1 в точке эквивалентности при титровании 0,1 М раствора NаС1 0,1 М раствором АgNOз такой же концентрации равен:
-: 1,00;
-: 4,88;
-: 5,25;
-: 2,56.
I: {{117}}; II-24; k=A;
S: Значение pH при определении хлоридов и бромидов методом роданидометрии:
-: рН=7;
-: рН >> 7;
-: рН < 7;
-: рН (1–13).
I: {{118}}; II-24; k=B;
S: Значение рН и титрант метода Мора:
-: рН > 7; NaC1;
-: рН = 7; NН4SСN;
+: рН = 7; АgNO3;
-: рН < 7; NaNO3.
I: {{119}}; II-24; k=B;
S: Изменение заряда частиц Аg+ при титровании раствора нитрата серебра раствором иодида:
-: с положительного на электронейтральный;
-: с положительного на отрицательный;
-: с отрицательного на электронейтральный;
-: заряд частиц не изменяется.
I: {{120}}; II-24; k=C;
S: Индикатор, применяемый при меркурометрическом определении хлоридов:
-: крахмал;
-: железоаммонийные квасцы;
-: роданид железа (III);
-: мурексид.
I: {{121}}; II-25; k=A;
S: Осадительный индикатор, при определении галогенид-ионов методом Мора:
-: K2Cr2O7;
-: K2CrO4;
-: KSCN;
-: FeNH4(SO4)2.
I: {{122}}; II-25; k=A;
S: Галогенид серебра, который осаждается первым, если к раствору, содержащему равные количества хлоридов и иодидов, добавляют раствор АgNОз; ПР(АgСl)=1 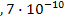 ПР(AgI) = 8
ПР(AgI) = 8 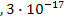 :
:
-: хлорид серебра;
-: хлорид серебра и иодид серебра одновременно;
-: иодид серебра;
-: хлорид серебра и частично иодид серебра.
I: {{123}; II-25; k=B;
S: Титрант и индикатор при определении серебра в сплавах:
-: KSСN и NH4Fe(SO4)2;
-: АgNОз и K2CrO4;
-: NH4Cl и KSСN;
-: KSСN и АgNОз.
I: {{124}}; II-25; k=B;
S: Значение pCl при титровании 0,1 н раствора NaCl раствором AgNO3такой же концентрации, если добавлено 50% титранта:
-: 1,00;
-: 1,48;
-: 2,00;
-: 3,00.
I: {{125}}; II-25; k=C;
S: Сопоставление растворимости (Р) соединений исходя из значений их ПР:
ПР(CaCO3) = 4,8 ∙ 10–9; ПР(CaSO4) = 9,0 ∙ 10–6:
-: одинаковая;
-: CaSO4 > CaCO3;
-: CaSO4 < CaCO3;
-: CaCO3 = CaSO4.
I: {{126}}; II-26; k=A;
S: Растворимость AgBr при осаждении AgBr в избытке AgNO3:
-: увеличивается;
-: уменьшается;
-: не изменяется;
-: уменьшается pH.
I: {{127}}; II-26; k=A;
S: ПР 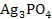 , если его растворимость составляет 4,68 ● 10–6 моль/дм3 равен:
, если его растворимость составляет 4,68 ● 10–6 моль/дм3 равен:
-: 2,5 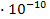 ;
;
-: 1 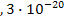 ;
;
-: 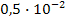 ;
;
-: 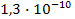 .
.
I: {{128}}; II-26; k=B;
S: Заряд частиц АgС1 при титровании раствора нитрата серебра раствором хлорида натрия изменяется:
-: с отрицательного на положительный;
-: с положительного на отрицательный;
-: частицы АgС1 электронейтральны;
-: заряд частиц не изменяется
I: {{129}}; II-26; k=B;
S: Значение pCl при титровании 0,1н раствора NaCl раствором AgNO3такой же концентрации, если добавлено 90 % титранта:
-: 2,00;
-: 2,50;
-: 2,28;
-: 3,00.
I: {{130}}; II-26; k=C;
S: Соотношение растворимостей (Р) соединений исходя из значений их ПР:
ПРAgCl =1 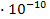 ; ПРAgJ =
; ПРAgJ = 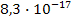 :
:
-: одинаковое;
-: AgCl > AgJ;
-: AgJ > AgCl;
-: AgJ = AgCl.
I: {{131}}; II-27; k=A;
S: При осаждении AgCl в избытке NaCl растворимость AgCl:
-: не изменяется;
-: уменьшается;
-: увеличивается;
-: увеличивается pH.
I: {{132}}; II-27; k=A;
S: рАg если, раствор NaС1 с концентрацией 0,1 М оттитрован на 95 % 0,1 М раствором АgNОз; ПР(АgС1)= 10–10 равен:
-: 3,6;
-: 4,3;
-: 7,7;
-: 5,8.
I: {{133}}; II-27; k=B;
S: рН при определении хлоридов методом Мора:
-: рН .> 7;
-: рН < 7;
-: рН = 7;
-: рН (2–6).
I: {{134}}; II-27; k=B;
S: Значение pCl при титровании 0,1 н раствора NaCl 0,1н раствором AgNO3, если добавлено 99 % титранта, равно:
-: 3,10;
-: 3,30;
-: 2,90;
-: 2,15.
I: {{135}}; II-27; k=C;
S: Оцените растворимость (Р) соединений исходя из значений ПР: ПРBaSO4 = 1,8 ● 10–10; ПРCaSO4 = 9,1 ●10–6:
-: одинаковая;
-: Р CaSO4 > Р BaSO4;
-: Р CaSO4 < Р BaSO4;
-: Р BaSO4 не изменяется.
I: {{136}}; II-28; k=A;
S: Соотношение скачков титрования растворов NaCl (I) и NaI (II) стандартным раствором AgNO3:
-: не изменяется;
-: I < II;
-: I > II;
-: зависит от pK.
I: {{137}}; II-28; k=A;
S: Стандартное вещество для установления титра раствора NН4SСN:
-: Nа2С2O4;
-: АgNO3;
-: АgС1;
-: КС1.
I: {{138}}; II-28; k=B;
S: Требования к осадкам в методах осадительного титрования:
-: интенсивная окраска, большое значение ПР;
-: быстрое выпадение, отсутствие соосаждения;
-: малое значение ПР, быстрое выпадение осадка;
-: интенсивная окраска, отсутствие соосаждения.
I: {{139}}; II-28; k=B;
S: Значение pCl при титровании 0,1н раствора NaCl 0,1н раствором AgNO3, если добавлено 100 % титранта, равно:
-: 4,55;
-: 4,76;
-: 4,88;
-: 5,00.
I: {{140}}; II-28; k=C;
S: Оцените растворимость соединений (Р) исходя из значений ПР:
ПР(Mg(OH)2) = 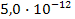 ; ПР(PbI2) =
; ПР(PbI2) = 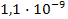 :
:
-: одинаковая;
-: Mg(OH)2 > PbI2;
-: Mg(OH)2 < PbI2;
-: PbI2 не изменяется.
I: {{141}}; II-29; k=A;
S: Растворимость осадка при осаждении BaSO4 в избытке BaCl2:
-: не изменяется;
-: увеличивается;
-: уменьшается;
-: зависит от pH.
I: {{142}}; II-29; k=A;
S: Изменение заряда частиц АgС1 при титровании хлоридов раствором нитрата серебра:
-: с электронейтрального на положительный;
-: с электронейтрального на отрицательный;
-: с отрицательного на положительный;
-: с положительного на отрицательный.
I: {{143}}; II-29; k=B;
S: Фактор, обусловливающий применение К2СrO4 в качестве индикатора при титровании хлоридов раствором АgNOз
-: изменение редокс-потенциала титруемого раствора;
-: изменение концентрации ионов водорода в растворе;
-: различие в величинах ПР(AgСl) и ПР(Аg2СгO4);
-: образование неокрашенного осадка.
I: {{144}}; II-29; k=B;
S: Значение pCl при титровании 0,1 н раствора NaС1 раствором AgNO3 такой же концентрации, если добавлено 101 % титранта, равен:
-: 6,10;
-: 6,00;
-: 7,00;
-: 6,46.
I: {{145}}; II-29; k=C;
S: Формула для расчета [Cl–] при титровании NaС1 по методу Мора после точки эквивалентности:
-: [Cl–] = 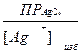 ;
;
-: [Cl–] = 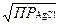 ;
;
-: [Cl–] = 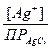 ;
;
-: [Cl–] = 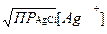 .
.
I: {{146}}; II-30; k=A;
S: Величина ПР характерна для соединения:
-: NaCl;
-: Na2SO4;
-: Ca3(PO4)2;
-: Ca(NO3)2.
I: {{147}}; II-30; k=A;
S: Стандартное вещество в методе роданидометрии:
-: NaNO3;
-: КС1;
-: АgNO3;
-: К2СгO4.
I: {{148}}; II-30; k=B;
S: Индикаторы, применяемые в методах осадительного титрования:
-: мурексид и железоаммонийные квасцы;
-: железоаммонийные квасцы и лакмус;
-: эозин и флуоресцеин;
-: крахмал и хромат калия.
I: {{149}}; II-30; k=B;
S: Значение pCl при титровании 100 см3 0,01 н раствора NaCl 0,1 н раствором AgNO3 когда добавлено 60% титранта, равно:
-: 2,10;
-: 2,42;
-: 2,80;
-: 3,00.
I: {{150}}; II-30; k=C;
S: Растворимость осадка при осаждении AgI в избытке KI:
-: не изменяется;
-: уменьшается;
-: увеличивается;
-: зависит от pH.
