Основные формулы, используемые в аналитической химии и примеры решения задач
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПЕРМСКИЙ ИНСТИТУТ (ФИЛИАЛ)
Федерального государственного бюджетного образовательного учреждения
Высшего профессионального образования
«Российский экономический университет им. Г.В. Плеханова»
Кафедра Технологии и организации питания и услуг
Одобрено кафедрой:
Протокол №
«» 20__г.
Зав. кафедрой
АНАЛИТИЧЕСКАЯ ХИМИЯ И ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Методические указания по выполнению контрольных работ для студентов заочной формы обучения
(Приложение к рабочей программе дисциплины)
Для направления:19.03.04 Технология продукции и организация общественного питания
Пермь 2015
Методические указания по выполнению контрольных работ составлены в соответствии с федеральными государственными образовательными стандартами третьего поколения.
Автор – составитель:
Шестакова Г.Е., к.х.н., доцент кафедры Технологии и организации питания и услуг
Цель выполнения контрольной работы –закрепление теоретических знаний и умение их применять при решении практических заданий.
1.1. Требования к содержанию контрольной работы:
· самостоятельный подход к изложению материала;
· систематизация теоретического материала с использованием различных литературных источников, включая дополнительную литературу по профилю специальности;
· наличие ссылок на номер первоисточника, указанного в списке рекомендуемой литературы;
· наличие рисунков, иллюстрирующих структурную организацию макромолекул; графических зависимостей и схем обмена веществ;
· практические задания должны быть аргументированы краткими теоретическими положениями.
Требования к оформлению контрольной работы:
· объем работы не должен превышать 20 – 24 страницы рукописного текста (ученическая тетрадь) или 10 – 15 страниц компьютерного текста (формат А4, кегль 14); после ответов по каждому заданию необходимо оставлять место для аргументации балловой оценки со стороны преподавателя-рецензента;
· страницы работы нумеруются, титульный лист является первой страницей (не нумеруется);
· на 2-ой странице дается содержание работы (номер раздела и его название, номера заданий по разделам и их формулировка);
· в конце контрольной работы приводится список использованной литературы (основной и дополнительной) и иных источников информации;
· рукописный текст должен быть написан разборчивым почерком, без помарок; небрежность в изложении и оформлении не допускается.
Контрольная работа должна быть представлена в деканат факультета не позднее, чем за 20 дней до начала экзаменационной сессии.
Контрольная работа является одним из условий допуска студента к экзамену. Работа оценивается в баллах – максимум 25 баллов, если студент набрал 10 и меньшее количество баллов, то работа считается незачтенной и отправляется на доработку в соответствии с замечаниями рецензента. На повторное рецензирование работа отправляется вместе с первоначальным оригиналом.
Контрольную работу целесообразно выполнять после отработки лабораторного практикума, который также оценивается в баллах.
При отсутствии студента на установочной сессии по каким-либо причинам, ему необходимо пройти тестирование (входной контроль остаточных знаний) – максимум 20 баллов.
Варианты контрольных работ
Контрольные работы призваны закрепить усвоение теоретической части каждого раздела программы.
Контрольная работа посвящена качественному и количественному анализу, задачей которых является обнаружение катионов и анионов анализируемого образца и количественному анализу этого объекта с использованием гравиметрических и титриметрических и физико-химических методов анализа.
В контрольную работу включено 5 вопросов, которые содержат теоретический материал по качественному, количественному, инструментальному методам анализа, решение расчетных задач. Выбор варианта контрольной работы осуществляется по специальной таблице по первой букве фамилии студента.
| Первая буква фамилии | Вариант контрольной работы | Первая буква фамилии | Вариант контрольной работы |
| А | П | ||
| Б | Р | ||
| В | С | ||
| Г | Т | ||
| Д | У | ||
| Е | Ф | ||
| Ж | Х | ||
| З | Ц | ||
| И | Ч | ||
| К | Ш | ||
| Л | Щ | ||
| М | Э | ||
| Н | Ю | ||
| О | Я |
При выполнении контрольных работ необходимо выполнять следующие правила:
1. На титульном листе указывать номер контрольной работы, наименование дисциплины, фамилию и инициалы студента и шифр.
2. Контрольную работу следует выполнять аккуратно, оставляя поля для замечаний рецензента.
3. Задачи своего варианта переписывать полностью и делать краткую запись условий задачи. Числовые значения всех физических величин, взятых из условия задачи или из таблиц, представлять в системе “СИ”.
4. Для пояснения решения задачи, если это возможно, написать уравнение реакции.
5. Решения должны сопровождаться пояснениями, в них необходимо указывать основные законы и формулы, на которых основывается решение.
6. При указании расчетной формулы приводить ее вывод.
7. Решение задач рекомендуется делать в общем виде, т.е. в буквенных обозначениях, поясняя их значение.
8. Проверить размерность полученной формулы.
9. Вычисления следует производить, подставляя заданные числовые значения физических величин только в расчетную формулу.
10. Значения физических констант и другие справочные данные берутся из таблиц. Расчеты производятся с учетом правил приближенных вычислений, которые приводятся в данном пособии.
11. В конце контрольной работы указать использованную литературу.
12. Контрольные работы, выполненные без указанных правил не засчитываются и возвращаются студенту на переработку.
Вариант № 1
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: аналитическая реакция, аналитический сигнал. Перечислите требования, предъявляемые к аналитическим реакциям. Ответ подтвердите уравнениями реакций.
2. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения 1 группы катионов.
3. Закончите и уравняйте ионно–электронным методом или методом электронного баланса уравнения окислительно-восстановительных реакций:
KJ + KMnO4 + H2SO4 =
KCrO4 + H2O2 + KOH =
Na2S2O3 + J2 =
4. Дайте обоснование титриметрического метода анализа. Покажите преимущества и недостатки данного метода.
5. Сколько мл надо взять 15М FeCl3 и 5М FeCl3, чтобы получить 1 л 10 М FeCl3.
Вариант № 2
1. Назовите принципы, положенные в основу классификации катионов и анионов на группы. Укажите общие аналитические признаки групп и действие группового реагента для 1 группы анионов.
2. Объясните и напишите уравнения химических реакций. Для каких целей в хода анализа катионов 3 аналитической группы используется реакция взаимодействия Sr2+и Са2+ ионов с насыщенным раствором сульфата аммония?
3. Закончите и уравняйте методом электронного баланса или методом полуреакций уравнения окислительно-восстановительных реакций:
KJ + KBrO3 + HCl = ; Na2S + KMnO4 + H2O = ;
H2C2O4 + KMnO4 + H2SO4 = ;
4. Покажите роль осадителя в гравиметрическом анализе. Примеры расчета осадителя в реакции.
5. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, является ли эквивалент веществ постоянной величиной, от чего он зависит?
CuSO4 + Na2H2Y = Na2CuY + H2SO4
2CuSO + 4KJ = 2CuJ + J2 + 2K2SO4
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
2Cu(OH)2 + H2SO4 = 2H2O + (CuОН)2SO4
Вариант № 3
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: реагент, групповой реагент. Перечислите требования, предъявляемые к нему. Ответ подтвердите примерами.
2. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения 2 группы катионов.
3. Дайте формулировку основного закона титриметрического анализа, приведите его математическое выражение. Дайте определение понятий: точка эквивалентности, конечная точка титрования, покажите связь между ними.
4. Дайте определение рН-индикаторам, укажите требования к ним, их характеристики: интервал перехода окраски. Обоснуйте принцип выбора индикатора.
5. Раскройте основы метода аргентометрии (метода Фаянса): обоснование, основное уравнение, особенности приготовления рабочих растворов: установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,05 моль /л AgNO3, объемом 250 мл.
Вариант № 4
1. Назовите принципы, положенные в основу классификации катионов и анионов на группы. Укажите общие аналитические признаки группы и действие группового реагента для 2 группы катионов.
2. Объясните и напишите уравнения химических реакций. Почему при систематическом анализе катионов 1 группы необходимо удалять катион аммония? Предложите несколько способов удаления солей аммония.
3. Рассчитайте содержание цинка в растворе, если на титрование пошло 10,8 мл 0,1 н трилона Б?
4. Рассчитайте титр трилона Б, если Кп = 1,0320, концентрация 0,1 г/экв/л, молекулярная масса трилона Б равна 372,2.
5. Раскройте основы метода аргентометрии (метод Фольгарда) : обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,05 моль/л NH4SCN, объемом 1 л.
Вариант № 5
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: чувствительность аналитических реакций, способы ее выражения. Каким образом ее можно повысить?
2. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения 4 группы катионов.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно – восстановительных реакций:
H2O2 + KMnO4 + H2SO4 == KJ + FeCl3 =
Na2S2O3 + j2 + H2O =
4. Укажите основные требования к реакциям, применяемым в титриметрическом анализе. Какие дополнительные требования предъявляются к реакциям окисления – восстановления, осаждения и комплексообразования? Приведите примеры используемых реакций.
5. Рассчитайте навеску MgSO4 7H2O, необходимую для приготовления 100 мл 0,1 Н раствора.
Вариант № 6
1. Назовите принципы, положенные в основу кислотно-основной классификации катионов. Укажите общие аналитические признаки групп и действие группового реагента для 3 группы катионов.
2. Объясните и напишите уравнения химических реакций. Почему катионы II группы не следует осаждать концентрированной соляной кислотой? Укажите особенности образующихся солей?
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
KJ+NaNO2+HCl = ; CrCl3+KMnO4+H2O = ; K2C2O4+KMnO4+H2SO4 =
4. Дайте определения понятия: титрованный раствор. Типы и способы приготовления титрованных растворов. Примеры. Фиксаналы. Рассчитайте молярную концентрацию 10% раствора NaOH (р = 1,11 г/см).
5. Рассчитайте, в каком количестве воды следует растворить 58,5 г NaCl, для получения раствора 1 моль/дм3.
Вариант № 7
1. Дайте определение и раскройте сущность основных понятий качественного анализа: групповые, характерные, специфические, селективные аналитические реакции и реагенты. Ответ подтвердите примерами.
2. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения 3 группы катионов.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
NaNO2 + KMnO4 + H2SO4 = H2O2 + KMnO4 + H2SO4 =
Na2S2O3 + J2 =
4. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, является ли эквивалент веществ постоянной величиной, от чего он зависит?
3KJ + KBrO3 + 6HCl = 3JCl + KBr + 3KCl + 3H2O
2KJ + H2O2 + H2SO4 = J2 + K2SO4 +2H2O
2KJ + Hg(NO3)2 = HgJ2 + 2KNO3.
5. Cколько воды потребуется прибавить к 200г 25% раствора NH3*H2O, чтобы получить 5% раствор?
Вариант № 8
1. Назовите принципы, положенные в основу классификации катионов и анионов на группы. Укажите общие аналитические признаки групп и действие группового реагента для 4 группы катионов.
2. Объясните и напишите уравнения химических реакций. Как и для чего проверяют полноту осаждения отделяемого иона? К каким ошибкам может привести а) неполнота осаждения катионов 2 группы в ходе анализа катионов 1 группы; б) неполнота осаждения Ва2+ ионов в ходе анализа катионов 3 группы?
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
KBr + KBrO3 + H2SO4 = Na2SO3 + J2 + H2O =
CrCl3 + H2O2 + KOH =
4. Раскройте основы метода йодометрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,2 моль/л J2, объемом 4 л.
5. Какие количества 80% и 10% растворов H2SO4 нужно взять, чтобы приготовить 1400 г 40% раствора.
Вариант № 9
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: способы выполнения реакций. Назовите имена ученых, предложивших тот или иной способ выполнения реакций. Ответ подтвердите примерами.
2. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения 5 группы катионов.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно – восстановительных реакций:
Na2S2O3 + KMnO4 + H2O = CrCl3 + H2O2 + NaOH =
KBr + KBrO3 + HCl =
4. Раскройте основы метода перманганатометрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,1 моль/л KMnO4, объемом 500 мл.
5. Какова молярная и нормальная концентрация раствора CuSO4, содержащего в 1л раствора 160г вещества.
Вариант № 10
1. Назовите принципы, положенные в основу кислотно-основной классификации катионов на группы. Укажите общие аналитические признаки групп и действие группового реагента для 5 группы катионов.
2. Объясните и напишите уравнения химических реакций. Какие равновесные системы существуют в водном растворе карбоната аммония? Почему осаждение катионов 3 аналитической группы этим реагентом ведут при нагревании с добавлением растворов аммиака и хлорида аммония?
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно – восстановительных реакций:
KBr + KMnO4 + H2SO4 = Na2S2O3 +J2 =
H2O2+ KJ + H2SO4 =
4. Раскройте основы метода алкалиметрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,5 моль/л КОН V=250 мл.
5. В каком количестве воды следует растворить 50,0г CuSO4 для получения раствора, содержащего 3% CuSO4.
Вариант № 11
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: дробный анализ. Напишите реакции дробного обнаружения Mg2+, Fe2+, Fe3+, NO2-, J-. Способы устранения влияния мешающих компонентов.
2. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения 6 группы катионов.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
KJ + CuSO4 =
FeSO4 + KMnO4 + H2SO4 =
Bi(NO3)3 + Na2SnO2 + NaOH =
4. Раскройте основы метода титриметрического анализа: обоснование, основное уравнение, особенности приготовления рабочих растворов, установочные вещеcтва, индикация, способы титрирования, возможности метода ацидиметрии. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 1 моль/л H2SO4, V=2 л.
5. Рассчитайте навеску FeSO4 для приготовления 1л раствора, содержащего 3% FeSО4.
Вариант № 12
1. Назовите принципы, положенные в основу кислотно-основной классификации катионов на группы. Укажите общие аналитические признаки групп и действие группового реагента для 6 группы катионов.
2. Объясните и напишите уравнения химических реакций. Почему для растворения карбонатов катионов 2 аналитической группы обычно используют хлороводородную (конц.) кислоту?
3. Закончите и уравняйте ионно–электронным методом или методом электронного баланса уравнения окислительно-восстановительных реакций:
KJ + KMnO4 + H2SO4 =
KCrO4 + H2O2 + KOH =
Na2S2O3 + J2 =
4. Раскройте основы метода трилонометрия: обоснования, основное уравнение особенности приготовления рабочих; установочные вещества индикация, способы титрования, возможности метода. Рассчитайте навеску вещества необходимую для приготовления рабочих растворов, концентрации 0,5 моль /л Na2H2Y, объемом 2,5 л.
5. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, являются ли эквивалент вещества постоянной величиной, от чего он зависит?
K2CO3 + 2HCl =2KCl + CO2 + H2O
K2CO3 + H3PO4 = KH2PO4 + KHCO3
MnSO4 + 2KOH = Mn(OH)2 + K2SO4
MnSO4 + 2Cl2 + 8KOH = K2MnO4 + 4KCl + K2SO4 + 4H2O
Вариант № 13
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: систематический анализ. Напишите уравнения реакций осаждения катионов 3 группы с групповым реагентом.
2. Составьте в молекулярном и ионном виде уравнения следующих химических реакций в водном растворе:
ZnCl2 + K4[Fe(CN)6]; ® MnCl2 + NaBiO3 + HNO3 ®
3. Закончите и уравняйте методом электронного баланса или методом полуреакций уравнения окислительно-восстановительных реакций:
KJ + KBrO3 + HCl = ; Na2S + KMnO4 + H2O = ;
H2C2O4 + KMnO4 + H2SO4 =
4. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, является ли эквивалент веществ постоянной величиной, от чего он зависит?
CuSO4 + Na2H2Y = Na2CuY + H2SO4
2CuSO + 4KJ = 2CuJ + J2 + 2K2SO4
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
2Cu(OH)2 + H2SO4 = 2H2O + (CuОН)2SO4
5. Раскройте основы метода аргентометрии (метода Фаянса): обоснование, основное уравнение, особенности приготовления рабочих растворов: установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,05 моль/л AgNO3, объемом 250 мл.
Вариант № 14
1. Назовите принципы, положенные в основу классификации анионов по Алимарину-Блоку на группы. Укажите общие аналитические признаки групп и действие группового реагента для 1 группы анионов.
2. Сформулируйте закон действующих масс, приведите его математическое выражение, укажите границы его применения. Покажите на примерах использование данного закона для управления химическими реакциями.
3. Дайте формулировку основного закона титриметрического анализа, приведите его математическое выражение. Дайте определение понятий: точка эквивалентности, конечная точка титрования, покажите связь между ними.
4. Покажите различные способы индикации в окислительно-восстановительном титровании. Приведите примеры.
5. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, является ли эквивалент веществ постоянной величиной, от чего он зависит? Приведите примеры.
Вариант № 15
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: органические реагенты. Их роль в качественном химическом анализе. Ответ подтвердите примерами реакций.
2. Сформулируйте правило произведения растворимости. Какие растворы называются ненасыщенными, насыщенными, перенасыщенными с позиции данного правила? Перечислите условия полноты выделения осадков. Приведите примеры.
3. Рассчитайте содержание цинка в растворе, если на титрование пошло 10,8 мл 0,1 н трилона Б?
4. Объясните теорию образования и необходимые условия осаждения аморфных осадков в гравиметрическом анализе. Приведите примеры.
5. Раскройте основы метода перманганатометрия: обоснование, основное уравнение; особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,02 моль/л KMnO4, объемом 200 мл.
Вариант № 16
1. Назовите принципы, положенные в основу классификации анионов по Алимарину-Блоку на группы. Укажите общие аналитические признаки групп и действие группового реагента для 2 группы анионов.
2. Составьте в молекулярном и ионном виде уравнения следующих химических реакций в водном растворе:
CuSO4 + H2S ® MgCl2 + (NH4)2HPO4 ®
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
H2O2 + KMnO4 + H2SO4 == KJ + FeCl3 =
Na2S2O3 + j2 + H2O =
4. Поясните роль исходных (стандартных, установочных) веществ в титриметрическом анализе. Укажите требования к ним. Приведите примеры таких веществ.
5. Cколько воды потребуется прибавить к 200г 25% раствора NH3×H2O, чтобы получить 5% раствор?
Вариант № 17
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: экстракционные методы разделения и обнаружения ионов (Co2+, Cr3+, CH3COO-,SCN-).
2. Дайте понятие обратимых химических реакций. Покажите роль закона действующих масс в приложении к обратимому процессу взаимодействия катионов калия с виннокаменной кислотой; значение константы равновесия для направления течения реакций.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
KJ + NaNO2 + HCl = CrCl3 + KMnO4 + H2O =
K2C2O4 + KMnO4 + H2SO4 =
4. Покажите способы выражения концентраций растворов в титриметрическом анализе: молярная концентрация, молярная концентрация эквивалента, титр, титр раствора по определяемому веществу. Что такое поправочный коэффициент? Его значение, формулы расчета.
5. Раскройте основы метода йодометрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,2 моль/л J2, объемом 4 л.
Вариант № 18
1. Назовите принципы, положенные в основу классификации анионов по Алимарину-Блоку на группы. Укажите общие аналитические признаки групп и действие группового реагента для 3 группы анионов.
2. Дайте определение окислительно-восстановительной системы и потенциалов (стандартного, реального, условного). Покажите на примерах зависимость величины окислительно-восстановительного потенциала от концентрации регентов и рН растворов.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно – восстановительных реакций:
NaNO2 + KMnO4 + H2SO4 = H2O2 + KMnO4 + H2SO4 =
Na2S2O3 + J2 =
4. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, является ли эквивалент веществ постоянной величиной, от чего он зависит?
10KJ + 2KMnO4 + 8H2SO4 = 5J2 + 2MnSO4 + 6K2SO4 + 8H2O
5KJ + 6KMnO4 + 9H2SO4 = 5KJO3 + 6MnSO4 + 3H2SO4 + 9H2O
5KJ + 2KMnO4 + 16HCl = 5JCl2 + 2MnCl2 + 7KCl + 8H2O
5. Раскройте основы метода перманганатометрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,1 моль/л KMnO4 , объемом 500 мл.
Вариант № 19
1. Дайте определение и раскройте сущность основных понятий качественного химического анализа: классификация методов качественного химического анализа по массе определяемого вещества. Укажите преимущества полумикрометода.
2. Составьте в молекулярном и ионном виде уравнения следующих химических реакций в водном растворе:
(NH4)2C2O4 + CaCl2 ®; NaOHизб. + ZnCl2 ®
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
KBr + KBrO3 + H2SO4 = Na2SO3 + J2 + H2O =
CrCl3 + H2O2 + KOH =
4. Раскройте основы метода алкалиметрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,5 моль/л КОН V=250 мл.
5. В каком количестве воды следует растворить 50,0г CuSO4 для получения раствора, содержащего 3% CuSO4.
Вариант № 20
1. Назовите принципы, положенные в основу классификации катионов и анионов на группы. Укажите общие аналитические признаки групп и действие группового реагента для 4 группы анионов (по классификации Алимарина-Блока).
2. Обоснуйте отклонение растворов сильных электролитов от закона действующих масс. Дайте формулировки понятий: ионная сила, активность, коэффициент активности.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
Na2S2O3 + KMnO4 + H2O = CrCl3 + H2O2 + NaOH =
KBr + KBrO3 + HCl =
4. Покажите различные способы индикации в титриметрическом анализе. Приведите примеры.
5. Раскройте основы метода титриметрического анализа: обоснование, основное уравнение, особенности приготовления рабочих растворов, установочные вещеcтва, индикация, способы титрирования, возможности метода ацидиметрии. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 1 моль/л H2SO4, V=2 л.
Вариант № 21
1. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения анионов при совместном присутствии CO32-, SO42-, S2-.
2. Дайте определение внутрикоплексных соединений. Какое свойство этих соединений делает возможным их широкое применение в качественном анализе. Напишите уравнения реакций на примере диметилглиоксимата никеля, ализарината алюминия; объясните их образование, укажите типы химических связей.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
KBr + KMnO4 + H2SO4 = Na2S2O3 +J2 =
H2O2+ KJ + H2SO4 =
4. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, являются ли эквивалент вещества постоянной величиной, от чего он зависит?
K2CO3 + 2HCl =2KCl + CO2 + H2O
K2CO3 + H3PO4 = KH2PO4 + KHCO3
MnSO4 + 2KOH = Mn(OH)2 + K2SO4
MnSO4 + 2Cl2 + 8KOH = K2MnO4 + 4KCl + K2SO4 + 4H2O
5. Раскройте основы метода трилонометрия: обоснования, основное уравнение особенности приготовления рабочих; установочные вещества индикация, способы титрования, возможности метода. Рассчитайте навеску вещества необходимую для приготовления рабочих растворов, концентрации 0,5 моль /л Na2H2Y, объемом 2,5 л.
Вариант № 22
1. Объясните и напишите уравнения химических реакций. Что называется «содовой вытяжкой» или «приготовленным раствором» для открытия анионов? Приведите примеры.
2. Составьте в молекулярном и ионном виде уравнения следующих химических реакций в водном растворе:
(NH4)2SO4 насыщ. + CaCl2 ® ; Na2S + CrCl3 ®
3. Дайте обоснование оптическим методам анализа. Объединенный Закон светопоглощения. Перечислите способы определений и укажите их сущность, достоинства, недостатки метода. Приведите примеры.
4. Дайте формулировку основного закона титриметрического анализа, приведите его математическое выражение. Дайте определение понятий: точка эквивалентности, конечная точка титрования, покажите связь между ними.
5. Дайте определение рН-индикаторам, укажите требования к ним, их характеристики: интервал перехода окраски. Обоснуйте принцип выбора индикатора.
Вариант № 23
1. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения анионов при совместном присутствии J-,NO2-, CH3COO-.
2. Раскройте основные положения теории растворов электролитов, используемых в аналитической химии, а также понятия о сильных и слабых электролитах, константе и степени электролитической диссоциации. Их математические выражения. Покажите влияние на степень диссоциации слабых электролитов добавления электролита с одноименным ионом. Напишите формулы известных Вам сильных кислот и оснований, слабых кислот и оснований, применяемых в качестве реагентов.
3. Закончите и уравняйте ионно–электронным методом или методом электронного баланса уравнения окислительно-восстановительных реакций:
KJ + KMnO4 + H2SO4 =
KCrO4 + H2O2 + KOH =
Na2S2O3 + J2 =
4. Дайте определение рН-индикаторам, укажите требования к ним, их характеристики: интервал перехода окраски. Обоснуйте принцип выбора индикатора.
5. Рассчитайте содержание цинка в растворе, если на титрование пошло 10,8 мл 0,1 н трилона Б?
Вариант № 24
1. Объясните и напишите уравнения химических реакций. Что произойдет при подкислении раствора, содержащего Na+, J-, NO2-,SO32- ионы?
2. Дайте понятие константы устойчивости и константы нестойкости комплексного иона. Укажите способы разрушения комплексных ионов. Напишите уравнения реакций и объясните, почему раствор хлорида диамин серебра (1) разрушается под действием концентрированной азотной кислоты или калия иодида.
3. Закончите и уравняйте методом электронного баланса или методом полуреакций уравнения окислительно-восстановительных реакций:
KJ + KBrO3 + HCl = ; Na2S + KMnO4 + H2O = ;
H2C2O4 + KMnO4 + H2SO4 = ;
4. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите является ли эквивалент веществ постоянной величиной, от чего он зависит?
K2Cr2O7 + 2BaCl2 + H2O = 2BaCrO4 + 2HCl + 2KCl
K2Cr2O7 + 6KJ + 7H2SO4 = 3J2 + 4K2SO4 + Cr2(SO4)3 + 7H2O
K2Cr2O7 + 4AgNO3 + H2O = 2Ag2CrO4 + 2KNO3 + 2HNO3
5. Раскройте основы метода аргентометрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,05 моль/л AgNO3 (метод Мора), объемом 6 л.
Вариант № 25
1. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения анионов при совместном присутствии SO42-, S2-, SO32-, S2O32-.
2. Составьте в молекулярном и ионном виде уравнения следующих химических реакций в водном растворе:
NH4OH + CrCl3 ; NH4OH конц. (изб.)+ CoCl2 ®
3. Дайте формулировку основного закона титриметрического анализа, приведите его математическое выражение. Дайте определение понятий: точка эквивалентности, конечная точка титрования, покажите связь между ними.
4. Объясните, на чем основан метод совместного определения Na2CO3 и NaHCO3 с применением двух индикаторов: фенолфталеина и метилоранжа.
5. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите является ли эквивалент веществ постоянной величиной, от чего он зависит?
3KJ + KBrO3 + 6HCl = 3JCl + KBr + 3KCl + 3H2O
2KJ + H2O2 + H2SO4 = J2 + K2SO4 +2H2O
2KJ + Hg(NO3)2 = HgJ2 + 2KNO3.
Вариант № 26
1. Объясните и напишите уравнения химических реакций. Почему мешающее влияние сульфит и тиосульфат – ионов при обнаружении карбонат – ионов устраняют в нейтральной среде перманганатом калия?
2. Дайте определение амфотерности с точки зрения теории электролитической диссоциации. Охарактеризуйте равновесие в водных растворах амфотерных гидроксидов, покажите условия смещения равновесия (на примере IV группы катионов).
3. Рассчитайте содержание цинка в растворе, если на титрование пошло 10,8 мл 0,1 н трилона Б?
4. Покажите способы выражения концентраций растворов в титриметрическом анализе: молярная концентрация, молярная концентрация эквивалента, титр, титр раствора по определяемому веществу. Что такое поправочный коэффициент? Его значение, формулы расчета.
5. Раскройте основы метода йодометрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,2 моль/л J2, объемом 4 л.
Вариант № 27
1. Предложите рациональную схему анализа и приведите уравнения реакций, лежащих в основе разделения и обнаружения анионов при совместном присутствии Cl-, Br-, J-.
2. Дайте определение и характеристику комплексных соединений: равновесие в растворах, особенности и способы получения. Покажите применение комплексных соединений в качественном анализе: для маскировки мешающих ионов, для обнаружения ионов, для растворения труднорастворимых соединений.
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно – восстановительных реакций:
H2O2 + KMnO4 + H2SO4 == KJ + FeCl3 =
Na2S2O3 + j2 + H2O =
4. Рассчитайте факторы эквивалентности, эквиваленты реагирующих веществ. Укажите, является ли эквивалент веществ постоянной величиной, от чего он зависит?
10KJ + 2KMnO4 + 8H2SO4 = 5J2 + 2MnSO4 + 6K2SO4 + 8H2O
5KJ + 6KMnO4 + 9H2SO4 = 5KJO3 + 6MnSO4 + 3H2SO4 + 9H2O
5KJ + 2KMnO4 + 16HCl = 5JCl2 + 2MnCl2 + 7KCl + 8H2O
5. Раскройте основы метода перманганатометрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,1 моль/л KMnO4 , объемом 500мл.
Вариант № 28
1. Объясните и напишите уравнения химических реакций. Почему при действии на соли бария дихроматом калия образуется BaCrO4? Почему реакцию необходимо проводить в присутствии уксусной кислоты?
2. Составьте в молекулярном и ионном виде уравнения следующих химических реакций в водном растворе:
Pb(CH3Coo)2 + HCl ® Al2(SO4)3 + Co(NO3)2 ®
3. Закончите и уравняйте методом электронного баланса или полуреакций уравнения окислительно-восстановительных реакций:
KJ + NaNO2 + HCl = CrCl3 + KMnO4 + H2O =
K2C2O4 + KMnO4 + H2SO4 =
4. Раскройте понятие «весовая форма в гравиметрическом анализе», укажите основные требования к ней. Укажите достоинства и недостатки весовых форм BaSO4, CaC2O4, Fe2O3, CaO.
5. Раскройте основы метода алкалиметрии: обоснование, основное уравнение, особенности приготовления рабочих растворов; установочные вещества, индикация, способы титрования, возможности метода. Рассчитайте навеску вещества, необходимую для приготовления рабочих растворов, концентрации 0,5 моль/л КОН V=250 мл.
Основные формулы, используемые в аналитической химии и примеры решения задач
Титриметрический анализ
Титриметрический анализ объединяет группу методов количественного химического анализа, основанных на измерении количества реагента, необходимого для взаимодействия с определяемым компонентом.
Количественные соотношения между реагирующими веществами выражаются законом эквивалентов:
Химические элементы и их соединения взаимодействуют в химических реакциях друг с другом в строго определенных массовых количествах, соответствующих их химическим эквивалентам.
Эквивалент (Э) – реальная или условная частица вещества Х, которая эквивалентна одному иону водорода в кислотно-основной реакции или одному электрону окислительно-восстановительной реакции (должна быть указана конкретная химическая реакция).
Э = fЭ (Х) Х
Фактор эквивалентности (fЭ) – число, обозначающее, какая доля реальной частицы вещества эквивалентна одному иону водорода в кислотно-основной реакции или одному электрону в окислительно-восстановительной реакции.
fЭ (Х) = 1/z; где: z – число эквивалентности
при fЭ = 1 Þ Э = РЧ (реальная частица); при fЭ < 1 Þ Э = УЧ (условная частица).
Масса 1 моль эквивалента называется молярной массой эквивалента (МЭ).
МЭ = fЭ ´ М
Важным следствием закона эквивалентов является основное уравнение титриметрии:
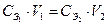
Произведение молярной концентрации эквивалента (СЭ) на объем раствора есть величина постоянная для обоих реагирующих веществ.
Расчеты в титриметрии основаны на принципе эквивалентности.
При выполнении расчетов следует учитывать некоторые метрологические правила: концентрация и масса вычисляются до четвертой значащей цифры после запятой, титр – до четвертой значащей цифры после нулей, объем и массовая доля в % – до сотых долей. Значащими являются все цифры, отличные от нуля. Сам нуль может быть значащим, если расположен между значащими цифрами или после них. Лишние цифры рекомендуется округлять.
