Задачи для самостоятельного решения. 81-100. Для данной реакции подберите коэффициенты методом электронного баланса
81-100. Для данной реакции подберите коэффициенты методом электронного баланса. Укажите окислитель и восстановитель.
81. KClO3 + Na2SO3 + = KCl + Na2SO4.
82. Au + HNO3 + HCl = AuCl3 + NO + H2O.
83. P + HNO3 + H2O = H3PO4 + NO.
84. Cl2 + I2 + H2O = HCl + HIO3.
85. MnS + HNO3 = MnSO4 + NO2 + H2O.
86. HCl + HNO3 = Cl2 + NO + H2O.
87. H2S + HNO3 = S + NO + H2O.
88. HClO4 + SO2 + H2O = HCl + H2SO4.
89. As + HNO3 = H3AsO4 + NO2 + H2O.
90. KI + KNO2 +H2SO4 = I2 + NO + K2SO4 + H2O.
91. KNO2 + S = K2S + N2 + SO2.
92. HI + H2SO4 = I2 + H2S + H2O.
93. H2SO3 + H2S = S + H2O.
94. H2SO3 + H2S = S + H2O.
95. Cr2(SO4)3 + Br2 + KOH = K2CrO4 + KBr + K2SO4 + H2O.
96. P + H2SO4 = H3PO4 + SO2 + H2O.
97. H2S + Cl2 + H2O = H2SO4 + HCl.
98. P + HIO3 + H2O = H3PO4 + HI.
99. NaAsO2 + I2 + NaOH = Na3AsO4 + HI.
100. K2Cr2O7 + SnCl2 + HCl = CrCl3 + SnCl4 + KCl + H2O.
101. Составьте гальваническую цепь, имея в распоряжении Cu, Pb, CuCl2 и Pb(NO3)2. Напишите уравнения электродных процессов и вычислите ЭДС этого элемента (концентрации растворов равны 1 моль/л).
Ответ: ЭДС = 0,463 В.
102. Составьте схему гальванического элемента, состоящего из железной и оловянной пластинок, погруженных в растворы хлоридов железа (II) и олова (II) соответственно. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента (концентрации растворов равны 1 моль/л).
Ответ: ЭДС = 0,314 В.
103. Гальванический элемент составлен по схеме: Ni | NiSO4 (0,1 M) || AgNO3 (0,1 M) | Ag. Напишите уравнения электродных процессов и вычислите ЭДС этого элемента.
Ответ: ЭДС =1,019 В.
104. Составьте схему гальванического элемента, состоящего из железной и ртутной пластинок, погруженных в растворы своих солей. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента (концентрации растворов равны 1 моль/л).
Ответ: ЭДС =1,294 В.
105. Из четырех металлов Ag, Cu, Al и Sn выберите те пары, которые дают наименьшую и наибольшую ЭДС составленного из них гальванического элемента.
Ответ: пара Cu и Ag имеет минимальную ЭДС, пара Al и Ag – максимальную ЭДС.
106. Составьте схему двух гальванических элементов, в одном из которых свинец являлся бы катодом, а в другом – анодом. Напишите уравнения электродных процессов и вычислите ЭДС каждого элемента.
107. Составьте схему гальванического элемента, состоящего из свинцовой и цинковой пластинок, погруженных в растворы своих солей, где [Pb2+] = [Zn2+] = 0,01 моль/л. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,637 В.
108. Составьте схему гальванического элемента, состоящего из алюминиевой и цинковой пластинок, погруженных в растворы своих солей, где [Al3+] = [Zn2+] = 0,1 моль/л. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,899 В.
109. Составьте схему гальванического элемента, у которого один электрод никелевый с [Ni2+] = 0,1 моль/л, а второй – свинцовый с [Pb2+] = 0,0001 моль/л. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС =0,035 В.
110. Составьте схему гальванического элемента, состоящего из цинковой пластинки, погруженной в 0,1 М раствор нитрата цинка, и свинцовой пластинки, погруженной в 1 М раствор нитрата свинца. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,666 В.
111.Составьте схему гальванического элемента, у которого один электрод никелевый с [Ni2+] = 0,1 моль/л, а второй – свинцовый с [Pb2+] = 0,0001 моль/л. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,035 В.
112. Составьте схему гальванического элемента, состоящего из кадмиевой пластинки, погруженной в 0,1 М раствор сульфата кадмия, и серебряной пластинки, погруженной в 0,01 М раствор нитрата серебра. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 1,113 В.
113. Составьте схему гальванического элемента, состоящего из двух алюминиевых пластинок, опущенных в растворы его соли с концентрацией [Al3+] = 1 моль/л у одного электрода и [Al3+] = 0,1 моль/л у другого электрода. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,029 В.
114. Составьте схему гальванического элемента, состоящего из двух серебряных электродов, опущенных в 0,0001 моль/л и 0,1 моль/л растворы AgNO3. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,563 В.
115. Напишите уравнения электродных процессов, суммарную реакцию и вычислите ЭДС гальванического элемента Ni | NiSO4 (0,01 M) || Cu(NO3)2 (0,1 M) | Cu.
Ответ: ЭДС = 0,596 В.
116. Составьте схему гальванического элемента, состоящего из кадмиевой пластинки, погруженной в 0,1 М раствор нитрата кадмия, и серебряной пластинки, погруженной в 1 М раствор нитрата серебра. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 1,233 В.
117. Составьте схему гальванического элемента, состоящего из двух алюминиевых пластинок, опущенных в растворы его соли с концентрацией [Al3+] = 1 моль/л у одного электрода и [Al3+] = 0,01 моль/л у другого электрода. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,059 В.
118. Составьте схему гальванического элемента, состоящего из двух медных электродов, опущенных в 0,001 М и 0,1 М растворы Сu(NO3)2. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,059 В.
119. Составьте схему гальванического элемента, состоящего из двух никелевых пластинок, опущенных в растворы никелевой соли с концентрацией [Ni2+] = 1 моль/л у одного электрода и [Ni2+] = 0,01 моль/л у другого электрода. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,059 В.
120. Составьте схему гальванического элемента, состоящего из двух свинцовых электродов, опущенных в 0,001 моль/л и 1 моль/л растворы Pb(NO3)2. Напишите уравнения электродных процессов и вычислите ЭДС данного элемента.
Ответ: ЭДС = 0,088 В.
Контрольные вопросы
1.Что называют гальваническим элементом? Описать принцип его работы.
2.Что такое стандартный электродный потенциал?
3.Что такое электродвижущая сила гальванического элемента? Как рассчитывается ЭДС гальванического элемента для стандартных условий и условий, отличных от стандартных?
4.В чем отличие металлических и концентрационных гальванических элементов?
5.Какие процессы протекают при работе гальванического элемента, состоящего из железного и серебряного электродов, опущенных в растворы своих солей?
6.Составьте схемы гальванических элементов, в которых ртутный электрод является: а) анодом; б) катодом.
7.Что такое электролиз?
8.Назовите продукты электролиза водного раствора нитрата меди на нерастворимом аноде.
9.Дайте определение явления перенапряжения. Когда оно возникает?
Коррозия металлов
Коррозия – это самопроизвольный процесс разрушения материалов и изделий из них в результате физико-химического воздействия окружающей среды, при котором металл переходит в окисленное (ионное) состояние и теряет присущие ему свойства.
Металлы и сплавы, приходя в соприкосновение с окружающей средой (газообразной или жидкой), подвергаются разрушению. Скорость коррозии металлов и металлических покрытий в атмосферных условиях определяется комплексным воздействием ряда факторов: наличием на поверхности адсорбированной влаги, загрязненностью воздуха коррозионно-агрессивными веществами, изменением температуры воздуха и металла, природой продуктов коррозии и т. д.
Согласно законам химической термодинамики коррозионные процессы возникают и протекают самопроизвольно лишь при условии уменьшения энергии Гиббса системы (∆G<0).
6.1.1.Классификация коррозионных процессов
1. По типу разрушенийкоррозия бывает сплошной и местной. При равномерном распределении коррозионных разрушений она не представляет собой опасности для конструкций и аппаратов, особенно в тех случаях, когда потери металлов не превышают технически обоснованных норм. Местная коррозия гораздо опаснее, хотя потери металла могут быть и небольшими. Опасность состоит в том, что, снижая прочность отдельных участков, она резко уменьшает надёжность конструкций, сооружений, аппаратов.
2.По условиям протеканияразличают: атмосферную, газовую, жидкостную, подземную, морскую, почвенную коррозию, коррозию блуждающими токами, коррозию под напряжением и др.
3. По механизму коррозионного процесса различают химическую и электрохимическую коррозию.
Химическая коррозия может протекать при взаимодействии с сухими газообразными окислителями и растворами неэлектролитов. С газами большинство металлов взаимодействует при повышенных температурах. При этом на поверхности протекают два процесса: окисление металла и накопление продуктов окисления, которые иногда предотвращают дальнейшую коррозию. В общем виде уравнение реакции окисления металлов кислородом выглядит следующим образом:
xM + y/2 O2 = MxOy. (1)
Энергия Гиббса окисления металлов равна энергии Гиббса образования оксидов, т. к. ∆G образования простых веществ равна 0. Для реакции окисления (1) она равна
∆G=∆G0 – 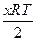 lnpO2,
lnpO2,
где ∆G0 – стандартная энергия Гиббса реакции; pO2– относительное давление кислорода.
Способы защиты от газовой коррозии: легирование металлов, создание защитных покрытий на поверхности и изменение свойств газовой среды.
Электрохимическая коррозия металлов развивается при контакте металла с растворами электролитов (все случаи коррозии в водных растворах, т. к. даже чистая вода является слабым электролитом, а морская вода – сильным). Основные окислители – это вода, растворенный кислород и ионы водорода.
Причина электрохимической коррозии состоит в том, что поверхность металла всегда является энергетически неоднородной из-за наличия примесей в металлах, различий по химическому и фазовому составу сплава и др. Это приводит к образованию на поверхности во влажной атмосфере микрогальванических элементов. На участках металла, имеющих более отрицательное значение потенциала, происходит процесс окисления этого металла:
М0+ nе–=Мn+(анодный процесс).
Окислители, принимающие электроны у катода, называются катодными деполяризаторами. Катодными деполяризаторами служат: ионы водорода (водородная деполяризация), молекулы кислорода (кислородная деполяризация).
На катодных участках поверхности происходит восстановление окислителей (табл..1).
Таблица 1
