Количественные характеристики реакции гидролиза
Степень гидролиза (aгидр.) - отношение числа гидролизованных молекул к общему числу растворённых молекул (выражается в процентах):
aгидр. = ([C]гидр. / [C]раств.) • 100%
Степень гидролиза зависит от химической природы образующейся при гидролизе кислоты (основания) и будет тем больше, чем слабее кислота (основание) (в определённых равных условиях).
ОСНОВНЫЕ КЛАССЫ
НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Классификация неорганических веществ
Основания
Оксиды
Кислоты
Соли
Генетическая связь
КЛАССИФИКАЦИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Простые вещества. Молекулы состоят из атомов одного вида (атомов одного элемента). В химических реакциях не могут разлагаться с образованием других веществ.
Сложные вещества (или химические соединения). Молекулы состоят из атомов разного вида (атомов различных химических элементов). В химических реакциях разлагаются с образованием нескольких других веществ.
| Неорганические вещества | |
| Простые | Металлы |
| Неметаллы | |
| Сложные | Оксиды |
| Основания | |
| Кислоты | |
| Соли |
Резкой границы между металлами и неметаллами нет, т.к. есть простые вещества, проявляющие двойственные свойства.
Аллотропия
Аллотропия - способность некоторых химических элементов образовывать несколько простых веществ, различающихся по строению и свойствам.
С - алмаз, графит, карбин.
O - кислород, озон.
S - ромбическая, моноклинная, пластическая.
P - белый, красный, чёрный.
Явление аллотропии вызывается двумя причинами:
1) различным числом атомов в молекуле, например кислород O2 и озон O3
2) образованием различных кристаллических форм, например алмаз и графит.
ОСНОВАНИЯ
Основания - сложные вещества, в которых атомы металлов соединены с одной или несколькими гидроксильными группами (с точки зрения теории электролитической диссоциации, основания - сложные вещества, при диссоциации которых в водном растворе образуются катионы металла (или NH4+) и гидроксид - анионы OH-).
Классификация. Растворимые в воде (щёлочи) и нерастворимые. Амфотерные основания проявляют также свойства слабых кислот.
Получение
1. Реакции активных металлов ( щелочных и щелочноземельных металлов) с водой:
2Na + 2H2O ® 2NaOH + H2
Ca + 2H2O ® Ca(OH)2 + H2
2. Взаимодействие оксидов активных металлов с водой:
BaO + H2O ® Ba(OH)2
3. Электролиз водных растворов солей
2NaCl + 2H2O ® 2NaOH + H2 + Cl2
Химические свойства
| Щёлочи | Нерастворимые основания |
| 1. Действие на индикаторы. | |
| лакмус - синий метилоранж - жёлтый фенолфталеин - малиновый | –– |
| 2. Взаимодействие с кислотными оксидами. | |
| 2KOH + CO2 ® K2CO3 + H2O KOH + CO2 ® KHCO3 | –– |
| 3. Взаимодействие с кислотами (реакция нейтрализации) | |
| NaOH + HNO3 ® NaNO3 + H2O | Cu(OH)2 + 2HCl ® CuCl2 + 2H2O |
| 4. Обменная реакция с солями | |
| Ba(OH)2 + K2SO4 ® 2KOH + BaSO4¯ 3KOH+Fe(NO3)3 ® Fe(OH)3¯ + 3KNO3 | –– |
| 5. Термический распад. | |
| –– | Cu(OH)2 –t°® CuO + H2O |
ОКСИДЫ
Классификация
Оксиды - это сложные вещества, состоящие из двух элементов, один из которых кислород.
| ОКСИДЫ | |
| Несолеобразующие | CO, N2O, NO |
| Солеобразующие | Основные-это оксиды металлов, в которых последние проявляют небольшую степень окисления +1, +2 Na2O; MgO; CuO |
| Амфотерные (обычно для металлов со степенью окисления +3, +4). В качестве гидратов им соответствуют амфотерные гидроксиды ZnO; Al2O3; Cr2O3; SnO2 | |
| Кислотные -это оксиды неметаллов и металлов со степенью окисления от +5 до +7 SO2; SO3; P2O5; Mn2O7; CrO3 | |
| Основным оксидам соответствуют основания, кислотным– кислоты, амфотерным – и те и другие |
Получение
1. Взаимодействие простых и сложных веществ с кислородом:
2Mg + O2 ® 2MgO
4P + 5O2 ® 2P2O5
S + O2 ® SO2
2CO + O2 ® 2CO2
2CuS + 3O2 ® 2CuO + 2SO2
CH4 + 2O2 ® CO2 + 2H2O
4NH3 + 5O2 –кат.® 4NO + 6H2O
2. Разложение некоторых кислородсодержащих веществ (оснований, кислот, солей) при нагревании:
Cu(OH)2 –t°® CuO + H2O
(CuOH)2CO3 –t°® 2CuO + CO2 + H2O
2Pb(NO3)2 –t°® 2PbO + 4NO2 + O2
2HMnO4 –t°;H2SO4(конц.)® Mn2O7 + H2O
Химические свойства
| Основные оксиды | Кислотные оксиды |
| 1. Взаимодействие с водой | |
| Образуется основание: Na2O + H2O ® 2NaOH CaO + H2O ® Ca(OH)2 | Образуется кислота: SO3 + H2O ® H2SO4 P2O5 + 3H2O ® 2H3PO4 |
| 2. Взаимодействие с кислотой или основанием: | |
| При реакции с кислотой образуется соль и вода MgO + H2SO4 –t°® MgSO4 + H2O CuO + 2HCl –t°® CuCl2 + H2O | При реакции с основанием образуется соль и вода CO2 + Ba(OH)2 ® BaCO3 + H2O SO2 + 2NaOH ® Na2SO3 + H2O |
| Амфотерные оксиды взаимодействуют | |
| с кислотами как основные: ZnO + H2SO4 ® ZnSO4 + H2O | с основаниями как кислотные: ZnO + 2NaOH ® Na2ZnO2 + H2O (ZnO + 2NaOH + H2O ® Na2[Zn(OH)4]) |
| 3. Взаимодействие основных и кислотных оксидов между собой приводит к солям. | |
| Na2O + CO2 ® Na2CO3 | |
| 4. Восстановление до простых веществ: | |
| 3CuO + 2NH3 ® 3Cu + N2 + 3H2O P2O5 + 5C ® 2P + 5CO |
КИСЛОТЫ
Кислоты - сложные вещества, состоящие из атомов водорода и кислотного остатка. (С точки зрения теории электролитической диссоциации: кислоты - электролиты, которые при диссоциации в качестве катионов образуют только H+).
Классификация
1. По составу: бескислородные и кислородсодержащие.
2. По числу атомов водорода, способных замещаться на металл: одно-, двух-, трёхосновные...
| Бескислородные: | Название соли | |
| HCl - хлористоводородная (соляная) | одноосновная | хлорид |
| HBr - бромистоводородная | одноосновная | бромид |
| HI - йодистоводородная | одноосновная | йодид |
| HF - фтористоводородная (плавиковая) | одноосновная | фторид |
| H2S - сероводородная | двухосновная | сульфид |
| Кислородсодержащие: | ||
| HNO3 – азотная | одноосновная | нитрат |
| H2SO3 - сернистая | двухосновная | сульфит |
| H2SO4 – серная | двухосновная | сульфат |
| H2CO3 - угольная | двухосновная | карбонат |
| H2SiO3 - кремниевая | двухосновная | силикат |
| H3PO4 - ортофосфорная | трёхосновная | ортофосфат |
Получение
1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот):
SO3 + H2O ® H2SO4
P2O5 + 3H2O ® 2H3PO4
2. Взаимодействие водорода с неметаллом и последующим растворением полученного продукта в воде (для бескислородных кислот):
H2 + Cl2 ® 2HCl
H2 + S ® H2S
3. Реакциями обмена соли с кислотой
Ba(NO3)2 + H2SO4 ® BaSO4¯ + 2HNO3
в том числе, вытеснение слабых, летучих или малорастворимых кислот из солей более сильными кислотами:
Na2SiO3 + 2HCl ® H2SiO3¯ + 2NaCl
2NaCl(тв.) + H2SO4(конц.) –t°® Na2SO4 + 2HCl
Химические свойства
1. Действие на индикаторы.
лакмус - красный
метилоранж - розовый
2. Взаимодействие с основаниями (реакция нейтрализации):
H2SO4 + 2KOH ® K2SO4 + 2H2O
2HNO3 + Ca(OH)2 ®Ca(NO3)2 + 2H2O
3. Взаимодействие с основными оксидами:
CuO + 2HNO3 –t°® Cu(NO3)2 + H2O
4. Взаимодействие с металлами:
Zn + 2HCl ® ZnCl2 + H2
2Al + 6HCl ® 2AlCl3 + 3H2
(металлы, стоящие в ряду напряжений до водорода, кислоты-неокислители).
5. Взаимодействие с солями (реакции обмена), при которых выделяется газ или образуется осадок:
H2SO4 + BaCl2 ® BaSO4¯ +2HCl
2HCl + K2CO3 ® 2KCl + H2O + CO2
СОЛИ
Соли - сложные вещества, которые состоят из атомов металла и кислотных остатков. Это наиболее многочисленный класс неорганических соединений.
Классификация
| СОЛИ | |
| Средние | |
| Кислые | |
| Основные | |
| Двойные | |
| Смешанные | |
| Комплексные |
Средние. При диссоциации дают только катионы металла (или NH4+)
Na2SO4 « 2Na+ +SO42-
CaCl2 « Ca2+ + 2Cl-
Кислые. При диссоциации дают катионы металла (NH4+), ионы водорода и анионы кислотного остатка.
NaHCO3 « Na+ + HCO3- « Na+ + H+ + CO32-
Продукты неполного замещения атомов водорода многоосновной кислоты на атомы металла.
Основные. При диссоциации дают катионы металла, анионы гидроксила и кислотного остатка.
Zn(OH)Cl « [Zn(OH)]+ + Cl- « Zn2+ + OH- + Cl-
Продукты неполного замещения групп OH соответствующего основания на кислотные остатки.
Двойные. При диссоциации дают два катиона и один анион.
KAl(SO4)2 « K+ + Al3+ + 2SO42-
Смешанные. Образованы одним катионом и двумя анионами:
CaOCl2 « Ca2+ + Cl- + OCl-
Комплексные. Содержат сложные катионы или анионы.
[Ag(NH3)2]Br « [Ag(NH3)2]+ + Br -
Na[Ag(CN)2] « Na+ + [Ag(CN)2]-
Средние соли
Получение
Большинство способов получения солей основано на взаимодействии веществ с противоположными свойствами:
1) металла с неметаллом:
2Na + Cl2 ® 2NaCl
2) металла с кислотой:
Zn + 2HCl ® ZnCl2 + H2
3) металла с раствором соли менее активного металла
Fe + CuSO4 ® FeSO4 + Cu
4) основного оксида с кислотным оксидом:
MgO + CO2 ® MgCO3
5) основного оксида с кислотой
CuO + H2SO4 –t°® CuSO4 + H2O
6) основания с кислотным оксидом
Ba(OH)2 + CO2 ® BaCO3¯ + H2O
7) основания с кислотой:
Ca(OH)2 + 2HCl ® CaCl2 + 2H2O
8) соли с кислотой:
MgCO3 + 2HCl ® MgCl2 + H2O + CO2
BaCl2 + H2SO4 ® BaSO4¯ + 2HCl
9) раствора основания с раствором соли:
Ba(OH)2 + Na2SO4 ® 2NaOH + BaSO4¯
10) растворов двух солей
3CaCl2 + 2Na3PO4 ® Ca3(PO4)2¯ + 6NaCl
Химические свойства
1. Термическое разложение.
CaCO3 ® CaO + CO2
2Cu(NO3)2 ® 2CuO + 4NO2 + O2
NH4Cl ® NH3 + HCl
2. Гидролиз.
Al2S3 + 6H2O « 2Al(OH)3¯ + 3H2S
FeCl3 + H2O « Fe(OH)Cl2 + HCl
Na2S + H2O « NaHS +NaOH
3. Обменные реакции с кислотами, основаниями и другими солями.
AgNO3 + HCl ® AgCl¯ + HNO3
Fe(NO3)3 + 3NaOH ® Fe(OH)3¯ + 3NaNO3
CaCl2 + Na2SiO3 ® CaSiO3¯ + 2NaCl
4. Окислительно-восстановительные реакции, обусловленные свойствами катиона или аниона.
2KMnO4 + 16HCl ® 2MnCl2 + 2KCl + 5Cl2 + 8H2O
Кислые соли
Получение
1. Взаимодействие кислоты с недостатком основания.
KOH + H2SO4 ® KHSO4 + H2O
2. Взаимодействие основания с избытком кислотного оксида
Ca(OH)2 + 2CO2 ® Ca(HCO3)2
3. Взаимодействие средней соли с кислотой
Ca3(PO4)2 + 4H3PO4 ® 3Ca(H2PO4)2
Химические свойства.
1. Термическое разложение с образованием средней соли
Ca(HCO3)2 ® CaCO3¯ + CO2 + H2O
2. Взаимодействие со щёлочью. Получение средней соли.
Ba(HCO3)2 + Ba(OH)2 ® 2BaCO3¯ + 2H2O
Основные соли
Получение
1. Гидролиз солей, образованных слабым основанием и сильной кислотой
ZnCl2 + H2O ® [Zn(OH)]Cl + HCl
2. Добавление (по каплям) небольших количеств щелочей к растворам средних солей металлов
AlCl3 + 2NaOH ® [Al(OH)2]Cl + 2NaCl
3. Взаимодействие солей слабых кислот со средними солями
2MgCl2 + 2Na2CO3 + H2O ® [Mg(OH)]2CO3¯ + CO2 + 4NaCl
Химические свойства.
1. Термическое разложение.
[Cu(OH)]2CO3(малахит) ® 2CuO + CO2 + H2O
2. Взаимодействие с кислотой: образование средней соли.
Sn(OH)Cl + HCl « SnCl2 + H2O
Комплексные соли
Строение
| K4[Fe(CN)6] | |
| K4[Fe(CN)6] | – Внешняя сфера |
| K4[Fe(CN)6] | – Внутренняя сфера |
| K4[Fe(CN)6] | – Комплексообразователь (центральный атом) |
| K4[Fe(CN)6] | – Координационное число |
| K4[Fe(CN)6] | – Лиганд |
Центральными атомами обычно служат ионы металлов больших периодов (Co, Ni, Pt, Hg, Ag, Cu); типичными лигандами являются OH-, CN-, NH3, CO, H2O; они связаны с центральным атомом донорно-акцепторной связью.
Получение
1. Реакции солей с лигандами:
AgCl + 2NH3 ® [Ag(NH3)2]Cl
FeCl3 + 6KCN ® K3[Fe(CN)6] + 3KCl
Химические свойства.
1. Разрушение комплексов за счёт образования малорастворимых соединений:
2[Cu(NH3)2]Cl + K2S ® CuS¯ + 2KCl + 4NH3
2. Обмен лигандами между внешней и внутренней сферами.
K2[CoCl4] + 6H2O ® [Co(H2O)6]Cl2 + 2KCl
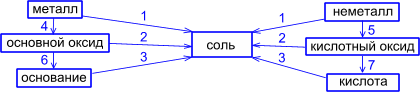
ГЕНЕТИЧЕСКАЯ СВЯЗЬ
МЕЖДУ РАЗЛИЧНЫМИ КЛАССАМИ СОЕДИНЕНИЙ
 |
Примеры
1. металл + неметалл ® соль
Hg + S ® HgS
2Al + 3I2 ® 2AlI3
2. основной оксид + кислотный оксид ® соль
Li2O + CO2® Li2CO3
CaO + SiO2 ® CaSiO3
3. основание + кислота ® соль
Cu(OH)2 + 2HCl ® CuCl2 + 2H2O
| FeCl3 | + | 3HNO3 | ® | Fe(NO3)3 | + | 3HCl |
| соль | кислота | соль | кислота |
4. металл ® основной оксид
2Ca + O2 ® 2CaO
4Li + O2 ® 2Li2O
5. неметалл ® кислотный оксид
S + O2 ® SO2
4As + 5O2 ® 2As2O5
6. основной оксид ® основание
BaO + H2O ® Ba(OH)2
Li2O + H2O ® 2LiOH
7. кислотный оксид ® кислота
P2O5 + 3H2O ® 2H3PO4
SO3 + H2O ® H2SO4
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
ЭЛЕКТРОХИМИЯ
Окислительно- восстановительные реакции
Электрохимия
