Систематическая номенклатура
Основная статья: Систематическая номенклатура альдегидов и кетонов
По номенклатуре ИЮПАК названия простых альдегидов образуются от названий соответствующих алканов с добавлением суффикса -аль, а диальдегидов — суффикса -диаль (в данном случае атом углерода альдегидной группы уже входит в состав родоначального алкана). При этом в названии номер при альдегидной группе, как правило, не ставят, поскольку она всегда занимает крайнее положение. Если карбонильная группа не входит в родоначальную структуру (например, если родоначальной структурой является циклический углеводород или гетероцикл), то к названию добавляется суффикс -карбальдегид[5][6].
Если в данном соединении альдегидная группа не является старшей, то в таких случаях её обозначают используя приставку формил-, указывая её положение[6].
В устаревших Женевской (1892) и Льежской (1930) номенклатурах, впоследствии заменённых систематической номенклатурой ИЮПАК, альдегиды обозначались при помощи суффикса -ал[7].
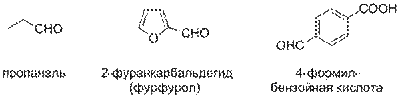
Классификация альдегидов
Альдегиды классифицируются следующим образом (в скобках приведены примеры)[8]:
- В зависимости от насыщенности углеводородного заместителя:
- предельные (насыщенные) альдегиды (ацетальдегид);
- непредельные (ненасыщенные) альдегиды (акролеин);
- ароматические альдегиды (бензальдегид).
- По числу карбонильных групп:
- альдегиды с одной карбонильной группой (формальдегид);
- диальдегиды (глиоксаль);
- многоатомные альдегиды.
Нахождение в природе
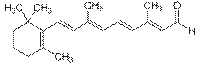
Структурная формула ретиналя
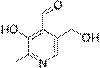
Пиридоксаль
Альдегидная группа содержится во многих природных веществах, таких, как углеводы (альдозы), некоторые витамины (ретиналь, пиридоксаль). Их следы содержатся в эфирных маслах и часто способствуют их приятному запаху, например, коричный альдегид (в кассиевом масле его может быть до 75 %, а в цейлонском коричном масле даже до 90 %) и ванилин.
Алифатический альдегид СН3(СН2)7С(Н)=О (тривиальное название — пеларгоновый альдегид) содержится в эфирных маслах цитрусовых растений, обладает запахом апельсина, его используют как пищевой ароматизатор[9].
Цитраль содержится в лемонграссовом и кориандровом маслах (до 80 %), цитронеллаль — в цитронелловом (приблизительно 30 %) и эвкалиптовом, бензальдегид — в масле горького миндаля. Куминовый альдегид содержится в масле тмина, гелиотропин — в масле гелитропа и сирени, анисовый альдегид и жасминальдегид в небольших количествах содержатся во многих эфирных маслах.[1][4].
Методы синтеза альдегидов
Лабораторные методы получения альдегидов
Окислительные методы
- Для получения альдегидов в лабораторных условиях часто используется реакция окисления первичных спиртов реагентами, представляющими собой комплексные соединения оксида хрома(VI) с третичными аминами, в частности, лучшими реагентами являются комплекс с пиридином (CrO3 · 2C5H5N, реагент Саррета — Коллинза) и хлорхромат пиридиния (C5H5N+CrO3Cl-, реагент Кори, PCC). Данные реагенты позволяют получать альдегиды с высоким выходом, а хлорхромат пиридиния также не затрагивает двойную связь. Для этих же целей применяют и другие селективные окислители, например оксид марганца(IV) MnO2, карбонат серебра на цеолите, а также диметилсульфоксид в присутствии основания (окисление по Сверну[en])[10].
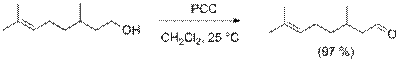
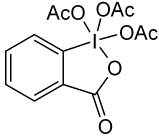
Периодинан Десса-Мартина
- Реакция окисления периодинаном Десса-Мартина. Первичные спирты при этом селективно окисляются до альдегидов.[11]
R − C H 2 O H → D M P R − C H O {\displaystyle {\mathsf {R{-}CH_{2}OH{\xrightarrow[{DMP}]{}}R{-}CHO}}} 
- Как метод получения альдегидов может использоваться восстановительный озонолиз симметричных дизамещённых алкенов либо циклических алкенов (в данном случае реакция приводит в образованию диальдегида). Аналогичное превращение может быть проведено под действием смеси OsO4 и NaIO4[12].
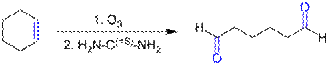
- Также к данному типу реакций относится окисление вицинальных диолов йодной кислотой или тетраацетатом свинца[13].
C H 2 ( O H ) − C H 2 ( O H ) → H I O 4 2 C H 2 O {\displaystyle {\mathsf {CH_{2}(OH){-}CH_{2}(OH){\xrightarrow[{HIO_{4}}]{}}2CH_{2}O}}} 
- Важным методом также является гидроборирование — окисление алкинов, в ходе которого к алкину против правила Марковникова присоединяется диалкилборан (например, дисиамилборан), а полученный продукт окисляется щелочным раствором пероксида водорода, что приводит к образованию альдегида[14].
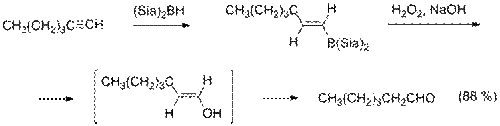
Восстановительные методы
Ряд производных карбоновых кислот (хлорангидриды, сложные эфиры, нитрилы, амиды) могут быть восстановлены до альдегидов под действием специфических восстановителей[15].
- Так, например, в реакции Розенмунда хлорангидриды восстанавливают под действием водорода на палладиевом катализаторе. Аналогичное превращение можно провести под действием три(трет-бутокси)алюмогидрида лития[16].
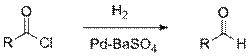
- Сложные эфиры селективно восстанавливаются до альдегидов под действием диизобутилалюминийгидрида[17].
