Константа гидролиза. Степень гидролиза, связь степени гидролиза с константой гидролиза и концентрацией раствора. Факторы, определяющие глубину гидролиза солей. Совместный гидролиз.
Гидролиз характеризуют степенью гидролиза аг. Это величина, равная отношению числа молекул (или их концентрации Сг), подвергшихся гидролизу, к общему количеству растворенных молекул соли (или их концентрации С): аг = Сг / С.
По существу степень гидролиза представляет собой долю молекул, подвергшихся гидролизу, от общего количества растворенных молекул соли.
Повышение температуры раствора соли во всех случаях приводит к усилению гидролиза, так как гидролиз ― эндотемический процесс (обратный нейтрализации).
Разбавление растворов также смещает равновесие в сторону образования продуктов гидролиза.
К гидролизу, как к равновесному процессу, можно применить закон действующих масс. Например, гидролиз ацетата натрия протекает в соответствии
с уравнением:
NaCH3COO + HOН ↔ NaOH + CH3COOH,
или в ионной форме:
CH3COO- + H+OH- ↔ OH- + CH3COOH.
Константа равновесия Кр для процесса гидролиза запишется в виде выражения:
[CH3COOH] ⋅ [OH−]
Кр = ——————————,
[CH3COO−] ⋅ [H2O]
или, принимая во внимание, что концентрация воды практически остается постоянной величиной,
[CH3COOH] ⋅ [OH−]
Кр⋅ [H2O] = ——————————.
[CH3COO−]
Постоянную величину Кр⋅[H2O] называют константой гидролиза Кг:
[CH3COOH] ⋅ [OH−]
Кг = Кр[H2O] = ————————— .
[CH3COO−]
Она не зависит от концентрации ионов в растворе, но зависит от температуры и природы веществ раствора. Последнее выражение константы гидролиза можно
упростить, если умножить числитель и знаменатель выражения на концентрацию ионов водорода [H+], тогда получим следующее выражение:
[OH−] ⋅ [ H+] ∙ [CH3COOH] Kн2о
Кг = —————————————— = ————— ,
[CH3COO- ] ⋅ [ H+ ] K дис.кислоты
где Kн2о ─ ионное произведение воды, равное [H+]⋅[OH-]; Кдис. кислоты – константа диссоциации кислоты, равная
[CH3COO−] ⋅ [ H+]
Кдис. кислоты = —————————.
[CH3COOH ]
По аналогии для гидролиза соли слабого основания и сильной кислоты (например, NH4Cl) получим:
Kн2о
Кг = —————————,
K дис. основания
где Кдис. основания – константа диссоциации основания.
Таким образом, зная константы диссоциации слабых электролитов (кислоты или основания) и ионное произведение воды, можно рассчитать константы гидролиза соответствующих солей.
Степень аг и константа Кг гидролиза связаны между собой для бинарного электролита соотношением (подобным таковому для степени и константы диссоциации):
Кг = αГ 2С/1−αГ, где С – концентрация соли, моль/л. Обычно степень гидролиза аг значительно
меньше единицы, поэтому приведенное выражение можно упростить : Кг ≈ аг2 С.
Откуда в явном виде степень гидролиза соли равна: аг = 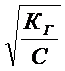 .
.
Принимая во внимание, что константа гидролиза соли определяется через ионное произведение воды и константы диссоцииации слабых электролитов (основания или кислоты, образующихся при гидролизе), можно степень гидро-
лиза представить и в таком виде:
аг = 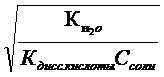 или аг =
или аг = 
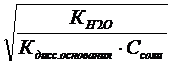
Использование вышеприведенных соотношений дает возможность рассчитать и степень гидролиза, и рН раствора соли.
Окислительно-восстановительные реакции (ОВР). Основные типы ОВР. Типичные окислители и восстановители. Составление уравнений ОВР
методом электронного и ионно-электронного баланса.
Окислительно-восстановительными называются реакции, в результате которых изменяются степени окисления атомов химических элементов, входящих в состав реагирующих веществ.
Окисление- это процесс отдачи атомом электронов, сопровождающийся повышением его степени окисления. Присоединение атомом электронов, приводящее к понижению его степени окисления, называется восстановлением.
Окислительно-восстановительные реакции подразделяются на следующие виды:
а) межмолекулярного окисления-восстановления, т. е. реакции, в которых окислитель и восстановитель входят в состав разных веществ (Fe0 + 2H+Cl = Fe+2Cl2 + H02 );
б)диспропорционирования, т. е. реакции, которые идут с изменением степени окисления атомов одного и того же элемента (Cl20 + 2KOH = KCl- + KCl+O + H2O);
в)внутримолекулярные , т. е. реакции, в которых атомы различных элементов, изменяющие свои степени окисления, входят в состав одного соединения
(N-3H4N+3 O2 = N20 + 3H2O).
Типичные восстановители: металлы, водород, уголь, окись углерода (II) (CO), сероводород (H2S); оксид серы (IV) (SO2); сернистая кислота H2SO3 и ее соли, галогеноводородные кислоты и их соли, катионы металлов в низших степенях окисления: SnCl2, FeCl2, MnSO4, Cr2(SO4)3; азотистая кислота HNO2; аммиак NH3; гидразин NH2NH2; оксид азота(II) (NO); Катод при электролизе.
Типичные окислители: галогены, перманганат калия(KMnO4); манганат калия (K2MnO4); оксид марганца (IV) (MnO2), дихромат калия (K2Cr2O7);
хромат калия (K2CrO4), азотная кислота (HNO3), серная кислота (H2SO4) конц, оксид меди(II) (CuO); оксид свинца(IV) (PbO2); оксид серебра (Ag2O); пероксид водорода (H2O2), хлорид железа(III) (FeCl3), бертоллетова соль (KClO3), анод при электролизе.
Составление ОВР методом электронного баланса:
Электронный баланс - метод нахождения коэффициентов в уравнениях окислительно-восстановительных реакций, в котором рассматривается обмен электронами между атомами элементов, изменяющих свою степень окисления. Число электронов, отданное восстановителем равно числу электронов, получаемых окислителем.
Уравнение составляется в несколько стадий:
1. Записывают схему реакции.
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
2. Проставляют степени окисления над знаками элементов, которые меняются.
KMn+7O4 + HCl-1 → KCl + Mn+2Cl2 + Cl20 + H2O
3. Выделяют элементы, изменяющие степени окисления и определяют число электронов, приобретенных окислителем и отдаваемых восстановителем.
Mn+7 + 5ē = Mn+2
2Cl-1 - 2ē = Cl20
4. Уравнивают число приобретенных и отдаваемых электронов, устанавливая тем самым коэффициенты для соединений, в которых присутствуют элементы, изменяющие степень окисления.
Mn+7 + 5ē = Mn+2 2
2Cl-1 - 2ē = Cl20 5
––––––––––––––––––––––––
2Mn+7 + 10Cl-1 = 2Mn+2 + 5Cl20
5. Подбирают коэффициенты для всех остальных участников реакции. При этом 10 молекул HCl участвуют в восстановительном процессе, а 6 в - ионообменном (связывание ионов калия и марганца).
2KMn+7O4 + 16HCl-1 = 2KCl + 2Mn+2Cl2 + 5Cl20 + 8H2O
Составление ОВР методом ионно-электронного баланса:
1. Записывают схему реакции.
K2SO3 + KMnO4 + H2SO4 → K2SO4 + MnSO4 + H2O
2. Записывают схемы полуреакций, с использованием реально присутствующих частиц (молекул и ионов) в растворе. При этом подводим материальный баланс, т.е. количество атомов элементов участвующих в полуреакции в левой части должно быть равно их количеству в правой. В зависимости от характера среды используют следующие правила стягивания избыточных ионов водорода и кислорода:
а. Избыточные ионы кислорода ( О ) в кислой среде образуют ( стягивают ) с ионами Н малодиссоциированные молекулы воды:
О + 2Н = Н2О.
б. Избыточные ионы кислорода в нейтральной или щелочной среде стягиваются с молекулами воды, образуя ОН группы:
О + НОН = 2ОН.
в. Избыточные ионы водорода ( Н ) в щелочной среде стягиваются с ионами ОН, образуя молекулы воды :
Н + ОН = Н2О
г. Недостающие ионы кислорода ( О ) в кислой и нейтральной средах берутся из молекул воды с образованием ионов Н :
Н2О – О = 2Н.
д. Недостающие ионы кислорода ( О ) в щелочной среде берутся из групп ОН с образованием молекул Н2О :
2ОН - О = Н2О.
е. Недостающие ионы Н в щелочной среде берутся из молекул воды с образованием ионов гидроксила:
Н2О – Н = ОН
MnO4- + 8H+ → Mn2+ + 4H2O восстановление
SO32- + H2O → SO42- + 2H+ окисление
3. Подводим электронный баланс, следуя необходимости равенства суммарного заряда в правой и левой частях уравнений полуреакций.
В приведенном примере в правой части уравнения полуреакции восстановления суммарный заряд ионов равен +7, в левой — +2, значит в правой части необходимо добавить пять электронов:
MnO4- + 8H+ + 5ē → Mn2+ + 4H2O
В уравнении полуреакции окисления суммарный заряд в правой части равен -2, в левой 0, значит в правой части необходимо вычесть два электрона:
SO32- + H2O – 2ē → SO42- + 2H+
Таким образом, в обоих уравнениях осуществлен ионно-электронный баланс и можно в них вместо стрелок поставить знаки равенства:
MnO4- + 8H+ + 5ē = Mn2+ + 4H2O
SO32- + H2O – 2ē = SO42- + 2H+
4. Следуя правилу о необходимости равенства количества электронов принятых окислителем и отданных восстановителем, находим наименьшее общее кратное для количеств электронов в обоих уравнениях (2∙5 = 10).
MnO4- + 8H+ + 5ē = Mn2+ + 4H2O 2
SO32- + H2O – 2ē = SO42- + 2H+ 5
5. Умножаем на коэффициенты (2,5) и суммируем оба уравнения.
MnO4- + 8H+ + 5ē = Mn2+ + 4H2O 2
SO32- + H2O – 2ē = SO42- + 2H+ 5
––––––––––––––––––––––––––––––––––––––––––––––
2MnO4- + 16H+ + 5SO32- + 5H2O = 2Mn2+ + 8H2O + 5SO42- + 10H+
или, суммируя (вычитая) одинаковые молекулы и ионы, получаем:
2MnO4- + 6H+ + 5SO32- = 2Mn2+ + 3H2O + 5SO42-
или в молекулярной форме:
5K2SO3 + 2KMnO4 + 3H2SO4 = 6K2SO4 + 2MnSO4 + 3H2O
В этом методе рассматривают переход электронов от одних атомов или ионов к другим с учетом характера среды (кислая, щелочная или нейтральная), в которой протекает реакция.
Электродный потенциал. Понятие о двойном электрическом слое и скачке потенциала на границе металл-раствор соли металла. Водородный электрод как электрод сравнения. Схема измерения электродного потенциала. Стандартные электродные потенциалы для металлов (ряд напряжений металлов). Уравнение Нернста.
Ряд стандартных электродных потенциалов:Если пластинку металла, погруженную в раствор его соли с концентрацией ионов металла, равной 1 моль/л, соединить со стандартным водородным электродом, то получится гальванический элемент. Электродвижущая сила этого элемента (ЭДС), измеренная при 25 °С, и характеризует стандартный электродный потенциал металла, обозначаемый обычно как Е° или φ°.
Стандартные потенциалы электродов, выступающих как восстановители по отношению к водороду, имеют знак “-”, а знак “+” имеют стандартные потенциалы электродов, являющихся окислителями.
Металлы, расположенные в порядке возрастания их стандартных электродных потенциалов, образуют так называемый электрохимический ряд напряжений металлов: Li, Rb, К, Ва, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H, Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au.
Значение стандартного электродного потенциала водородного электрода, являющегося электродом сравнения и соответствующего процессу: 2Н+ + 2е = Н2, принято равным нулю.
Ряд напряжений характеризует химические свойства металлов:
1. Чем более отрицателен электродный потенциал металла, тем больше его восстановительная способность.
2. Каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые стоят в электрохимическом ряду напряжений металлов после него.
3. Все металлы, имеющие отрицательный стандартный электродный потенциал, т. е. находящиеся в электрохимическом ряду напряжений металлов левее водорода, способны вытеснять его из растворов кислот.
Как и в случае определения значения Е° металлов, значения Е° неметаллов измеряются при температуре 25 °С и при концентрации всех атомных и молекулярных частиц, участвующих в равновесии, равной 1 моль/л.
Алгебраическое значение стандартного окислительно-восстановительного потенциала характеризует окислительную активность соответствующей окисленной формы.
Величина электродного потенциала окислительно-восстановительной системы зависит от концентрации окисленной и восстановленной формы и температуры. Эта зависимость выражается уравнением Нернста:
Е(Ox/Red) = Е°(Ox/Red) + 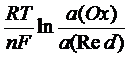 , где
, где
Е(Ox/Red) - искомый потенциал окислительно-восстановительной системы (в вольтах)
Е°(Ox/Red) - ее стандартный потенциал
R – универсальная газовая постоянная (8,324 Дж/моль∙К)
T – абсолютная температура
F – постоянноя Фарадея (96485 Кл/моль)
n – количество электронов передаваемых от окисленной формы к восстановленной
a(Ox) и a(Red) активности окисленной и восстановленной формы соответственно. В случае разбавленных растворов (ионная сила растворов близка к нулю) вместо активностей можно использовать их молярные концентрации:
Е(Ox/Red) = Е°(Ox/Red) + 
При температуре Т = 298° К, подставляя численные значения R и F, используя десятичный логарифм вместо натурального (ln(a) = 2,3∙lg(a)) получаем:
Е(Ox/Red) = Е°(Ox/Red) + 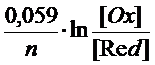
Для системы металл/раствор соли данного металла с учетом того, что активность гетерофазы [Red] величина постоянная и равна единице уравнение принимает вид:
Е(Меn+/Me) = Е°(Меn+/Ме) + 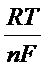 ∙ ln[Меn+] = Е°(Меn+/Ме) +
∙ ln[Меn+] = Е°(Меn+/Ме) + 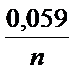 ∙ ln[Меn+]
∙ ln[Меn+]
Если в уравнение полуреакции входит протон или гидроксид-ион, то величина электродного потенциала зависит и от рН среды.
Например, для полуреакции: МnО4- +8Н+ + 5е- = Мn2+ + 4Н2О потенциал рассчитывается по формуле:
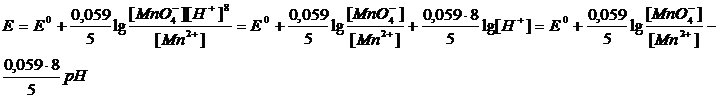 Как уже отмечалось, для водных растворов в качестве стандартного электрода обычно используют водородный электрод (Pt, Н2[0,101 МПа] | Н+[a= 1]), потенциал которого при давлении водорода 0,101 МПа и термодинамич. активности а ионов Н+ в растворе, равной 1, принимают условно равным нулю (водородная шкала Э. п.).
Как уже отмечалось, для водных растворов в качестве стандартного электрода обычно используют водородный электрод (Pt, Н2[0,101 МПа] | Н+[a= 1]), потенциал которого при давлении водорода 0,101 МПа и термодинамич. активности а ионов Н+ в растворе, равной 1, принимают условно равным нулю (водородная шкала Э. п.).
Величина потенциала любого водородного электрода (соответствующего полуреакции 2Н+ + 2е = Н2), принимая активность водорода (Н2) равной единице, рассчитывается по формуле:
Е(Н+/Н2) = Е0 (Н+/Н2) + 0,059 ∙ lg[H+].
С учетом того, что стандартный потенциал Е0 (Н+/Н2) равен нулю, а lg[H+] = -рН получаем:
Е(Н+/Н2) = - 0,059 ∙ рН.
Процессы коррозии и другие процессы окисления протекающие под действием атмосферного кислорода и воды соответствуют полуреакции:
О2 + 4Н+ + 4е = 2Н2О Е0 = 1,228 В.
Уравнение Нернста для этого процесса:
Е = Е0 +0,059 ∙ lg[H+] + (0,059/4) ∙ lgP(O2), или Е = Е0 - 0,059 ∙ рН + (0,059/4) ∙ lgP(O2)
где P(O2) – парциальное давление кислорода. Если парциальное давление кислорода равно одной атмосфере, то уравнение принимает вид:
Е = Е0 - 0,059 ∙ рН
Окислительно-восстановительные системы с инертными электродами. Стандартные окислительно-восстановительные потенциалы и оценка направления самопроизвольного протекания ОВР. Выбор окислителей и восстановителей с учетом стандартных потенциалов.
Стандартные потенциалы окислительно-восстановительных реакций: Возможность протекания любой окислительно-восстановительной реакции в реальных условиях обусловлена рядом причин: температурой, природой окислителя и восстановителя, кислотностью среды, концентрацией веществ, участвующих в реакции, и т. д. Учесть все эти факторы бывает трудно, но, помня о том, что любая окислительно-восстановительная реакция протекает с переносом электронов от восстановителя к окислителю, можно установить критерий возможности протекания такой реакции.
Количественной характеристикой окислительно-восстановительных процессов являются нормальные окислительно-восстановительные потенциалы окислителей и восстановителей (или стандартные потенциалы электродов).
Чтобы понять физико-химический смысл таких потенциалов, необходимо проанализировать так называемые электрохимические процессы.
Химические процессы, сопровождающиеся возникновением электрического тока или вызываемые им, называются электрохимическими.
Чтобы понять природу электрохимических процессов, обратимся к рассмотрению нескольких достаточно простых ситуаций. Представим себе металлическую пластинку, погруженную в воду. Под действием полярных молекул воды ионы металла отрываются от поверхности пластинки и гидратированными переходят в жидкую фазу. Последняя при этом заряжается положительно, а на металлической пластинке появляется избыток электронов. Чем дальше протекает процесс, тем больше становится заряд, как пластинки, так и жидкой фазы.
Благодаря электростатическому притяжению катионов раствора и избыточных электронов металла на границе раздела фаз возникает так называемый двойной электрический слой, который тормозит дальнейший переход ионов металла в жидкую фазу. Наконец, наступает момент, когда между раствором и металлической пластинкой устанавливается равновесие, которое можно выразить уравнением:
Ме0 – ne- ↔ Men+
или с учетом гидратации ионов в растворе:
Ме0 – ne- + mH2O ↔ Men+ ∙ mH2O
Состояние этого равновесия зависит от природы металла, концентрации его ионов в растворе, от температуры и давления.
При погружении металла не в воду, а в раствор соли этого металла равновесие в соответствии с принципом Ле Шателье смещается влево и тем больше, чем выше концентрация ионов металла в растворе. Активные металлы, ионы которых обладают хорошей способностью переходить в раствор, будут в этом случае заряжаться отрицательно, хотя в меньшей степени, чем в чистой воде.
Равновесие можно сместить вправо, если тем или иным способом удалять электроны из металла. Это приведет к растворению металлической пластинки. Наоборот, если к металлической пластинке подводить электроны извне, то на ней будет происходить осаждение ионов из раствора.
При погружении металла в раствор на границе раздела фаз образуется двойной электрический слой. Разность потенциалов, возникающую между металлом и окружающей его жидкой фазой, называют электродным потенциалом. Этот потенциал является характеристикой окислительно-восстановительной способности металла в виде твердой фазы.
У изолированного металлического атома (состояние одноатомного пара, возникающее при высоких температурах и высоких степенях разрежения) окислительно-восстановительные свойства характеризуются другой величиной, называемой ионизационным потенциалом. Ионизационный потенциал — это энергия, необходимая для отрыва электрона от изолированного атома.
Абсолютное значение электродного потенциала нельзя измерить непосредственно. Вместе с тем не представляет труда измерение разности электродных потенциалов, которая возникает в системе, состоящей из двух пар металл - раствор. Такие пары называют полуэлементами. Условились определять электродные потенциалы металлов по отношению к так называемому стандартному водородному электроду, потенциал которого произвольно принят за ноль. Стандартный водородный электрод состоит из специально приготовленной платиновой пластинки, погруженной в раствор кислоты с концентрацией ионов водорода 1 моль/л и омываемой струёй газообразного водорода под давлением 105 Па, при температуре 25 °С.
Ряд стандартных электродных потенциалов:Если пластинку металла, погруженную в раствор его соли с концентрацией ионов металла, равной 1 моль/л, соединить со стандартным водородным электродом, то получится гальванический элемент. Электродвижущая сила этого элемента (ЭДС), измеренная при 25 °С, и характеризует стандартный электродный потенциал металла, обозначаемый обычно как Е° или φ°.
Стандартные потенциалы электродов, выступающих как восстановители по отношению к водороду, имеют знак “-”, а знак “+” имеют стандартные потенциалы электродов, являющихся окислителями.
Металлы, расположенные в порядке возрастания их стандартных электродных потенциалов, образуют так называемый электрохимический ряд напряжений металлов: Li, Rb, К, Ва, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H, Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au.
Значение стандартного электродного потенциала водородного электрода, являющегося электродом сравнения и соответствующего процессу: 2Н+ + 2е = Н2, принято равным нулю.
Ряд напряжений характеризует химические свойства металлов:
1. Чем более отрицателен электродный потенциал металла, тем больше его восстановительная способность.
2. Каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые стоят в электрохимическом ряду напряжений металлов после него.
3. Все металлы, имеющие отрицательный стандартный электродный потенциал, т. е. находящиеся в электрохимическом ряду напряжений металлов левее водорода, способны вытеснять его из растворов кислот.
Как и в случае определения значения Е° металлов, значения Е° неметаллов измеряются при температуре 25 °С и при концентрации всех атомных и молекулярных частиц, участвующих в равновесии, равной 1 моль/л.
Алгебраическое значение стандартного окислительно-восстановительного потенциала характеризует окислительную активность соответствующей окисленной формы.
Количественным критерием оценки возможности протекания той или иной окислительно-восстановительной реакции является положительное значение разности стандартных окислительно-восстановительных потенциалов полуреакций окисления и восстановления.
Стандартные электродные потенциалы окислительно-восстановительных систем:
| окисленная форма | количество электронов | восстановленная форма | Е0, В |
| F2 | 2e | 2F- | 2,87 |
| O3 + 2H+ | 2e | O2 + H2O | 2,07 |
| H2O2 + 2H+ | 2e | 2H2O | 1,77 |
| Au+ | 1e | Au | 1,68 |
| MnO4- + 8H+ | 5e | Mn2+ + 4H2O | 1,51 |
| HClO + H+ | 2e | Cl- + H2O | 1,50 |
| PbO2 + 4H+ | 2e | Pb2+ + 2H2O | 1,46 |
| ClO3- + 6H+ | 6e | Cl- + 3H2O | 1,45 |
| ClO4- + 8H+ | 8e | Cl- + 4H2O | 1,38 |
| Cl2 | 2e | 2Cl- | 1,34 |
| Cr2O72- + 14H+ | 6e | 2Cr3+ + 7H2O | 1,33 |
| MnO2 + 4H+ | 2e | Mn2+ + 2H2O | 1,23 |
| Pt2+ | 2e | Pt | 1,20 |
| Br2 | 2e | 2Br- | 1,07 |
| HNO2 + H+ | 1e | NO + H2O | 1,00 |
| NO3- + 4H+ | 3e | NO + 2H2O | 0,96 |
| Hg2+ | 2e | Hg | 0,84 |
| Ag+ | 1e | Ag | 0,80 |
| NO3- + 2H+ | 1e | NO2 + H2O | 0,80 |
| Fe3+ | 1e | Fe2+ | 0,77 |
| O2 + 2H+ | 2e | H2O2 | 0,68 |
| MnO4- + 2H2O | 3e | MnO2 + 4OH- | 0,60 |
| I2 | 2e | 2I- | 0,54 |
| Cu2+ | 2e | Cu | 0,34 |
| SO42- + 2H+ | 2e | SO32- + H2O | 0,22 |
| Sb3+ | 3e | Sb | 0,20 |
| SO42- + 2H+ | 2e | SO2 + H2O | 0,17 |
| Cu2+ | 1e | Cu+ | 0,16 |
| Cu+ | 1e | Cu | 0,15 |
| S + 2H+ | 2e | H2S | 0,14 |
| 2H+ | 2e | H2 | 0,0000 |
| Fe3+ | 3e | Fe | -0,06 |
| Se + 2H+ | 2e | H2Se | -0,08 |
| CrO42- + 4H2O | 3e | [Cr(OH)6]3- + 5OH- | -0,13 |
| Pb2+ | 2e | Pb | -0,13 |
| Sn2+ | 2e | Sn | -0,14 |
| O2 + 2H2O | 2e | H2O2 | -0,15 |
| Ni2+ | 2e | Ni | -0,23 |
| Co2+ | 2e | Co | -0,29 |
| Cd2+ | 2e | Cd | -0,40 |
| Cr3+ | 1e | Cr2+ | -0,41 |
| Fe2+ | 2e | Fe | -0,44 |
| Cr3+ | 3e | Cr | -0,74 |
| Zn2+ | 2e | Zn | -0,76 |
| 2H2O | 2e | H2 +2OH- | -0,83 |
| Cr2+ | 2e | Cr | -0,91 |
| Mn2+ | 2e | Mn | -1,18 |
| [Zn(OH)4]2- | 2e | Zn +4OH- | -1,20 |
| Al3+ | 3e | Al | -1,66 |
| U3+ | 3e | U | -1,80 |
| H2 | 2e | 2H- | -2,23 |
| [Al(OH)4]- | 3e | Al + 4OH- | -2,33 |
| Mg2+ | 2e | Mg | -2,37 |
| Na+ | 1e | Na | -2,71 |
| Ca2+ | 2e | Ca | -2,87 |
| Sr2+ | 2e | Sr | -2,89 |
| Ba2+ | 2e | Ba | -2,91 |
| K+ | 1e | K | -2,92 |
| Cs+ | 1e | Cs | -2,92 |
| Rb+ | 1e | Rb | -2,92 |
| Li+ | 1e | Li | -3,01 |
Комплексные соединения. Основные положения координационной теории. Строение комплексного соединения: комплексообразователь, лиганды, внешняя и внутренняя сфера. Координационное число и степень окисления иона-комплексообразователя. Заряд комплексного иона.
Комплексные соединения называют часто координационными соединениями, подчеркивая тем самым способность простых неизменных частиц определенным образом располагаться (координироваться) друг около друга в комплексном ионе или комплексной молекуле.
Природу химических связей в комплексах, их строение и принципы их образования объясняет координационная теория.
Метод валентных связей предполагает sp3d2-гибридизацию валентных орбиталей кобальта. Такая структура соответствует геометрической фигуре октаэдр.
В представлении теории кристаллического поля d–подуровень расщепляется на два новых подуровня в октаэдрическом поле лигандов, причем, расщепление в слабом поле лигандов, которое создают анионы фтора (F-), относящиеся (как и анионы всех галогенов типа Х-) к лигандам области слабого поля. Так как расщеплением можно пренебречь, правило Хунда распространяется на все пять d-орбиталей иона кобальта и заполнение орбиталей в комплексном анионе [СоF6]3- будет таким же как и в свободном ионе Со3+. Всего одна пара и четыре неспаренных d-электрона. Комплекс парамагнитен. Если сменить лиганд слабого поля на лиганд сильного поля, например фторид на цианид-ион относящийся к лигандам сильного поля, в комплексном анионе [Co(CN)6]3- все шесть d-электронов катиона кобальта будут находиться на трех нижних орбиталях dε. Комплекс диамагнитен – все электроны спарены.
Основы современной координационной теории были изложены в конце прошлого века швейцарским химиком Альфредом Вернером, обобщившим в единую систему весь накопившийся к тому времени экспериментальный материал по комплексным соединениям. Им были введены понятия о центральном атоме (комплексообразователь) и его координационном числе, внутренней и внешней сфере комплексного соединения, изомерии комплексных соединений, предприняты попытки объяснения природы химической связи в комплексах.
Все основные положения координационной теории Вернера используются и в настоящее время.
Комплексообразователь: Образование комплексного иона или нейтрального комплекса можно представить себе в виде обратимой реакции общего типа:
M + nL =[MLn]
где M – нейтральный атом, положительно или отрицательно заряженный условный ион, объединяющий (координирующий) вокруг себя другие атомы, ионы или молекулы L. Атом M получил название комплексообразователя или центрального атома.
В комплексных ионах [Cu(NH3)4]2+, [SiF6]2- , [Fe(CN)6]4-,[BF4]- комплексообразователями являются медь(II), кремний(IV), железо(II), бор(III).
Чаще всего комплексообразователем служит атом элемента в положительной степени окисления.
Отрицательные условные ионы (т.е. атомы в отрицательной степени окисления) играют роль комплексообразователей сравнительно редко. Это, например, атом азота(-III) в катионе аммония [NH4]+ и т.п.
Атом-комплексообразователь может обладать нулевой степенью окисления. Так, карбонильные комплексы никеля и железа, имеющие состав [Ni(CO)4] и [Fe(CO)5], содержат атомы никеля(0) и железа(0).
Комплексообразователь (выделен желтым цветом) может участвовать в реакциях получения комплексов, как будучи одноатомным ионом, например:
Ag+ + 2NH3 = [Ag(NH3)2]+;
Ag+ + 2CN- = [Ag(CN)2]-
так и находясь в составе молекулы:
SiF4 + 2F- =[SiF6]2-;
I2 + I- = [I(I)2]-;
PH3 + H+ =[PH4]+;
BF3 + NH3 =[B(NH3)F3]
В комплексной частице может быть два и более атомов-комплексообразователей. В этом случае говорят о многоядерных комплексах.
Комплексное соединение может включать несколько комплексных ионов, в каждом из которых содержится свой комплексообразователь.
Например, в одноядерном комплексном соединении состава [Cu(NH3)4][PtCl6]комплексообразователи – Cu(II) и Pt(IV).
Лиганды:В комплексном ионе или нейтральном комплексе вокруг комплексообразователя координируются ионы, атомы или простые молекулы (L). Все эти частицы, имеющие химические связи с комплексообразователем, называются лигандами (от латинского "ligare" - связывать). В комплексных ионах [SnCl6]2- и [Fe(CN)6]4- лигандами являются ионы Cl- и CN-, а в нейтральном комплексе [Cr(NH3)3(NCS)3] лиганды – молекулы NH3 и ионы NCS-.
Лиганды, как правило, не связаны друг с другом, и между ними действуют силы отталкивания. Лигандами могут быть различные неорганические и органические ионы и молекулы. Важнейшими лигандами являются ионы CN-, F- , Cl-, Br-, I-, NO2-, OH-, SO3,S2-, C2O42-, CO32-, молекулы H2O, NH3, CO, карбамида (NH2)2CO, органических соединений – этилендиамина NH2CH2CH2NH2, a-аминоуксусной кислоты NH2CH2COOH и этилендиаминтетрауксусной кислоты (ЭДТА)и другие.
Дентатность лиганда: Чаще всего лиганд бывает связан с комплексообразователем через один из своих атомов одной двухцентровой химической связью. Такого рода лиганды получили название монодентатных. К числу монодентатных лигандов относятся все галогенид-ионы, цианид-ион, аммиак, вода и другие. Некоторые распространенные лиганды типа молекул воды H2O, гидроксид-иона OH-, тиоцианат-иона NCS-, амид-иона NH2-, монооксида углерода CO в комплексах преимущественно монодентатны, хотя в отдельных случаях (в мостиковых структурах) становятся бидентатными.
Существует целый ряд лигандов, которые в комплексах являются практически всегда бидентатными. Это этилендиамин, карбонат-ион, оксалат-ион и т.п. Каждая молекула или ион бидентатного лиганда образует с комплексообразователем две химические связи в соответствии с особенностями своего строения.
Например, в комплексном соединении [Co(NH3)4CO3]NO3 бидентатный лиганд – ион CO32- - образует две связи с комплексообразователем – условным ионом Co(III), а каждая молекула лиганда NH3 – только одну связь.
Полидентатные лиганды могут выступать в роли мостиковых лигандов, объединяющих два и более центральных атома.
Координационное число: Важнейшей характеристикой комплексообразователя является количество химических связей, которые он образует с лигандами, или координационное число (КЧ). Эта характеристика комплексообразователя определяется главным образом строением его электронной оболочки и обусловливается валентными возможностями центрального атома или условного иона-комплексообразователя.
Когда комплексообразователь координирует монодентатные лиганды, то координационное число равно числу присоединяемых лигандов. А число присоединяемых к комплексообразователю полидентатных лигандов всегда меньше значения координационного числа.
Значение координационного числа комплексообразователя зависит от его природы, степени окисления, природы лигандов и условий (температуры, природы растворителя, концентрации комплексообразователя и лигандов и др.), при которых протекает реакция комплексообразования. Значение КЧ может меняться в различных комплексных соединениях от 2 до 8 и даже выше. Наиболее распространенными координационными числами являются 4 и 6.
Между значениями координационного числа и степенью окисления элемента-комплексообразователя существует определенная зависимость. Так, для элементов-комплексообразователей, имеющих степень окисления +I [Ag(I), Cu(I), Au(I), (II) и др.] наиболее характерно координационное число 2 – например, в комплексах типа [Ag(NH3)2]+, [Cu(CN)2]-, [IBr2]-.
Элементы-комплексообразователи со степенью окисления +II [Zn(II), Pt(II), Pd(II), Cu(II) и др.) часто образуют комплексы, в которых проявляют координационное число 4, такие как [Zn(NH3)4]2+, [PtCl4]2-, [Pd(NH3)2Cl2]0, [ZnI4]2-, [Cu(NH3)4]2+.
В аквакомплексах координационное число комплексообразователя в степени окисления +II чаще всего равно 6: [Fe(H2O)6]2+, [Mg(H2O)6]2+, [Ni(H2O)6]2+.
Элементы-комплексообразователи, обладающие степенью окисления +III и +IV [Pt(IV), Al(III), Co(III), Cr(III), Fe(III)], имеют в комплексах, как правило, КЧ 6.
Например, [Co(NH3)6]3+, [Cr(OH)6]3-, [PtCl6]2- , [AlF6]3-, [Fe(CN)6]3-.
Известны комплексообразователи, которые обладают практически постоянным координационным числом в комплексах разных типов. Таковы кобальт(III), хром(III) или платина(IV) с КЧ 6 и бор(III), платина(II), палладий(II), золото(III) с КЧ 4. Тем не менее большинство комплексообразователей имеет переменное координационное число. Например, для алюминия(III) возможны КЧ 4 и КЧ 6 в комплексах [Al(OH)4]- и [Al(H2O)2(OH)4]-.
Координационные числа 3, 5, 7, 8 и 9 встречаются сравнительно редко. Есть всего несколько соединений, в которых КЧ равно 12 – например, таких как K9[Bi(NCS)12].
Внутренняя и внешняя сфера комплексного соединения:
Лиганды, непосредственно связанные с комплексообразователем, образуют вместе с ним
